
Ciao a tutti! Capisco perfettamente come a volte la chimica, e in particolare la costante universale dei gas, possa sembrare un muro insormontabile. Non preoccupatevi, non siete soli! Molti studenti (e persino qualche genitore!) si sentono allo stesso modo. L'obiettivo di questo articolo è rendere questo concetto accessibile, interessante e, soprattutto, utile. Cercheremo di demistificare la costante dei gas, partendo dalle basi e arrivando a capire il suo significato pratico. Preparatevi a un viaggio entusiasmante nel mondo della chimica!
Che cos'è la Costante Universale dei Gas (R)?
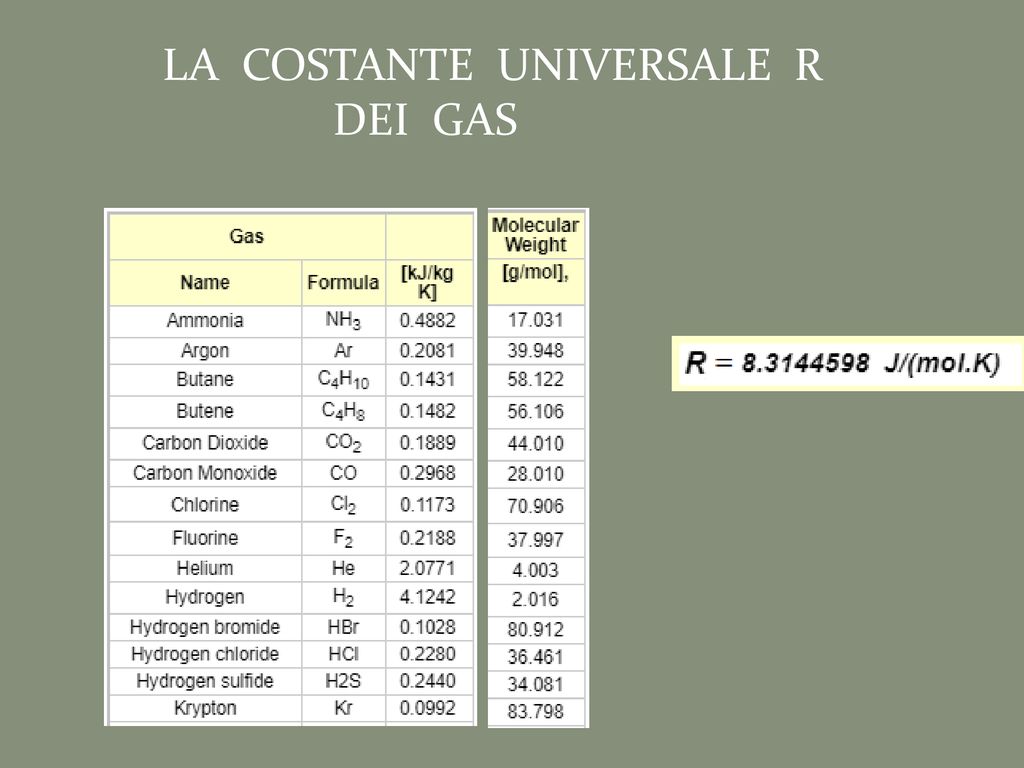
La costante universale dei gas, spesso indicata con la lettera R, è una costante fisica fondamentale che mette in relazione le unità di energia, temperatura, quantità di sostanza (misurata in moli) e volume per i gas ideali. In parole povere, è un numero che ci aiuta a capire come si comportano i gas in diverse condizioni. Non lasciatevi spaventare dalla parola "ideale"; vedremo poi perché è importante.
Immaginate di gonfiare un palloncino. La quantità di aria (e quindi di gas) che ci mettete dentro, la temperatura dell'aria e la pressione all'interno del palloncino sono tutti collegati. La costante R è proprio l'elemento che permette di mettere in relazione tutti questi fattori.
È espressa in diverse unità di misura, ma quella più comunemente usata è 8.314 J/(mol·K) (Joule per mole per Kelvin). Ricordate, le unità di misura sono importanti! Ci dicono di cosa stiamo parlando e come le diverse grandezze sono collegate tra loro.
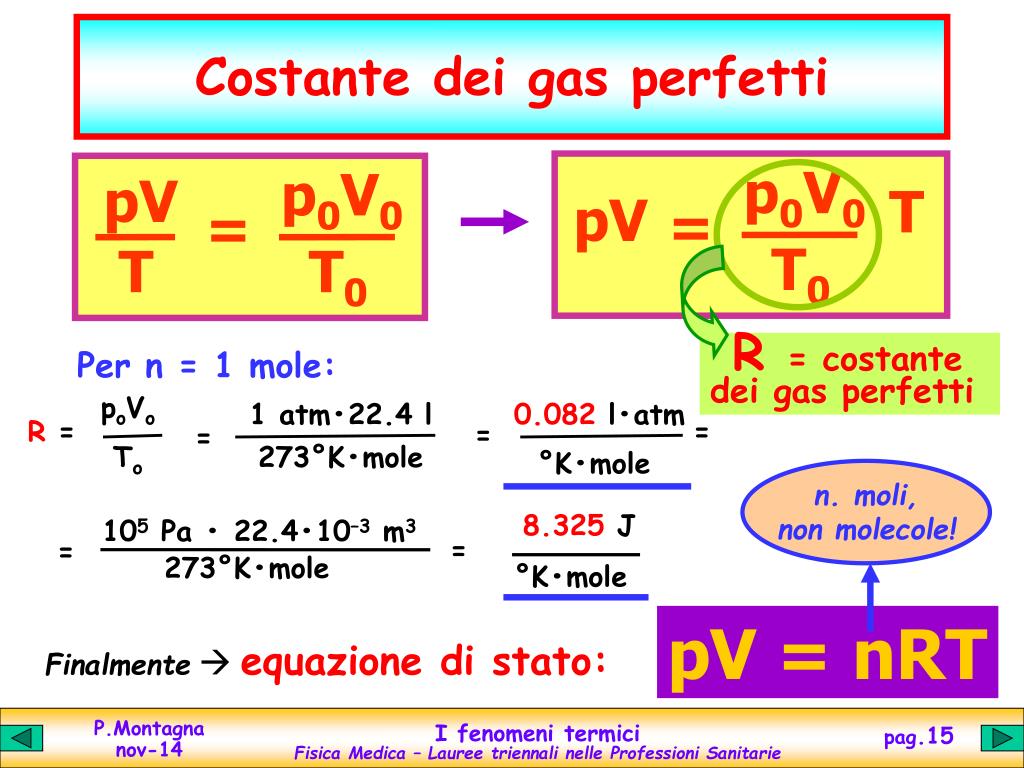
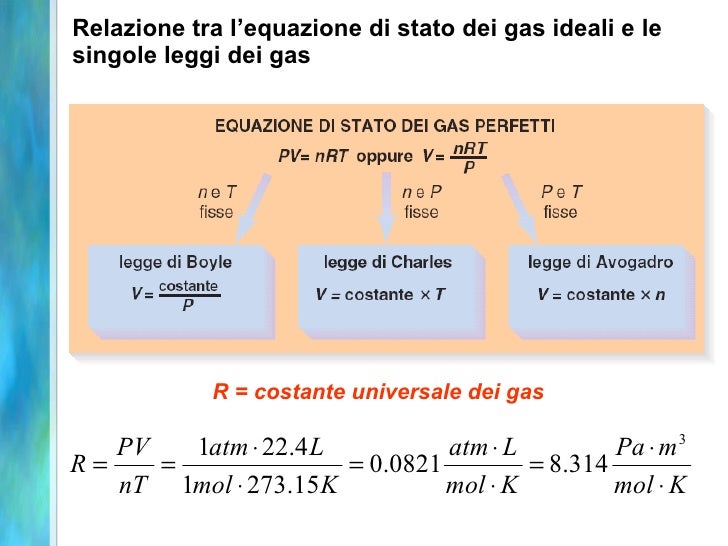
L'Equazione dei Gas Ideali: PV = nRT
La costante R è protagonista di una delle equazioni più importanti della chimica: l'equazione dei gas ideali. Questa equazione ci dice:
PV = nRT
Dove:

- P = Pressione del gas
- V = Volume del gas
- n = Numero di moli del gas
- R = Costante universale dei gas
- T = Temperatura del gas (in Kelvin)
Questa equazione è uno strumento potentissimo! Ci permette di calcolare una di queste variabili se conosciamo le altre. Ad esempio, possiamo calcolare il volume di un gas se conosciamo la sua pressione, la temperatura e il numero di moli.
Perché "Ideali"? E cosa succede nella realtà?
L'equazione dei gas ideali funziona perfettamente... per i gas ideali. Ma cosa significa? Un gas ideale è un gas teorico in cui le molecole non interagiscono tra loro e non occupano spazio. Nella realtà, i gas reali si comportano in modo simile ai gas ideali a basse pressioni e alte temperature. In condizioni estreme (alte pressioni o basse temperature), le interazioni tra le molecole diventano più importanti e l'equazione dei gas ideali non è più precisa.
Tuttavia, l'equazione dei gas ideali è una ottima approssimazione nella maggior parte delle situazioni che incontriamo quotidianamente. È uno strumento fondamentale per capire il comportamento dei gas e per fare calcoli approssimativi.
Un insegnante di chimica delle scuole superiori mi ha raccontato: "Cerco sempre di spiegare ai miei studenti che l'equazione dei gas ideali è come una 'scorciatoia'. Ci dà una risposta rapida e abbastanza precisa nella maggior parte dei casi. Poi, se abbiamo bisogno di maggiore precisione, possiamo usare equazioni più complesse."
Applicazioni Pratiche della Costante R
Ora che abbiamo capito cos'è la costante R e come si usa, vediamo dove la possiamo trovare nella vita di tutti i giorni:
- Gonfiare una gomma di automobile: La pressione delle gomme varia con la temperatura. Usando l'equazione dei gas ideali (e quindi la costante R), possiamo prevedere come cambierà la pressione quando la temperatura esterna aumenta o diminuisce.
- Processi industriali: Molte industrie chimiche utilizzano gas nei loro processi di produzione. La costante R è fondamentale per calcolare la quantità di gas necessaria per una reazione, o per prevedere come cambierà il volume di un gas durante una reazione.
- Meteorologia: La costante R è usata nei modelli meteorologici per prevedere il comportamento dell'atmosfera. La pressione, la temperatura e l'umidità dell'aria sono tutti fattori che influenzano il tempo, e la costante R ci aiuta a metterli in relazione.
- Respirazione: Anche il nostro corpo utilizza gas! Lo scambio di ossigeno e anidride carbonica nei polmoni è regolato da leggi fisiche che coinvolgono la costante R.
Come vedete, la costante R non è solo un numero astratto! È uno strumento potente che ci aiuta a capire e a prevedere il comportamento dei gas in una vasta gamma di situazioni.
Esercizi Pratici per Capire Meglio
Il modo migliore per capire un concetto è metterlo in pratica! Ecco alcuni esercizi che potete provare:
Esercizio 1: Calcolare il Volume di un Gas
Avete 2 moli di azoto (N2) a una pressione di 1 atmosfera e a una temperatura di 25°C (che corrispondono a 298.15 K). Qual è il volume occupato dal gas?
Suggerimento: Usate l'equazione PV = nRT e ricordatevi di usare le unità di misura corrette!
(La risposta è circa 48.9 litri)
Esercizio 2: L'Effetto della Temperatura sulla Pressione
Una gomma di automobile contiene aria a una pressione di 2.2 atmosfere a 20°C. Se la temperatura aumenta a 35°C, qual è la nuova pressione della gomma? (Assumendo che il volume rimanga costante).
Suggerimento: Riorganizzate l'equazione PV = nRT per trovare una relazione tra P e T quando V e n sono costanti.
(La risposta è circa 2.32 atmosfere)
Esercizio 3: Esperimento Domestico - Palloncino che si Gonfia
Prendete un palloncino sgonfio e mettetelo nel freezer per qualche minuto. Poi, tiratelo fuori e osservate cosa succede. Il palloncino si sgonfia! Questo perché la temperatura dell'aria all'interno del palloncino diminuisce, e quindi anche il volume del palloncino diminuisce (a pressione costante). Questo è un esempio pratico di come la temperatura influenza il volume di un gas.
Consigli Utili per Studenti e Genitori
Ecco alcuni consigli che spero vi saranno utili:
- Non abbiate paura di fare domande! Se qualcosa non è chiaro, chiedete al vostro insegnante, a un amico, o cercate su internet. Non c'è niente di male a non capire subito!
- Fate tanti esercizi! Più vi esercitate, più vi diventerà facile usare l'equazione dei gas ideali.
- Cercate di collegare la chimica alla vita di tutti i giorni! Come abbiamo visto, la costante R è presente in molte situazioni che incontriamo quotidianamente. Cercare questi collegamenti vi aiuterà a rendere la chimica più interessante e significativa.
- Genitori, supportate i vostri figli! Incoraggiateli a fare domande, aiutateli a trovare risorse online, e celebrate i loro successi! Un ambiente di supporto può fare la differenza.
- Utilizzate risorse online: Ci sono molti siti web e video che spiegano la costante dei gas in modo chiaro e semplice. Ricercate "costante dei gas spiegata" su Youtube o Google per trovare esempi e spiegazioni aggiuntive.
Un'esperta di didattica della chimica consiglia: "Dividete i problemi complessi in passaggi più piccoli e gestibili. Iniziate con i concetti base e poi passate gradualmente a quelli più avanzati. Non scoraggiatevi se all'inizio vi sembra difficile; con la pratica, diventerà sempre più facile!"
Motivazione Finale
La chimica, e in particolare la costante universale dei gas, può sembrare complessa all'inizio. Ma spero che questo articolo vi abbia dimostrato che non è così inaccessibile come sembra. Con un po' di impegno, di curiosità e di pratica, potrete padroneggiare questo concetto e apprezzare la sua importanza nel mondo che ci circonda. Quindi, non arrendetevi! Continuate a esplorare, a sperimentare e a imparare. La chimica è ovunque, e sta aspettando solo di essere scoperta!
Ricordate: la comprensione è la chiave! Non memorizzate semplicemente le formule; cercate di capire cosa significano e come funzionano. E soprattutto, divertitevi! La chimica può essere affascinante e appagante. Buono studio a tutti!