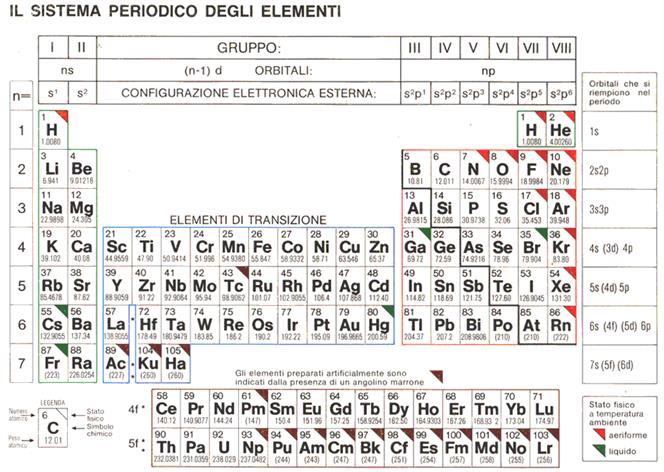
Quanti di noi hanno guardato la tavola periodica degli elementi sentendosi sopraffatti da un muro di simboli e numeri? Genitori che cercano di aiutare i figli con i compiti, studenti che lottano per capire come si combinano gli atomi, insegnanti che cercano modi per rendere la chimica più accessibile: la sfida è reale e condivisa. La buona notizia è che decifrare il numero di ossidazione, una chiave fondamentale per comprendere le reazioni chimiche, non deve essere un incubo. Prendiamoci per mano e trasformiamo questo ostacolo in un'opportunità di apprendimento!
Cos'è il Numero di Ossidazione? Un Concetto Essenziale
Il numero di ossidazione, a volte chiamato stato di ossidazione, è un numero che viene assegnato a un atomo in una sostanza chimica per indicare il grado di ossidazione (perdita di elettroni) o riduzione (acquisto di elettroni). In termini più semplici, ci dice quanti elettroni un atomo sembra aver guadagnato o perso quando si lega ad altri atomi.
Immagina che gli atomi siano come bambini che giocano con delle figurine. Alcuni bambini (atomi) sono più propensi a "condividere" le loro figurine (elettroni) con altri. Il numero di ossidazione ci dice chi sta "dando" e chi sta "ricevendo" in questo gioco di condivisione atomica.
Perché è Importante?
Comprendere il numero di ossidazione è fondamentale per:
- Prevedere le formule chimiche: Sapendo il numero di ossidazione, si può prevedere come gli atomi si combineranno per formare composti.
- Bilanciare le equazioni chimiche: Le reazioni redox (ossidoriduzione) coinvolgono il trasferimento di elettroni, e il numero di ossidazione aiuta a bilanciare correttamente queste equazioni.
- Comprendere le reazioni chimiche: Il numero di ossidazione fornisce informazioni sul comportamento degli elementi durante le reazioni, come la corrosione, la combustione e la respirazione.
- Nomenclatura dei composti inorganici: Sapere i numeri di ossidazione è necessario per dare il nome corretto ai composti.
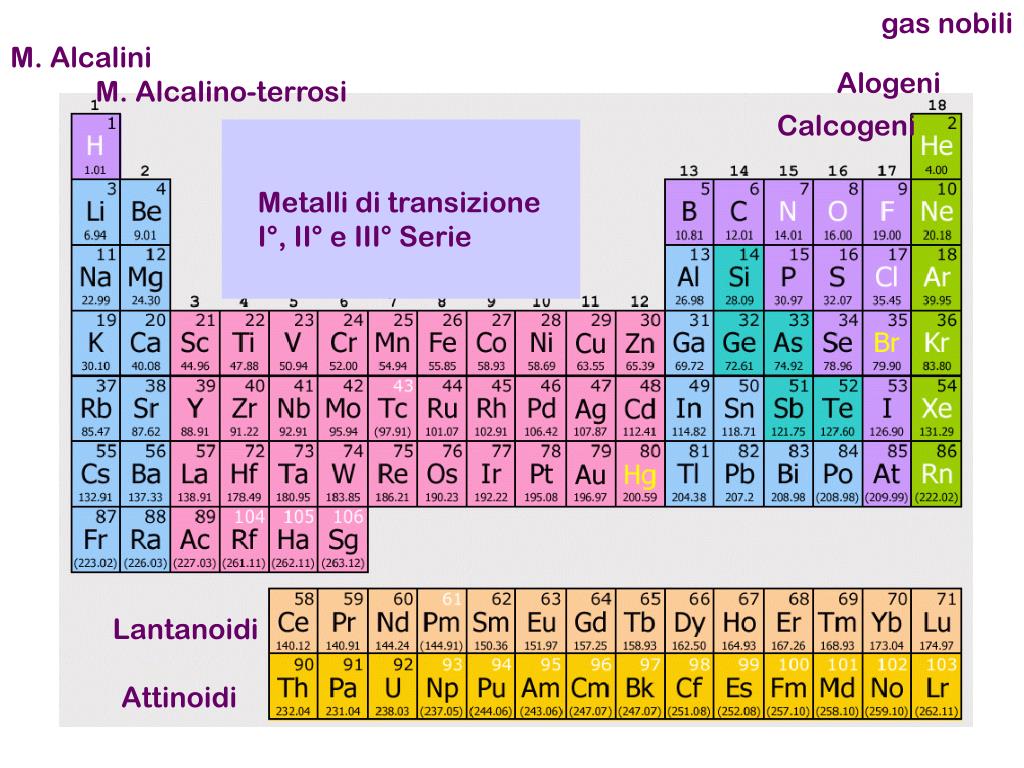
La Tavola Periodica: Una Guida per i Numeri di Ossidazione
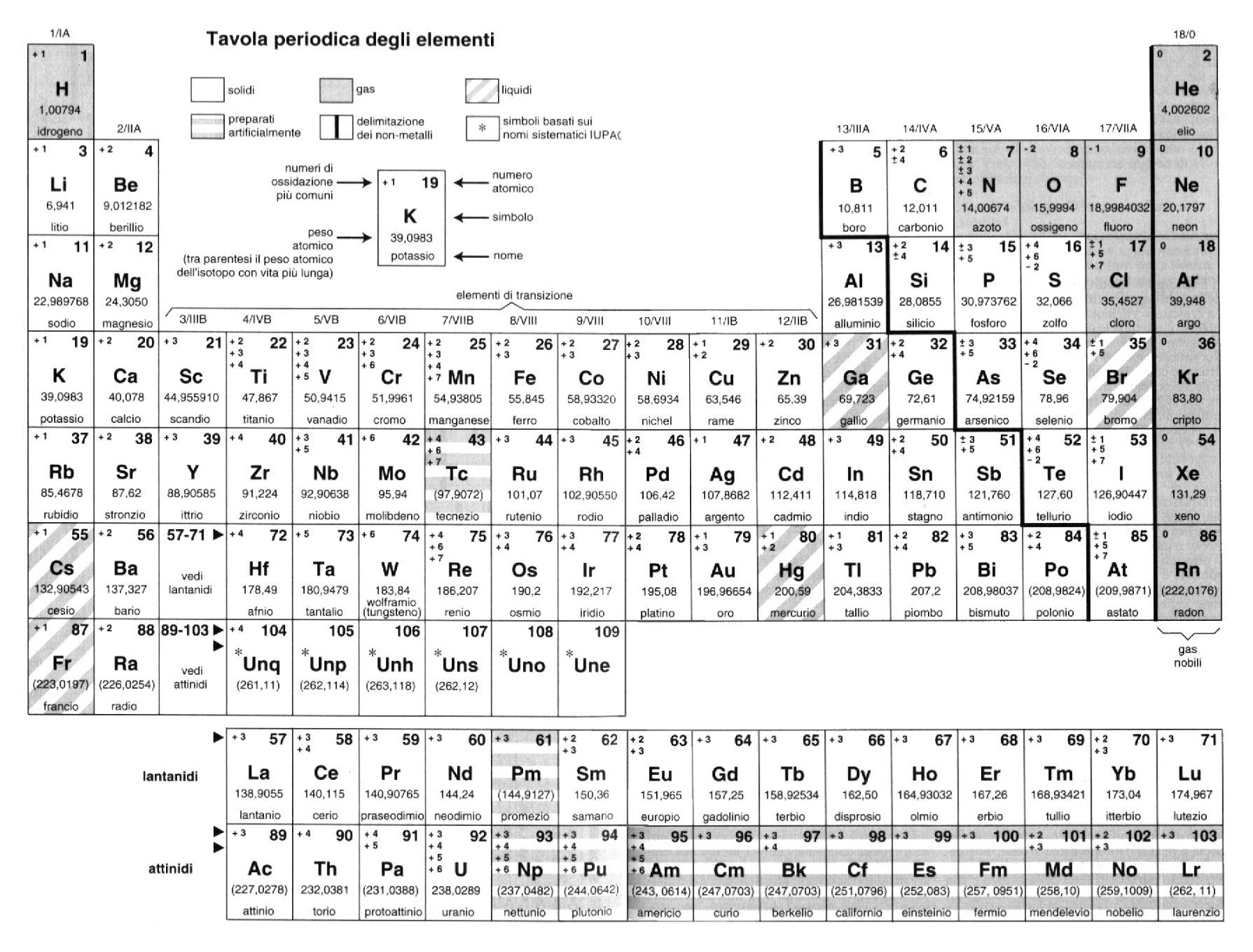
La tavola periodica non è solo un elenco di elementi; è una miniera d'oro di informazioni sui numeri di ossidazione! La posizione di un elemento nella tavola periodica può spesso fornire indizi sul suo numero di ossidazione più comune.
Regole Generali per l'Assegnazione del Numero di Ossidazione
Ecco alcune regole fondamentali per assegnare il numero di ossidazione:
- Elementi allo stato elementare: Il numero di ossidazione di un elemento allo stato elementare (es. O2, Fe, Cu) è sempre 0.
- Ioni monoatomici: Il numero di ossidazione di uno ione monoatomico è uguale alla sua carica (es. Na+ ha numero di ossidazione +1, Cl- ha numero di ossidazione -1).
- Idrogeno: L'idrogeno ha un numero di ossidazione di +1 nella maggior parte dei composti, tranne negli idruri metallici (es. NaH), dove ha un numero di ossidazione di -1.
- Ossigeno: L'ossigeno ha un numero di ossidazione di -2 nella maggior parte dei composti, tranne nei perossidi (es. H2O2), dove ha un numero di ossidazione di -1, e nel difluoruro di ossigeno (OF2), dove ha un numero di ossidazione di +2.
- Alogeni: Gli alogeni (gruppo 17) hanno un numero di ossidazione di -1 nella maggior parte dei composti, tranne quando si combinano con ossigeno o altri alogeni più elettronegativi.
- La somma dei numeri di ossidazione: La somma dei numeri di ossidazione di tutti gli atomi in una molecola neutra è 0. La somma dei numeri di ossidazione di tutti gli atomi in uno ione poliatomico è uguale alla carica dello ione.
- Metalli alcalini (Gruppo 1): Hanno sempre numero di ossidazione +1.
- Metalli alcalino-terrosi (Gruppo 2): Hanno sempre numero di ossidazione +2.
Esempi Pratici
Vediamo alcuni esempi per chiarire come applicare queste regole:
- H2O: L'ossigeno ha numero di ossidazione -2. Poiché la molecola è neutra, i due atomi di idrogeno devono avere un numero di ossidazione totale di +2, quindi ogni atomo di idrogeno ha un numero di ossidazione di +1.
- CO2: L'ossigeno ha numero di ossidazione -2, quindi due atomi di ossigeno hanno un numero di ossidazione totale di -4. Il carbonio deve quindi avere un numero di ossidazione di +4 per rendere la molecola neutra.
- SO42-: L'ossigeno ha numero di ossidazione -2, quindi quattro atomi di ossigeno hanno un numero di ossidazione totale di -8. Poiché lo ione ha una carica di -2, lo zolfo deve avere un numero di ossidazione di +6 ( +6 - 8 = -2).
Strategie per l'Apprendimento Efficace
Ecco alcuni consigli per rendere l'apprendimento dei numeri di ossidazione più efficace e divertente:
- Iniziare con le basi: Assicurarsi di comprendere le regole fondamentali prima di affrontare composti più complessi.
- Esercitarsi, esercitarsi, esercitarsi: Fare molti esercizi è il modo migliore per padroneggiare il concetto. Iniziare con esempi semplici e poi passare a quelli più difficili.
- Utilizzare risorse visive: Le tavole periodiche con i numeri di ossidazione evidenziati possono essere molto utili.
- Collaborare con gli altri: Studiare con amici o compagni di classe può rendere l'apprendimento più interattivo e meno intimidatorio.
- Usare app e risorse online: Esistono molte app e siti web che offrono esercizi, tutorial e guide sui numeri di ossidazione.
- Creare schemi e flashcard: Riassumere le regole e i numeri di ossidazione più comuni in schemi e flashcard può aiutare a memorizzarli.
- Applicare i concetti alla vita reale: Cercare esempi di reazioni chimiche nella vita quotidiana (es. la ruggine del ferro, la combustione del gas) e cercare di capire il ruolo del numero di ossidazione in queste reazioni.
Esempi in Classe e a Casa
In classe: L'insegnante può organizzare giochi a squadre in cui gli studenti devono assegnare i numeri di ossidazione a diversi composti. Si può usare una lavagna interattiva per mostrare esempi e far esercitare gli studenti in tempo reale.
A casa: I genitori possono aiutare i figli a trovare esempi di reazioni chimiche in cucina (es. l'ossidazione di una mela tagliata) e spiegare il ruolo dei numeri di ossidazione. Si possono usare app educative per rendere l'apprendimento più divertente e interattivo.

Errori Comuni da Evitare
Ecco alcuni errori comuni che gli studenti commettono quando imparano i numeri di ossidazione:
- Confondere il numero di ossidazione con la carica ionica: Anche se sono correlati, non sono la stessa cosa. Il numero di ossidazione è un concetto formale, mentre la carica ionica è una proprietà fisica.
- Dimenticare le regole: È fondamentale conoscere le regole per assegnare il numero di ossidazione.
- Non considerare la struttura della molecola: In alcuni casi, la struttura della molecola può influenzare il numero di ossidazione degli atomi.
- Non bilanciare correttamente le equazioni chimiche: Un errore comune è non bilanciare correttamente le equazioni redox, il che porta a numeri di ossidazione errati.
Conclusione: Un Viaggio alla Scoperta della Chimica
Comprendere i numeri di ossidazione può sembrare difficile all'inizio, ma con un approccio strutturato e tanta pratica, diventa un'abilità preziosa per chiunque si avvicini alla chimica. Ricorda, ogni grande scienziato è partito dalle basi. Non scoraggiarti, sperimenta, fai domande e, soprattutto, divertiti ad esplorare il meraviglioso mondo della chimica! La tavola periodica, con i suoi numeri di ossidazione, non è un muro insormontabile, ma una porta d'accesso a una comprensione più profonda del mondo che ci circonda. Abbracciala!
E tu, sei pronto a iniziare il tuo viaggio nella chimica? Prendi la tua tavola periodica, una matita e un quaderno, e preparati a scoprire i segreti degli atomi e delle loro combinazioni!