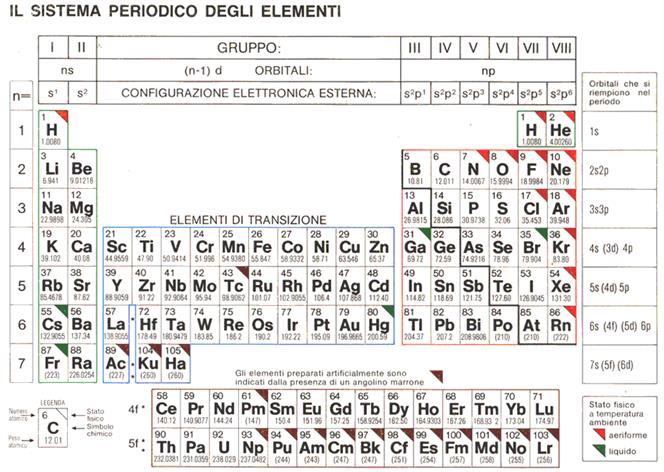
Capita a tutti, soprattutto quando ci si avvicina alla chimica: fissare la Tavola Periodica degli Elementi e sentirsi un po' smarriti. Tanti simboli, numeri, colori… Un vero e proprio labirinto per chi non ha familiarità. Ma non temete! In realtà, la Tavola Periodica è uno strumento potentissimo, una vera e propria mappa che ci guida alla scoperta delle proprietà degli elementi e dei loro comportamenti. E tra le informazioni più preziose che ci offre, ci sono i numeri di ossidazione.
Immaginate di dover capire come si legano tra loro gli atomi per formare le molecole che compongono il mondo che ci circonda. Senza i numeri di ossidazione, sarebbe come navigare a vista in una notte senza stelle. Essi ci forniscono una chiave di lettura fondamentale per prevedere e comprendere le reazioni chimiche.
Cosa sono i Numeri di Ossidazione?
Il numero di ossidazione, a volte abbreviato con l'acronimo N.O., rappresenta la carica elettrica ipotetica che un atomo assumerebbe in un composto se tutti i legami fossero ionici. In altre parole, ci dice quanti elettroni un atomo ha "guadagnato" o "perso" quando si lega con altri atomi. È importante sottolineare che si tratta di una carica ipotetica; nella realtà, molti legami sono covalenti, cioè con una condivisione di elettroni e non un trasferimento completo.
Per capire meglio, pensiamo all'acqua (H2O). L'ossigeno è più elettronegativo dell'idrogeno, cioè attrae gli elettroni con più forza. Pertanto, in questo composto, l'ossigeno "guadagna" (parzialmente) due elettroni (uno da ciascun atomo di idrogeno), e quindi ha un numero di ossidazione di -2. L'idrogeno, invece, "perde" (parzialmente) un elettrone e ha un numero di ossidazione di +1.
Perché sono Importanti?
I numeri di ossidazione non sono solo un concetto teorico. Hanno un impatto concreto sulla nostra vita quotidiana:
- Previsione delle reazioni chimiche: Sapere i numeri di ossidazione ci permette di prevedere quali reazioni avverranno e quali prodotti si formeranno. Pensate alla corrosione del ferro (ruggine): è una reazione di ossidazione, dove il ferro perde elettroni.
- Nomenclatura dei composti: I numeri di ossidazione sono fondamentali per dare un nome corretto ai composti chimici. Ad esempio, il ferro può avere numero di ossidazione +2 o +3, e questo si riflette nel nome dei suoi ossidi: ossido di ferro(II) (FeO) e ossido di ferro(III) (Fe2O3).
- Bilanciamento delle equazioni chimiche: Le reazioni chimiche devono rispettare la legge di conservazione della massa: il numero di atomi di ciascun elemento deve essere lo stesso sia nei reagenti che nei prodotti. I numeri di ossidazione ci aiutano a bilanciare le equazioni redox, dove si verificano trasferimenti di elettroni.
- Comprendere i processi biologici: Molti processi vitali, come la respirazione cellulare, coinvolgono reazioni di ossidoriduzione (redox). La comprensione dei numeri di ossidazione è cruciale per capire come questi processi funzionano.
Come trovare i Numeri di Ossidazione nella Tavola Periodica
La Tavola Periodica è organizzata in modo tale da fornire indicazioni sui numeri di ossidazione più comuni degli elementi. Ecco alcune regole generali:

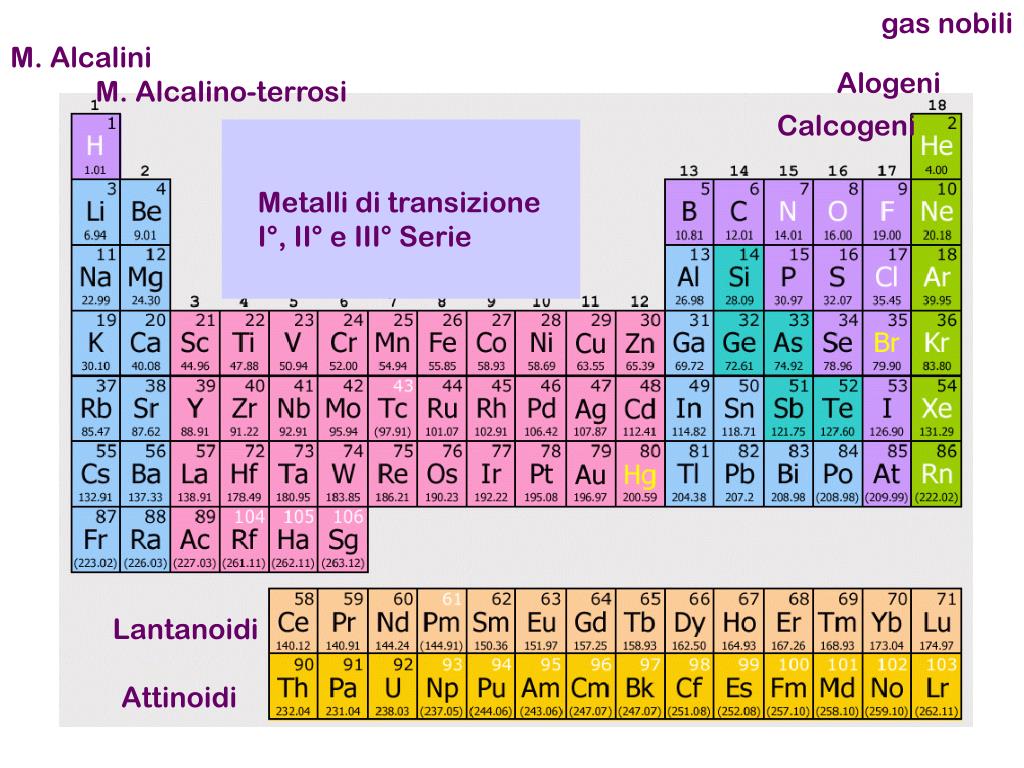
- Gruppo 1 (Metalli Alcalini): Generalmente hanno numero di ossidazione +1 (es. Na, K).
- Gruppo 2 (Metalli Alcalino-Terrosi): Generalmente hanno numero di ossidazione +2 (es. Mg, Ca).
- Gruppo 17 (Alogeni): Generalmente hanno numero di ossidazione -1 (es. Cl, Br), ma possono avere numeri di ossidazione positivi quando si legano con elementi più elettronegativi come l'ossigeno.
- Ossigeno: Generalmente ha numero di ossidazione -2, tranne nel caso dei perossidi (es. H2O2), dove ha numero di ossidazione -1.
- Idrogeno: Generalmente ha numero di ossidazione +1, tranne negli idruri metallici (es. NaH), dove ha numero di ossidazione -1.
- Metalli di Transizione: Spesso hanno più numeri di ossidazione possibili. La Tavola Periodica di solito indica i numeri di ossidazione più comuni.
È importante notare che queste sono solo regole generali. Ci sono eccezioni, e alcuni elementi possono avere più numeri di ossidazione a seconda del composto in cui si trovano. Una Tavola Periodica con i numeri di ossidazione riporta, per ciascun elemento, i numeri di ossidazione più comuni. Questo è particolarmente utile per i metalli di transizione, che presentano una varietà maggiore.
Un Esempio Pratico: Il Manganese (Mn)
Il manganese è un metallo di transizione con diversi numeri di ossidazione possibili, che vanno da -3 a +7. Una Tavola Periodica con i numeri di ossidazione indicherà probabilmente i valori +2, +3, +4, +6 e +7. Questo significa che il manganese può formare una varietà di composti, ognuno con proprietà diverse. Ad esempio:
- MnO (ossido di manganese(II)): Il manganese ha numero di ossidazione +2.
- MnO2 (biossido di manganese): Il manganese ha numero di ossidazione +4.
- KMnO4 (permanganato di potassio): Il manganese ha numero di ossidazione +7. Questo composto è un forte ossidante.
La capacità del manganese di assumere diversi numeri di ossidazione lo rende un elemento versatile, utilizzato in diversi settori, dalla produzione di acciaio alla sintesi di composti chimici.
Affrontare le Obiezioni
Alcuni potrebbero sostenere che l'uso dei numeri di ossidazione è un'eccessiva semplificazione della realtà, poiché i legami non sono sempre puramente ionici. Questo è vero. Tuttavia, i numeri di ossidazione rimangono uno strumento estremamente utile per:
- Prevedere la reattività chimica.
- Bilanciare le equazioni chimiche.
- Comprendere i meccanismi delle reazioni redox.
Anche se non descrivono perfettamente la distribuzione reale delle cariche, forniscono un modello concettuale che ci aiuta a capire come gli atomi interagiscono tra loro.
Come Imparare a Usare i Numeri di Ossidazione
Ecco alcuni consigli per imparare a usare i numeri di ossidazione in modo efficace:
- Iniziate con gli elementi più comuni: Concentratevi prima sui numeri di ossidazione degli elementi dei gruppi 1, 2, 16 e 17.
- Utilizzate una Tavola Periodica con i numeri di ossidazione: Vi aiuterà a visualizzare i numeri di ossidazione più comuni per ciascun elemento.
- Fate esercizi: Bilanciate le equazioni redox e cercate di prevedere i prodotti delle reazioni chimiche.
- Consultate un libro di testo o un insegnante: Se avete dubbi, non esitate a chiedere aiuto.
Ricordate che la pratica rende perfetti! Più vi esercitate, più facile diventerà usare i numeri di ossidazione per risolvere i problemi di chimica.
Oltre la Teoria: Applicazioni Pratiche
Consideriamo l'esempio delle batterie. Le batterie funzionano grazie a reazioni di ossidoriduzione. Nella batteria zinco-rame, lo zinco metallico si ossida (perde elettroni) e il rame(II) si riduce (guadagna elettroni). Comprendere i numeri di ossidazione dello zinco (0 e +2) e del rame (0 e +2) è essenziale per capire come la batteria genera elettricità. Allo stesso modo, la corrosione dei metalli, come la ruggine del ferro, è un processo di ossidazione. Il ferro (Fe), con numero di ossidazione 0, si trasforma in ossido di ferro (Fe2O3), dove il ferro ha numero di ossidazione +3.
La fotosintesi clorofilliana, un processo fondamentale per la vita sulla Terra, è anch'essa una complessa reazione di ossidoriduzione. L'acqua (H2O) viene ossidata (l'ossigeno, con numero di ossidazione -2, si trasforma in ossigeno gassoso, O2, con numero di ossidazione 0) e il diossido di carbonio (CO2) viene ridotto (il carbonio, con numero di ossidazione +4, si trasforma in glucosio, C6H12O6, dove il carbonio ha un numero di ossidazione medio di 0). La comprensione dei numeri di ossidazione aiuta a capire come l'energia solare viene convertita in energia chimica.

Riflessioni Finali
Spero che questo articolo vi abbia aiutato a demistificare i numeri di ossidazione e a capire la loro importanza in chimica. Non abbiate paura di affrontare questo argomento, perché una volta compreso, vi aprirà le porte a una comprensione più profonda del mondo che vi circonda. La Tavola Periodica con i numeri di ossidazione è un alleato prezioso in questo percorso. Imparate a consultarla e a sfruttare le informazioni che vi offre.
La chimica è ovunque, e i numeri di ossidazione sono uno degli strumenti più potenti per decifrarla!
Ora, riflettete: in quali altri aspetti della vostra vita quotidiana pensate che la chimica (e quindi i numeri di ossidazione) giochi un ruolo importante?