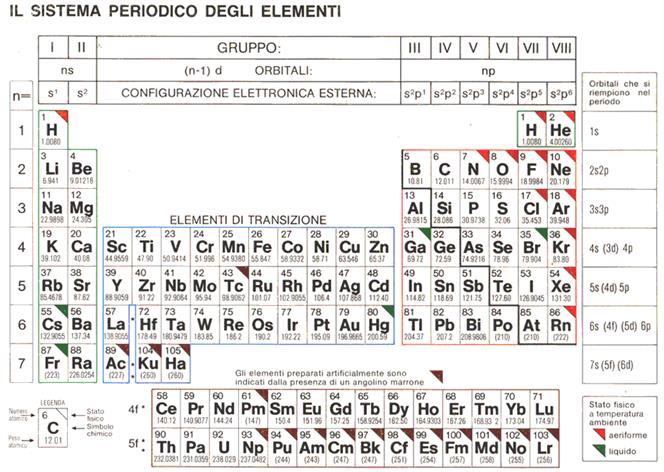
Ciao a tutti! Se siete qui, probabilmente state lottando con la tavola periodica e, in particolare, con quei numeri di ossidazione che sembrano voler nascondersi dietro ogni angolo. Tranquilli, non siete soli! Molti studenti, e persino professionisti, trovano questo argomento un po' ostico. Ma non temete, cercheremo di semplificare il tutto, partendo dal perché questi numeri sono così importanti e come influenzano la nostra vita quotidiana.
Perché Preoccuparsi dei Numeri di Ossidazione?
I numeri di ossidazione, o stati di ossidazione, sono essenzialmente la "carica" che un atomo sembrerebbe avere in una molecola o in un composto ionico se gli elettroni fossero trasferiti completamente. Capire questi numeri è fondamentale per:
- Prevedere come gli atomi si combineranno per formare composti.
- Bilanciare equazioni chimiche, soprattutto quelle redox (ossidoriduzione).
- Comprendere la reattività chimica delle diverse sostanze.
- Applicazioni pratiche in settori come la medicina, l'ingegneria e l'agricoltura.
Immaginate di voler preparare un fertilizzante per le vostre piante. Conoscere i numeri di ossidazione degli elementi coinvolti (azoto, fosforo, potassio, ad esempio) vi permette di scegliere i composti giusti e di dosarli correttamente per evitare di danneggiare le piante. Oppure, pensate alla produzione di farmaci: la corretta ossidazione di un composto può fare la differenza tra un medicinale efficace e una sostanza tossica.
La Tavola Periodica: Una Mappa per i Numeri di Ossidazione
La tavola periodica non è solo un elenco di elementi; è una vera e propria mappa che ci fornisce indizi preziosi sui numeri di ossidazione. La posizione di un elemento nel gruppo (colonna verticale) spesso ci dice quali sono i suoi numeri di ossidazione più comuni.
Regole Generali
Prima di addentrarci nei dettagli, ecco alcune regole generali che vi aiuteranno:
- Elementi allo stato elementare: Hanno numero di ossidazione 0 (es. O2, Fe, Cu).
- Ione monoatomico: Il numero di ossidazione è uguale alla carica dello ione (es. Na+ ha numero di ossidazione +1, Cl- ha numero di ossidazione -1).
- Ossigeno: Solitamente ha numero di ossidazione -2, tranne nel perossido (H2O2) dove è -1 e nel composto con il fluoro (OF2) dove è +2.
- Idrogeno: Solitamente ha numero di ossidazione +1, tranne negli idruri metallici (NaH, LiH) dove è -1.
- Fluoro: Ha sempre numero di ossidazione -1.
- La somma dei numeri di ossidazione in una molecola neutra è 0.
- La somma dei numeri di ossidazione in uno ione poliatomico è uguale alla carica dello ione.
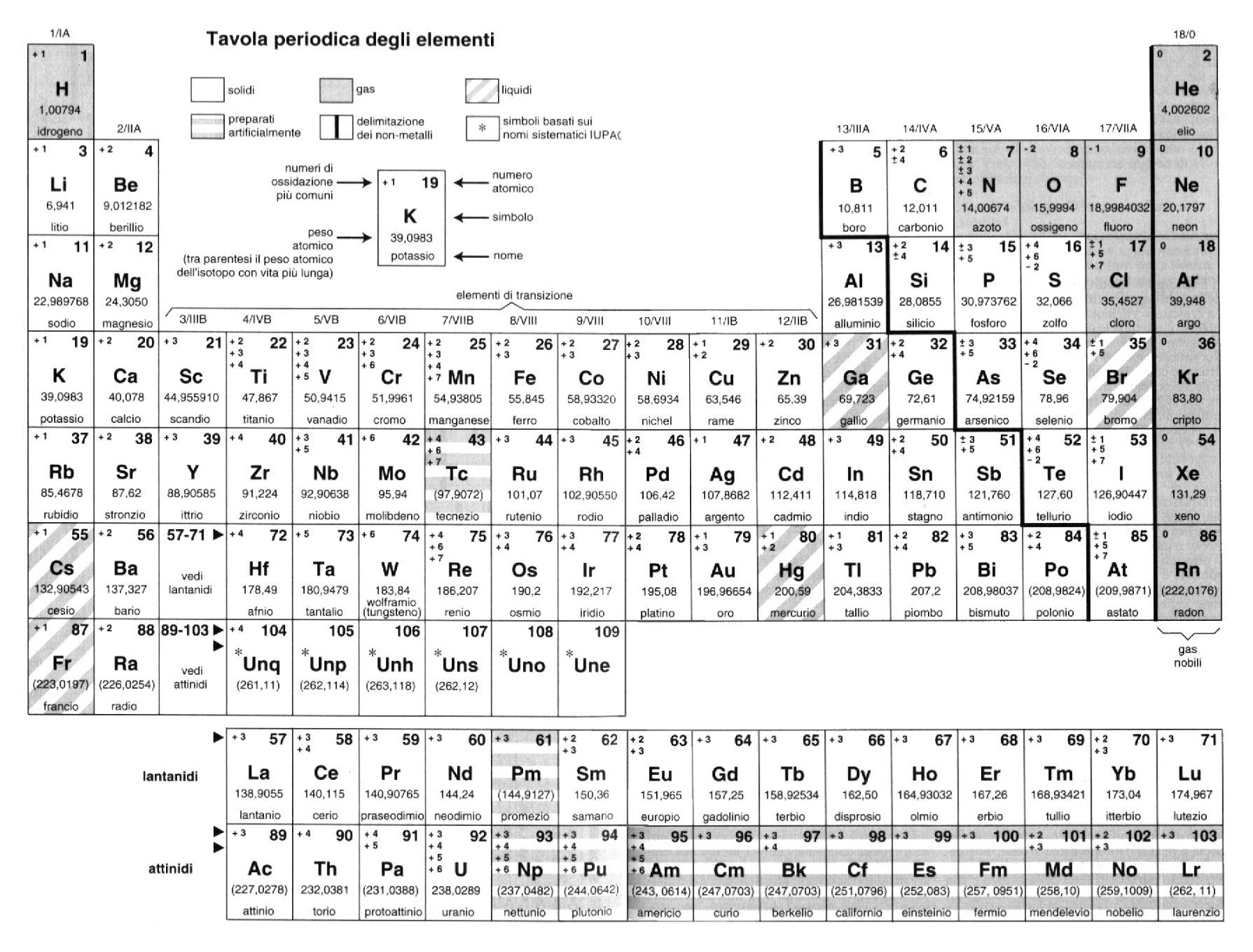
Gruppi Principali e Numeri di Ossidazione Comuni
- Gruppo 1 (Metalli Alcalini): Hanno numero di ossidazione +1. (Li, Na, K, Rb, Cs, Fr)
- Gruppo 2 (Metalli Alcalino-Terrosi): Hanno numero di ossidazione +2. (Be, Mg, Ca, Sr, Ba, Ra)
- Gruppo 13 (Gruppo del Boro): Solitamente hanno numero di ossidazione +3, ma alcuni elementi possono avere anche +1. (B, Al, Ga, In, Tl)
- Gruppo 14 (Gruppo del Carbonio): Possono avere numeri di ossidazione +4, +2, -4. Il carbonio è particolarmente versatile. (C, Si, Ge, Sn, Pb)
- Gruppo 15 (Gruppo dell'Azoto): Possono avere numeri di ossidazione +5, +3, -3. L'azoto è molto importante nei fertilizzanti. (N, P, As, Sb, Bi)
- Gruppo 16 (Gruppo dell'Ossigeno): Solitamente hanno numero di ossidazione -2. (O, S, Se, Te, Po)
- Gruppo 17 (Alogeni): Solitamente hanno numero di ossidazione -1, ma possono assumere anche valori positivi quando combinati con ossigeno o altri alogeni. (F, Cl, Br, I, At)
- Gruppo 18 (Gas Nobili): Generalmente inerti e con numero di ossidazione 0. (He, Ne, Ar, Kr, Xe, Rn)
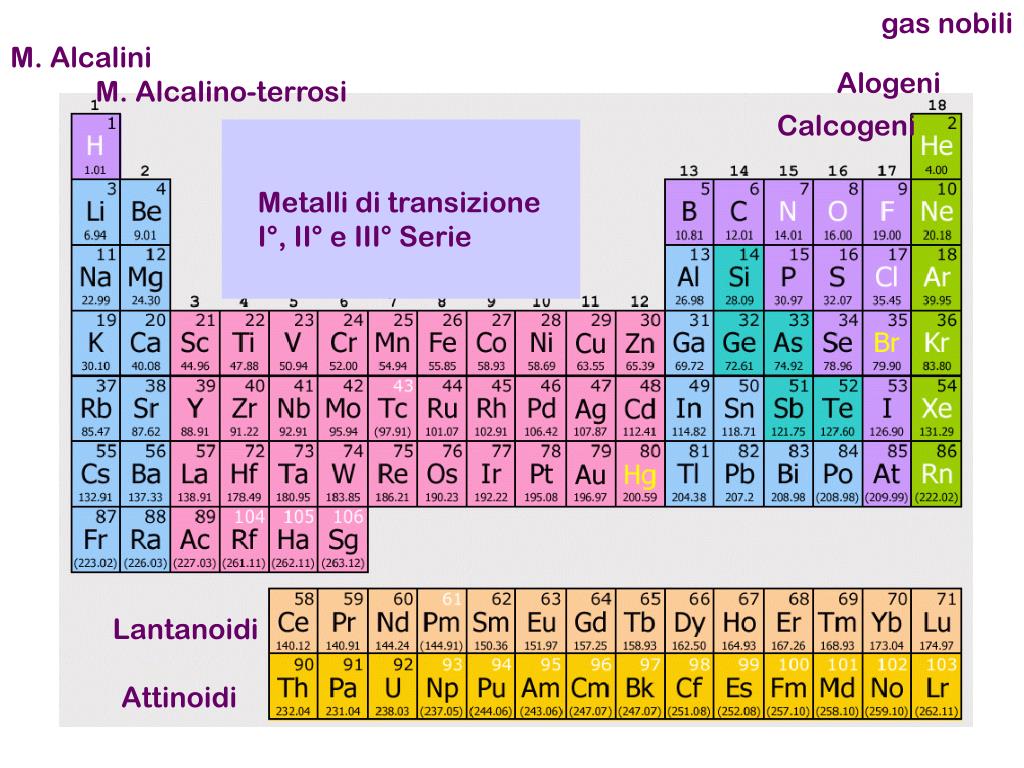
Metalli di Transizione: Un Caso a Parte
I metalli di transizione sono noti per avere molti numeri di ossidazione. Questo è dovuto alla disponibilità degli elettroni negli orbitali d. Ad esempio:
- Ferro (Fe): +2 e +3 sono i più comuni, ma può avere anche altri numeri di ossidazione.
- Manganese (Mn): +2, +4, +7 sono comuni.
- Cromo (Cr): +2, +3, +6 sono importanti.
Questa variabilità rende i metalli di transizione particolarmente utili come catalizzatori in molte reazioni chimiche. La loro capacità di cambiare stato di ossidazione facilita il trasferimento di elettroni e accelera le reazioni.
Come Calcolare i Numeri di Ossidazione: Esempi Pratici
Vediamo alcuni esempi concreti per capire come calcolare i numeri di ossidazione in diversi composti:
Esempio 1: KMnO4 (Permanganato di Potassio)
- Sappiamo che il potassio (K) ha numero di ossidazione +1 e l'ossigeno (O) ha numero di ossidazione -2.
- La somma dei numeri di ossidazione deve essere 0 (perché la molecola è neutra).
- Quindi: (+1) + x + 4(-2) = 0, dove x è il numero di ossidazione del manganese (Mn).
- Risolvendo l'equazione: x = +7. Il manganese ha numero di ossidazione +7 nel KMnO4.
Esempio 2: SO42- (Ione Solfato)
- Sappiamo che l'ossigeno (O) ha numero di ossidazione -2.
- La somma dei numeri di ossidazione deve essere -2 (perché lo ione ha carica -2).
- Quindi: x + 4(-2) = -2, dove x è il numero di ossidazione dello zolfo (S).
- Risolvendo l'equazione: x = +6. Lo zolfo ha numero di ossidazione +6 nello ione solfato.
Esempio 3: Cr2O72- (Ione Dicromato)
- Sappiamo che l'ossigeno (O) ha numero di ossidazione -2.
- La somma dei numeri di ossidazione deve essere -2 (perché lo ione ha carica -2).
- Quindi: 2x + 7(-2) = -2, dove x è il numero di ossidazione del cromo (Cr).
- Risolvendo l'equazione: 2x = +12 => x = +6. Il cromo ha numero di ossidazione +6 nello ione dicromato.
Controindicazioni: Quando le Regole Non Bastano
È importante ricordare che queste sono solo regole generali. Ci sono eccezioni e composti in cui il calcolo dei numeri di ossidazione può essere più complesso. Ad esempio, nei composti organici, dove la struttura molecolare gioca un ruolo fondamentale, o in alcuni composti interalogeni.
Alcuni potrebbero sostenere che memorizzare tutti i numeri di ossidazione sia l'unico modo per padroneggiare l'argomento. Ma questo approccio è inefficiente e poco pratico. Comprendere i principi sottostanti e saper applicare le regole è molto più importante e vi permetterà di affrontare anche situazioni complesse.

Applicazioni Reali: Oltre il Libro di Testo
Come accennato all'inizio, i numeri di ossidazione non sono solo un esercizio accademico. Hanno un impatto significativo in molte aree:
- Chimica Ambientale: Comprendere i processi redox che avvengono nell'ambiente è fondamentale per affrontare problemi come l'inquinamento.
- Elettrochimica: Le batterie e le celle a combustibile si basano su reazioni redox.
- Metallurgia: L'estrazione e la purificazione dei metalli spesso coinvolgono reazioni redox.
- Industria Alimentare: La conservazione degli alimenti e la prevenzione dell'ossidazione sono cruciali.
Pensate alla corrosione del ferro (la ruggine). È un processo redox in cui il ferro si ossida a ossido di ferro (ruggine). Capire i numeri di ossidazione coinvolti ci permette di sviluppare strategie per prevenire o rallentare questo processo, proteggendo strutture metalliche, automobili e altre applicazioni.
Soluzioni Pratiche per la Vita di Tutti i Giorni
Nonostante possa sembrare un argomento complesso, la comprensione dei numeri di ossidazione può offrirvi vantaggi anche nella vita quotidiana:

- Scelta di prodotti per la pulizia: Alcuni prodotti contengono agenti ossidanti o riducenti che possono essere efficaci per la pulizia ma anche dannosi per certe superfici. Conoscere i numeri di ossidazione degli elementi coinvolti può aiutarvi a fare scelte più consapevoli.
- Conservazione degli alimenti: Sapere come l'ossidazione influisce sulla freschezza degli alimenti vi permette di adottare strategie per conservarli meglio (es. usare contenitori ermetici, aggiungere antiossidanti).
- Giardinaggio: La scelta dei fertilizzanti giusti dipende dalla comprensione dei numeri di ossidazione degli elementi essenziali per le piante.
In definitiva, padroneggiare i numeri di ossidazione è un investimento che paga in termini di comprensione del mondo che ci circonda e di capacità di prendere decisioni più informate.
Spero che questa guida vi sia stata utile. Ricordate, la pratica rende perfetti! Più esercizi fate, più familiarità acquisirete con i numeri di ossidazione e più facile diventerà applicarli.
E ora, cosa ne dite di provare a calcolare i numeri di ossidazione in alcuni composti che trovate in casa? Che ne pensate di NaOH (idrossido di sodio), H2SO4 (acido solforico) o NaClO (ipoclorito di sodio)? Buon divertimento!