
Quante volte, studiando chimica o fisica, ti sei trovato di fronte a concetti astratti come gli spettri di emissione e di assorbimento, sentendoti un po' perso nel mare di linee colorate? Non sei solo! Molti studenti si scontrano con la difficoltà di visualizzare e comprendere appieno cosa rappresentano questi spettri, e come sono legati alla struttura atomica e molecolare della materia. Cerchiamo di far luce insieme su questo argomento, rendendolo più accessibile e interessante.
Cosa sono gli Spettri: Una Finestra sull'Atomo
Immagina che ogni atomo sia come un minuscolo strumento musicale, capace di emettere o assorbire suoni (o meglio, luce) a frequenze specifiche. Questi "suoni" di luce, quando scomposti, formano quello che chiamiamo spettro. Uno spettro è, in sostanza, una rappresentazione visiva della distribuzione dell'intensità della luce in funzione della sua frequenza (o lunghezza d'onda).
Come spiega il professor Richard Feynman, fisico premio Nobel, "La natura usa solo i lunghi fili della nostra conoscenza per tessere il suo meraviglioso arazzo." (Feynman, R. P. (1965). The Character of Physical Law). Gli spettri, in questo contesto, sono uno di questi fili, che ci permettono di comprendere la natura più intima della materia.
Spettri di Emissione: L'Impronta Digitale di un Elemento
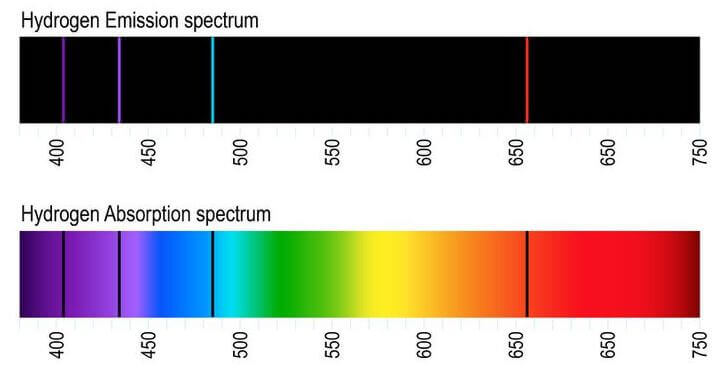
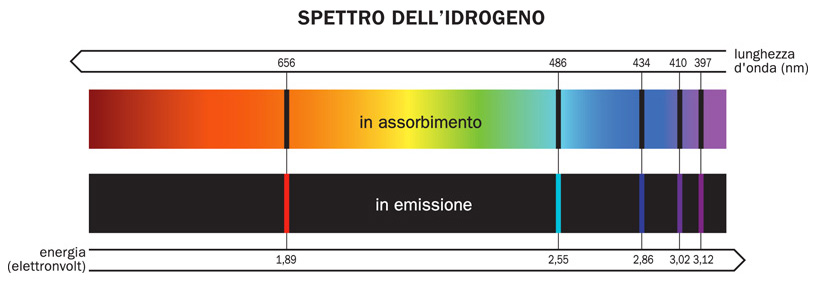
Uno spettro di emissione si ottiene quando un elemento viene eccitato, ad esempio riscaldandolo o sottoponendolo a una scarica elettrica. Gli atomi, assorbendo energia, portano i loro elettroni a livelli energetici superiori. Quando questi elettroni ritornano ai livelli energetici inferiori, rilasciano l'energia in eccesso sotto forma di fotoni di luce.
La particolarità è che ogni elemento emette fotoni a lunghezze d'onda specifiche, creando uno spettro di emissione unico, come un'impronta digitale. Questo perché i livelli energetici degli elettroni sono quantizzati, ovvero possono assumere solo determinati valori. La differenza di energia tra questi livelli corrisponde all'energia dei fotoni emessi.
Punti chiave sugli spettri di emissione:
- Si ottengono quando un elemento eccitato rilascia energia.
- Sono composti da linee colorate su sfondo nero.
- Ogni elemento ha uno spettro di emissione unico.
- Permettono di identificare gli elementi presenti in un campione.
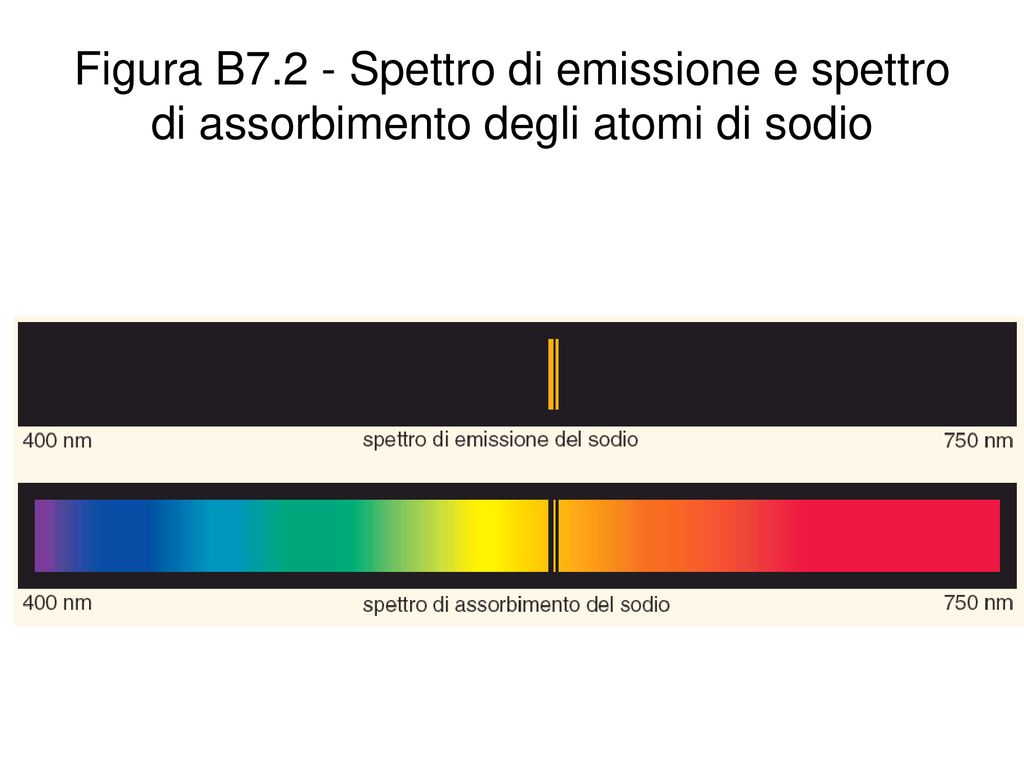
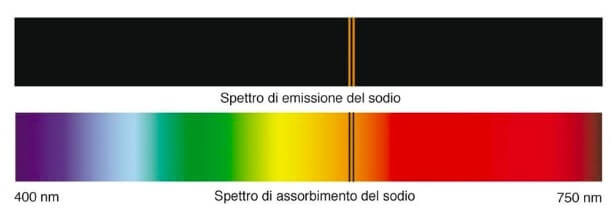
Esempio pratico: Prendi una lampada al sodio. Se scomponi la luce emessa, otterrai uno spettro di emissione caratterizzato da due linee gialle molto vicine. Queste linee sono specifiche del sodio e ti permettono di identificarlo in qualsiasi sorgente luminosa.
Spettri di Assorbimento: Il Lato Oscuro della Luce
Uno spettro di assorbimento si ottiene quando la luce bianca (che contiene tutte le lunghezze d'onda) attraversa un gas freddo. Gli atomi del gas assorbono solo le lunghezze d'onda corrispondenti alle transizioni elettroniche possibili, ovvero quelle che portano gli elettroni a livelli energetici superiori.
In questo caso, lo spettro risultante sarà uno spettro continuo (come quello della luce bianca) interrotto da linee nere. Queste linee nere corrispondono alle lunghezze d'onda che sono state assorbite dagli atomi del gas.
Punti chiave sugli spettri di assorbimento:
- Si ottengono quando la luce bianca attraversa un gas freddo.
- Sono composti da uno spettro continuo interrotto da linee nere.
- Le linee nere corrispondono alle lunghezze d'onda assorbite.
- Le linee nere sono le stesse che si vedrebbero nello spettro di emissione dello stesso elemento.
Esempio pratico: Osserva la luce del sole attraverso un prisma. Noterai delle linee nere nello spettro continuo. Queste linee (chiamate linee di Fraunhofer) sono dovute all'assorbimento di determinate lunghezze d'onda da parte degli elementi presenti nell'atmosfera solare.
La Relazione tra Emissione e Assorbimento: Un Equilibrio Perfetto
È importante notare che le lunghezze d'onda assorbite da un elemento sono le stesse delle lunghezze d'onda emesse dallo stesso elemento quando è eccitato. Questo è un concetto fondamentale. Ciò significa che gli spettri di emissione e di assorbimento di un elemento sono complementari. Uno è la "negazione" dell'altro.
Come afferma il fisico teorico Max Planck, "Una nuova verità scientifica non trionfa convincendo i suoi oppositori e facendogli vedere la luce, ma piuttosto perché alla fine i suoi oppositori muoiono e cresce una nuova generazione che ha familiarità con essa." (Planck, M. (1949). Scientific Autobiography and Other Papers). Anche se questo concetto può sembrare difficile all'inizio, con la pratica e la visualizzazione, diventerà sempre più chiaro.
Applicazioni Pratiche: Oltre il Laboratorio
Gli spettri di emissione e di assorbimento non sono solo concetti teorici. Hanno innumerevoli applicazioni pratiche in diversi campi:
- Chimica Analitica: Identificazione e quantificazione degli elementi presenti in un campione.
- Astrofisica: Determinazione della composizione chimica delle stelle e delle galassie. Analizzando la luce che ci arriva dalle stelle, gli astronomi possono identificare gli elementi presenti nella loro atmosfera.
- Medicina: Diagnosi di alcune malattie attraverso l'analisi spettrale di campioni biologici.
- Scienza dei Materiali: Caratterizzazione delle proprietà dei materiali.
- Monitoraggio Ambientale: Rilevamento di inquinanti nell'aria e nell'acqua.
Come Approfondire la Tua Comprensione
Ecco alcuni suggerimenti per migliorare la tua comprensione degli spettri di emissione e di assorbimento:
- Visualizza: Utilizza animazioni e simulazioni interattive online per visualizzare il processo di emissione e assorbimento della luce. Esistono molte risorse gratuite disponibili, come quelle offerte da PhET Interactive Simulations (Università del Colorado Boulder).
- Sperimenta: Se possibile, prova a realizzare uno spettroscopio semplice con materiali di recupero (ad esempio, un CD e una scatola di cartone) per osservare gli spettri di diverse sorgenti luminose.
- Esercitati: Risolvi esercizi e problemi che richiedono l'applicazione dei concetti relativi agli spettri.
- Discuti: Parla con i tuoi compagni di studio o con il tuo insegnante per chiarire eventuali dubbi e confrontare le tue interpretazioni.
- Collega i concetti: Cerca di collegare gli spettri alla struttura atomica e molecolare della materia. Comprendere come gli elettroni si muovono tra i livelli energetici è fondamentale per capire l'origine degli spettri.
Strumenti Utili
Esistono diversi strumenti che possono aiutarti a visualizzare e analizzare gli spettri:
- Spettroscopi: Strumenti che permettono di osservare e analizzare gli spettri di luce.
- Software di analisi spettrale: Programmi che permettono di elaborare e interpretare i dati spettrali.
- Database di spettri: Raccolte di spettri di emissione e di assorbimento di diversi elementi e composti. Il National Institute of Standards and Technology (NIST) offre un database completo e gratuito online.
Ricorda, la comprensione degli spettri di emissione e di assorbimento è un passo fondamentale per svelare i segreti dell'universo che ci circonda. Non scoraggiarti di fronte alle difficoltà iniziali. Con un po' di impegno e curiosità, potrai padroneggiare questo affascinante argomento e aprire una finestra sulla bellezza e la complessità della natura.
Come diceva Marie Curie, "Non bisogna mai avere paura di ciò che si sta facendo quando si ritiene che sia giusto." (Quinn, S. (1995). Marie Curie: A Life). Quindi, continua a esplorare, a sperimentare e a imparare! La conoscenza è la chiave per comprendere il mondo che ci circonda.