
Capire l'acidità dei composti organici può sembrare un compito arduo, qualcosa che interessa solo a chimici in camice bianco. In realtà, la Scala di Acidità ha implicazioni molto concrete nella nostra vita quotidiana, dal funzionamento dei farmaci che assumiamo, alla degradazione degli alimenti che consumiamo, fino ai processi industriali che ci forniscono i materiali di cui abbiamo bisogno. Molti di noi si sono trovati ad avere a che fare con bruciori di stomaco, causati da un eccesso di acidità nello stomaco. Anche questo è un esempio pratico di come l'acidità influenzi la nostra salute. Se questo concetto vi sembra lontano, spero che questo articolo vi aiuti a capire meglio quanto sia rilevante.
Cos'è l'Acidità? Un Concetto Chiave
In termini semplici, l'acidità di un composto organico si riferisce alla sua capacità di donare un protone (ione idrogeno, H+). Più facilmente un composto cede un protone, più è considerato acido. Ma attenzione! Non stiamo parlando solo degli acidi forti che conosciamo dal laboratorio. Anche composti apparentemente innocui, come l'alcol etilico (presente nelle bevande alcoliche), possono comportarsi da acidi, sebbene in misura molto minore. L'importanza sta nella relatività: l'acidità è sempre definita in relazione ad un'altra sostanza.
Immaginate di avere una calamita. La sua "forza" (capacità di attrarre metalli) è relativa. Attrae più facilmente un chiodo di ferro rispetto ad un pezzo di legno. Allo stesso modo, un acido cederà il suo protone più facilmente ad una base forte piuttosto che ad una base debole.
Il Ruolo della Struttura Molecolare
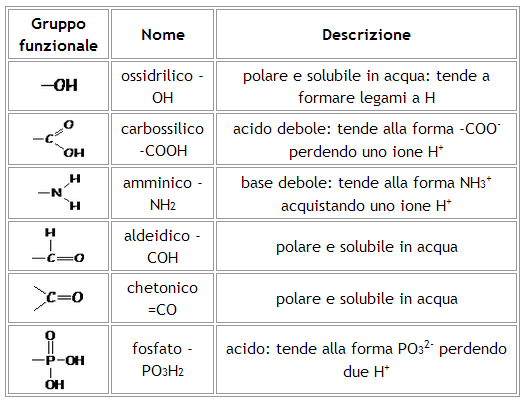
La struttura molecolare di un composto organico è il fattore determinante della sua acidità. Diversi elementi strutturali influenzano la facilità con cui un protone può essere rilasciato. Consideriamo i seguenti aspetti:
- Elettronegatività: Gli atomi elettronegativi, come l'ossigeno (O), l'azoto (N) e gli alogeni (fluoro, cloro, bromo, iodio), attirano gli elettroni verso di sé. Se un atomo elettronegativo è legato all'idrogeno, indebolisce il legame H-X (dove X è l'atomo elettronegativo) rendendo più facile la sua rottura e la conseguente liberazione del protone.
- Effetto Induttivo: Gli atomi elettronegativi possono influenzare l'acidità anche a distanza, attraverso l'effetto induttivo. La loro presenza, anche se non direttamente legati all'idrogeno acido, può polarizzare la molecola e facilitare la donazione del protone.
- Risonanza: La stabilizzazione per risonanza della base coniugata (la specie chimica che si forma dopo che l'acido ha ceduto il protone) aumenta l'acidità. Più la base coniugata è stabile, più l'acido è propenso a donare il protone. Ad esempio, gli acidi carbossilici (presenti nell'aceto e in molti altri composti organici) sono più acidi degli alcoli perché la base coniugata, lo ione carbossilato, è stabilizzata per risonanza.
- Ibridazione dell'atomo di carbonio: L'ibridazione dell'atomo di carbonio a cui è legato l'idrogeno influisce sull'acidità. Un carbonio sp è più elettronegativo di un carbonio sp2, che a sua volta è più elettronegativo di un carbonio sp3. Pertanto, gli alchini terminali (contenenti un idrogeno legato a un carbonio sp) sono più acidi degli alcheni (legato a un carbonio sp2) e degli alcani (legato a un carbonio sp3).
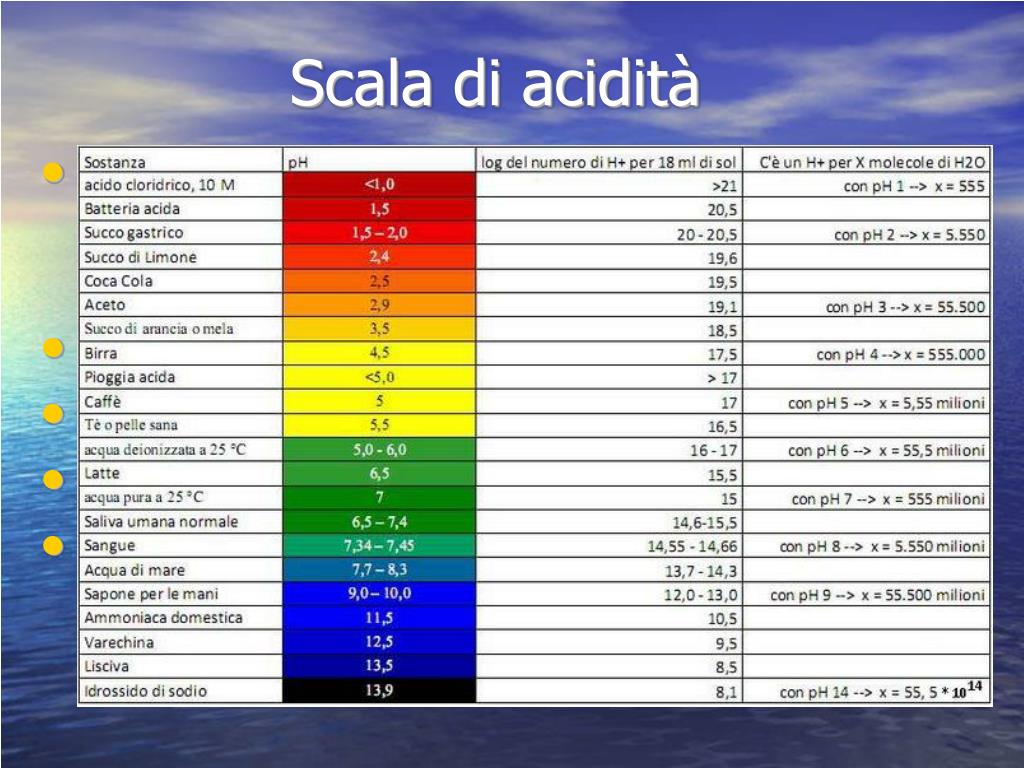
La Scala di Acidità: Misurare l'Acidità
Per quantificare l'acidità, si utilizza la costante di dissociazione acida, Ka. Questa costante esprime l'equilibrio tra un acido (HA), la sua base coniugata (A-) e lo ione idrogeno (H+) in soluzione acquosa:
HA ⇌ H+ + A-

La Ka è definita come:
Ka = [H+][A-] / [HA]
Dove le parentesi quadre indicano le concentrazioni all'equilibrio. Più alto è il valore di Ka, più forte è l'acido. Tuttavia, i valori di Ka possono essere molto piccoli e difficili da gestire. Per questo motivo, si preferisce utilizzare il pKa, che è il logaritmo negativo in base 10 della Ka:
pKa = -log10(Ka)

In questo modo, più basso è il valore del pKa, più forte è l'acido. Questa scala è estremamente utile per confrontare l'acidità di diversi composti.
Esempi Pratici di pKa
Ecco alcuni esempi di valori di pKa per darvi un'idea della scala:
- Acido cloridrico (HCl): pKa ≈ -7 (acido forte)
- Acido solforico (H2SO4): pKa1 ≈ -3 (acido forte)
- Acido acetico (CH3COOH): pKa ≈ 4.76
- Fenolo (C6H5OH): pKa ≈ 10
- Etanolo (CH3CH2OH): pKa ≈ 16
- Ammoniaca (NH3): pKa ≈ 38 (in acqua, si considera l'acido coniugato NH4+, con pKa ≈ 9.25)
- Etano (CH3CH3): pKa ≈ 50 (acido estremamente debole)
Come si può notare, la scala è molto ampia. Un composto con un pKa di -7 è circa 1057 volte più acido di un composto con un pKa di 50!
Applicazioni Pratiche: Dove Entra in Gioco l'Acidità
L'acidità dei composti organici è fondamentale in molti campi:
- Chimica Organica: La comprensione dell'acidità è essenziale per prevedere e controllare le reazioni chimiche. Molte reazioni organiche richiedono l'uso di acidi o basi come catalizzatori.
- Biochimica: Il pH del corpo umano (e di tutti gli organismi viventi) è strettamente controllato. L'acidità e la basicità influenzano l'attività degli enzimi e la stabilità delle biomolecole.
- Farmaceutica: Le proprietà acido-base dei farmaci influenzano la loro solubilità, l'assorbimento, la distribuzione, il metabolismo e l'escrezione (ADME) nel corpo. Un farmaco con un certo pKa sarà più o meno efficace a seconda del pH dell'ambiente in cui si trova.
- Scienza dei Materiali: L'acidità superficiale dei materiali influenza le loro proprietà catalitiche, adesive e di corrosione.
- Scienza degli Alimenti: L'acidità influisce sul sapore, sulla conservazione e sulla trasformazione degli alimenti. Ad esempio, l'acido citrico (presente nel limone) viene utilizzato come conservante e per conferire un sapore aspro.
Affrontare le Critiche: Acidità in Ambiente Non Acquoso
Un possibile contro argomento è che la scala di pKa tradizionale è definita in acqua. Tuttavia, molte reazioni chimiche avvengono in solventi non acquosi. In questi casi, l'acidità relativa dei composti può variare significativamente a causa degli effetti del solvente. Ad esempio, un acido che è forte in acqua potrebbe essere debole in un solvente aprotico polare come il dimetilsolfossido (DMSO). Per questo motivo, esistono scale di acidità specifiche per diversi solventi. È fondamentale considerare il solvente quando si valuta l'acidità di un composto.
Inoltre, alcuni studiosi sostengono che il concetto di acidità e basicità sia troppo semplificato e che non tenga conto di altri fattori, come la polarizzabilità e gli effetti sterici. Tuttavia, la scala di acidità rimane uno strumento prezioso e ampiamente utilizzato per comprendere e prevedere il comportamento chimico dei composti organici.
Un Approccio Pratico alla Comprensione
Invece di memorizzare semplicemente i valori di pKa, cercate di capire i fattori che influenzano l'acidità. Analizzate la struttura molecolare dei composti e identificate gli atomi elettronegativi, i gruppi che stabilizzano la base coniugata e l'ibridazione degli atomi di carbonio. Cercate di visualizzare mentalmente la donazione del protone e la formazione della base coniugata. Con la pratica, sarete in grado di stimare l'acidità relativa dei composti organici senza dover consultare tabelle di pKa.
Considerate gli acidi carbossilici. Sono ubiquitari in natura e nelle sintesi chimiche. La loro acidità è dovuta alla presenza del gruppo carbossile (-COOH), in cui l'idrogeno è legato all'ossigeno. L'ossigeno è un atomo elettronegativo, che indebolisce il legame O-H. Inoltre, la base coniugata, lo ione carbossilato, è stabilizzata per risonanza, il che rende la donazione del protone più favorevole.
Al contrario, gli alcani sono acidi estremamente deboli. Non contengono atomi elettronegativi legati all'idrogeno e la base coniugata, un carbanione, non è stabilizzata in alcun modo. La donazione di un protone da un alcano richiede una grande quantità di energia.
Passi Successivi: Approfondire la Vostra Conoscenza
Spero che questo articolo vi abbia fornito una solida base per comprendere l'acidità dei composti organici. Per approfondire la vostra conoscenza, vi consiglio di:
- Consultare libri di testo di chimica organica.
- Cercare risorse online, come video lezioni e articoli scientifici.
- Risolvere esercizi e problemi pratici.
- Discutere con altri studenti e professori.
Ricordate, la chimica è una disciplina cumulativa. Ogni nuovo concetto si basa su quelli precedenti. Non abbiate paura di fare domande e di chiedere aiuto quando necessario.
Ora che avete una comprensione di base dell'acidità, come pensate che questo influenzi la vostra prospettiva sulla chimica e sul mondo che vi circonda?