
Ciao! Capisco benissimo: la tavola periodica può sembrare un labirinto, soprattutto quando si tratta di capire quali elementi sono metalli. Non preoccuparti, non sei solo! Molti studenti trovano questa parte un po' ostica. Ma insieme, la renderemo molto più chiara e semplice.
Cosa sono i Metalli, Davvero?
Prima di tuffarci nella tavola periodica, cerchiamo di capire cosa rende un elemento un metallo. Immagina che i metalli siano come degli amici socievoli e ben organizzati. Generalmente, i metalli hanno queste caratteristiche:
- Lucentezza: Brillano, riflettono la luce. Pensa all'oro o all'argento.
- Conducibilità: Conducono bene il calore e l'elettricità. Ecco perché usiamo il rame nei fili elettrici e l'alluminio nelle pentole.
- Malleabilità: Possono essere modellati in lamine sottili. Pensa alla stagnola di alluminio.
- Duttilità: Possono essere tirati in fili sottili. Pensa al rame nei cavi.
- Solidi (a temperatura ambiente): Quasi tutti i metalli sono solidi a temperatura ambiente, con l'eccezione del mercurio (Hg), che è liquido.
Dove Trovare i Metalli Nella Tavola Periodica
Ora, passiamo alla tavola periodica. La maggior parte degli elementi nella tavola periodica sono metalli! In generale, li troverai sul lato sinistro e al centro della tavola. C'è una linea "a scaletta" (a volte evidenziata con un colore diverso) che separa i metalli dai non metalli. Tutto quello che si trova a sinistra di questa linea (eccetto l'idrogeno, H, che è un'eccezione!) è considerato un metallo.
Possiamo dividere i metalli in diverse categorie:
Metalli Alcalini
Questi sono i più reattivi! Si trovano nel primo gruppo (la prima colonna) della tavola periodica, tranne l'idrogeno (H). Esempi sono il litio (Li), il sodio (Na) e il potassio (K). Ricorda, sono molto reattivi e non si trovano mai allo stato puro in natura.
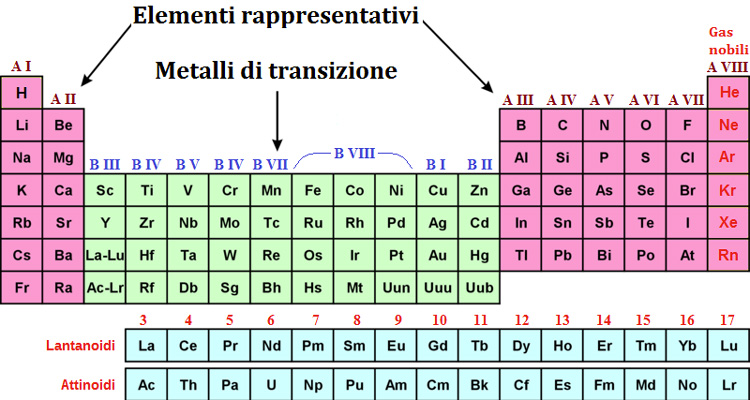
Metalli Alcalino-Terrosi
Anche questi sono reattivi, ma meno dei metalli alcalini. Si trovano nel secondo gruppo (la seconda colonna) della tavola periodica. Esempi sono il magnesio (Mg) e il calcio (Ca). Il calcio è fondamentale per le nostre ossa!
Metalli di Transizione
Questi metalli si trovano nella parte centrale della tavola periodica (i gruppi 3-12). Sono noti per le loro proprietà variabili e la loro capacità di formare composti colorati. Esempi sono il ferro (Fe), il rame (Cu), l'oro (Au) e l'argento (Ag). Sono molto importanti in diverse applicazioni, dall'elettronica alla gioielleria.
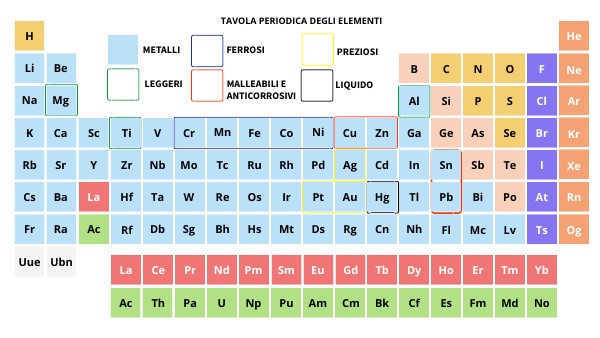
Metalli del Blocco p
Questi metalli si trovano nel blocco "p" della tavola periodica, a destra della linea "a scaletta", ma prima dei non metalli. Alcuni esempi sono l'alluminio (Al), il gallio (Ga), l'indio (In), lo stagno (Sn) e il piombo (Pb). Hanno proprietà intermedie tra i metalli di transizione e i non metalli.
Lantanidi e Attinidi (Metalli delle Terre Rare)
Questi metalli si trovano in fondo alla tavola periodica, in due righe separate. Sono spesso usati in applicazioni tecnologiche avanzate, come magneti e catalizzatori. Esempi sono il cerio (Ce) e l'uranio (U).

Un Trucchetto Utile
Un modo semplice per ricordare dove si trovano i metalli è visualizzare una "montagna" nella tavola periodica. La base della montagna è la parte con i metalli più attivi (alcalini e alcalino-terrosi), la vetta della montagna è la zona dei non metalli, e le pendici sono i metalli di transizione e i metalli del blocco p.
Esercitati e Divertiti!
Il modo migliore per imparare è esercitarsi! Prendi una tavola periodica, evidenzia i metalli, e cerca esempi di come vengono usati nella vita di tutti i giorni. Non scoraggiarti se all'inizio ti sembra difficile. Con un po' di pratica, diventerai un esperto! E ricorda, l'apprendimento è un viaggio, non una gara! Buon divertimento!