
Capita a tutti, prima o poi, di trovarsi di fronte alla tavola periodica e sentirsi un po' sopraffatti. Non preoccuparti, è un'esperienza comune! Ricordare tutti gli elementi e le loro proprietà può sembrare un'impresa titanica, ma con il giusto approccio, anche i concetti più complessi diventano accessibili. In questo articolo, ci concentreremo su un gruppo specifico: gli alogeni. Impareremo cosa sono, dove si trovano nella tavola periodica, quali sono le loro caratteristiche principali e come interagiscono con altri elementi. Preparati a scoprire un mondo affascinante e a rendere lo studio della chimica un'esperienza più semplice e gratificante!
Cosa Sono Gli Alogeni? Una Definizione Chiara
Gli alogeni sono un gruppo di elementi chimici che occupano il gruppo 17 (VIIA) della tavola periodica. Il termine "alogeno" deriva dal greco antico "halos genes", che significa "generatori di sale". Questo nome riflette la loro tendenza a reagire con i metalli per formare sali, come il cloruro di sodio (NaCl), il comune sale da cucina.
Ma cosa rende questi elementi così speciali? La risposta sta nella loro struttura atomica: hanno sette elettroni nel loro guscio di valenza, l'ultimo livello energetico occupato dagli elettroni. Questo significa che hanno un forte desiderio di acquisire un elettrone aggiuntivo per raggiungere una configurazione elettronica stabile, simile a quella dei gas nobili. Questa "fame" di elettroni li rende altamente reattivi.
Consiglio pratico per gli studenti: Immagina gli alogeni come persone che cercano disperatamente un ultimo pezzo di puzzle per completare un'immagine. Questa analogia può aiutarti a ricordare la loro tendenza ad acquisire un elettrone.
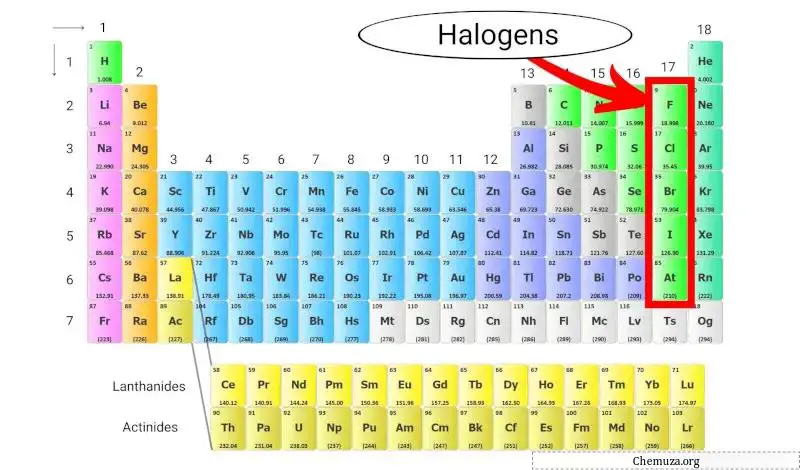
Quali Sono Gli Alogeni? Identifichiamoli Nella Tavola Periodica
Ecco l'elenco degli alogeni che troviamo nel gruppo 17 della tavola periodica:

- Fluoro (F)
- Cloro (Cl)
- Bromo (Br)
- Iodio (I)
- Astato (At)
- Tennesso (Ts) (elemento sintetico, le cui proprietà sono ancora in fase di studio)
Un consiglio per i genitori: Aiutate i vostri figli a visualizzare la tavola periodica e a individuare gli alogeni. Potete creare un gioco a quiz per rendere l'apprendimento più divertente e interattivo.
Proprietà Caratteristiche Degli Alogeni: Un'Analisi Dettagliata
Gli alogeni condividono diverse proprietà chimiche e fisiche, anche se queste variano in intensità scendendo lungo il gruppo. Ecco alcune delle caratteristiche più importanti:

- Elevata Elettronegatività: Gli alogeni sono tra gli elementi più elettronegativi della tavola periodica. L'elettronegatività è la misura della capacità di un atomo di attrarre elettroni in un legame chimico. Questa elevata elettronegatività spiega la loro tendenza ad acquisire elettroni.
- Elevata Reattività: Come abbiamo già accennato, gli alogeni sono molto reattivi. Il fluoro è l'alogeno più reattivo, seguito dal cloro, dal bromo e dallo iodio. L'astato è radioattivo e meno reattivo.
- Stati Fisici Vari: Gli alogeni si presentano in diversi stati fisici a temperatura ambiente: il fluoro e il cloro sono gas, il bromo è un liquido e lo iodio è un solido.
- Colorazione: Gli alogeni hanno colori caratteristici. Il fluoro è un gas giallo pallido, il cloro è un gas giallo-verde, il bromo è un liquido rosso-marrone e lo iodio è un solido viola scuro.
- Tossicità: Molti alogeni sono tossici e possono essere dannosi per la salute. Ad esempio, il cloro è un gas irritante che può causare problemi respiratori.
Approfondimento: Secondo uno studio pubblicato sul "Journal of Chemical Education", l'utilizzo di dimostrazioni pratiche in classe, come la reazione tra un metallo e un alogeno, può migliorare significativamente la comprensione delle proprietà degli alogeni da parte degli studenti.
La Reattività Degli Alogeni: Un Approfondimento
La reattività degli alogeni diminuisce scendendo lungo il gruppo. Questo significa che il fluoro è l'alogeno più reattivo e l'astato è il meno reattivo (anche se, a causa della sua radioattività, è difficile studiarne le proprietà in dettaglio). La reattività è legata all'energia di ionizzazione, ovvero l'energia necessaria per rimuovere un elettrone da un atomo. Più bassa è l'energia di ionizzazione, più facile è rimuovere un elettrone e, quindi, più reattivo è l'elemento. Scendendo lungo il gruppo, l'energia di ionizzazione diminuisce, ma la diminuzione delle dimensioni atomiche (e quindi una maggiore attrazione del nucleo sugli elettroni di valenza) ha un impatto maggiore sulla reattività.
Gli alogeni reagiscono con molti altri elementi, inclusi i metalli, gli idrogeni e altri non metalli. Ad esempio, il fluoro reagisce vigorosamente con quasi tutti gli elementi, mentre lo iodio è meno reattivo. La reazione degli alogeni con i metalli porta alla formazione di sali ionici, mentre la reazione con i non metalli porta alla formazione di composti covalenti.
Alcuni Composti Importanti Degli Alogeni
Gli alogeni formano numerosi composti importanti che hanno diverse applicazioni. Ecco alcuni esempi:
- Cloruro di Sodio (NaCl): Il comune sale da cucina, essenziale per la vita e utilizzato in molti processi industriali.
- Acido Cloridrico (HCl): Un acido forte utilizzato in laboratorio e nell'industria chimica. Si trova anche nello stomaco umano, dove aiuta nella digestione.
- Fluoruro di Sodio (NaF): Aggiunto all'acqua potabile e ai dentifrici per prevenire la carie.
- Clorofluorocarburi (CFC): Un tempo utilizzati come refrigeranti e propellenti, ma ora banditi a causa del loro impatto negativo sullo strato di ozono.
- Poliuretano espanso: Alcuni di essi, in particolare quelli usati nell'edilizia, contengono alogeni per renderli ignifughi.
Applicazioni Pratiche Degli Alogeni: Dove Li Troviamo Nella Vita Quotidiana?
Gli alogeni hanno una vasta gamma di applicazioni nella vita quotidiana. Ecco alcuni esempi:
- Disinfezione dell'acqua: Il cloro è ampiamente utilizzato per disinfettare l'acqua potabile e le piscine, uccidendo batteri e virus.
- Medicina: Lo iodio è utilizzato come antisettico e disinfettante per le ferite. Viene anche utilizzato in alcuni farmaci e come tracciante in medicina nucleare.
- Illuminazione: Le lampade alogene contengono iodio o bromo, che aumentano la luminosità e la durata della lampada.
- Industria chimica: Gli alogeni sono utilizzati come reagenti in molte reazioni chimiche per la produzione di plastica, farmaci e altri prodotti chimici.
- Agricoltura: Alcuni pesticidi e erbicidi contengono alogeni.
Spunto di riflessione: Incoraggia gli studenti a riflettere sull'importanza degli alogeni nella loro vita quotidiana. Questo può rendere l'apprendimento più significativo e coinvolgente.
Consigli per Insegnanti e Studenti: Rendere l'Apprendimento Degli Alogeni Più Efficace
Ecco alcuni consigli per rendere l'apprendimento degli alogeni più efficace:
- Utilizzare analogie e metafore: Come abbiamo fatto in questo articolo, le analogie e le metafore possono aiutare gli studenti a comprendere concetti astratti.
- Utilizzare supporti visivi: La tavola periodica, immagini, video e animazioni possono aiutare gli studenti a visualizzare gli alogeni e le loro proprietà.
- Eseguire esperimenti pratici: Gli esperimenti pratici, come la reazione tra un metallo e un alogeno, possono rendere l'apprendimento più coinvolgente e memorabile.
- Incoraggiare la discussione e la collaborazione: La discussione e la collaborazione tra studenti possono aiutare a chiarire dubbi e a consolidare la comprensione.
- Rendere l'apprendimento rilevante: Collegare l'apprendimento degli alogeni alla vita quotidiana e alle applicazioni pratiche può rendere l'apprendimento più significativo.
- Usare flashcards: Create flashcards per aiutare a memorizzare i nomi, i simboli e le proprietà degli alogeni.
- Risolvere esercizi: La risoluzione di esercizi e problemi può aiutare a consolidare la comprensione dei concetti.
Messaggio finale: Non scoraggiarti se all'inizio ti sembra difficile. Con impegno e la giusta strategia, puoi imparare tutto ciò che ti serve sugli alogeni e sulla chimica in generale. Abbi fiducia nelle tue capacità e non aver paura di chiedere aiuto quando ne hai bisogno! Ricorda che l'apprendimento è un viaggio, non una destinazione, e ogni passo avanti è un successo.