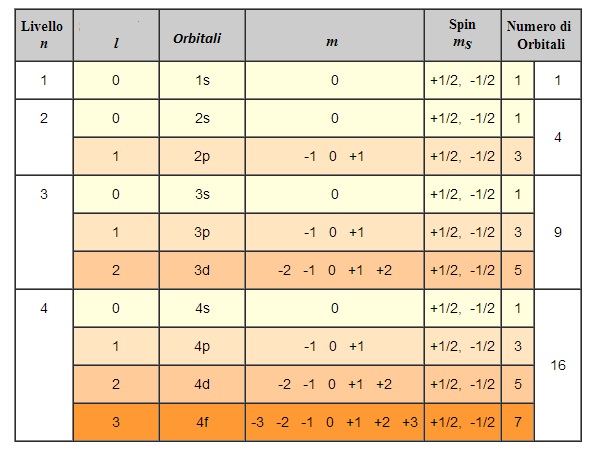
Il concetto di numero massimo di elettroni in un orbitale è fondamentale per comprendere la struttura elettronica degli atomi e, di conseguenza, il comportamento chimico degli elementi. Determina come gli elettroni si distribuiscono intorno al nucleo, influenzando la formazione di legami chimici e le proprietà delle molecole.
Cosa significa "Numero Massimo di Elettroni in un Orbitale"?
Un orbitale è una regione dello spazio intorno al nucleo di un atomo dove c'è un'alta probabilità di trovare un elettrone. Ogni orbitale può ospitare al massimo due elettroni. Questo limite non è arbitrario, ma è una diretta conseguenza del Principio di Esclusione di Pauli.
Perché è importante?
Comprendere questo principio è cruciale per diverse ragioni:
- Struttura Atomica: Aiuta a visualizzare e capire come gli elettroni si dispongono negli orbitali atomici, definendo la configurazione elettronica di un elemento.
- Tavola Periodica: La struttura della tavola periodica riflette direttamente il riempimento degli orbitali atomici. Ogni periodo corrisponde al riempimento di un nuovo livello energetico, e ogni blocco (s, p, d, f) corrisponde al riempimento di un certo tipo di orbitale.
- Legami Chimici: La capacità di un atomo di formare legami chimici dipende dalla sua configurazione elettronica, in particolare dagli elettroni di valenza (quelli nel livello energetico più esterno). La conoscenza del numero massimo di elettroni in un orbitale aiuta a prevedere come gli atomi si combineranno per formare molecole.
- Proprietà Chimiche: Le proprietà chimiche di una sostanza sono determinate dalla sua struttura elettronica. Capire come gli elettroni sono distribuiti negli orbitali permette di prevedere la reattività, l'energia di ionizzazione, l'affinità elettronica e altre proprietà importanti.
Il Principio di Esclusione di Pauli
Il Principio di Esclusione di Pauli, formulato dal fisico austriaco Wolfgang Pauli, afferma che due elettroni in un atomo non possono avere tutti e quattro i numeri quantici uguali. I numeri quantici descrivono lo stato di un elettrone: n (numero quantico principale), l (numero quantico angolare o azimutale), ml (numero quantico magnetico), e ms (numero quantico di spin). Un orbitale è definito dai primi tre numeri quantici (n, l, ml). Quindi, per ospitare due elettroni nello stesso orbitale, devono differire nel numero quantico di spin (ms), che può assumere solo due valori: +1/2 e -1/2 (spin "up" e spin "down").

"È impossibile che due elettroni di uno stesso atomo abbiano tutti e quattro i numeri quantici uguali." - Wolfgang Pauli
Implicazioni per gli Studenti
Gli studenti spesso trovano difficoltà a visualizzare gli orbitali e la distribuzione degli elettroni. È importante utilizzare modelli visivi, come diagrammi orbitalici, per illustrare come gli elettroni riempiono gli orbitali seguendo le regole di Hund (che massimizzano lo spin totale) e il principio di Aufbau (che riempie gli orbitali in ordine crescente di energia). Errori comuni includono l'errata attribuzione di più di due elettroni a un singolo orbitale o la violazione del principio di Hund.
Applicazioni Pratiche
La comprensione del numero massimo di elettroni in un orbitale ha applicazioni pratiche in vari campi:
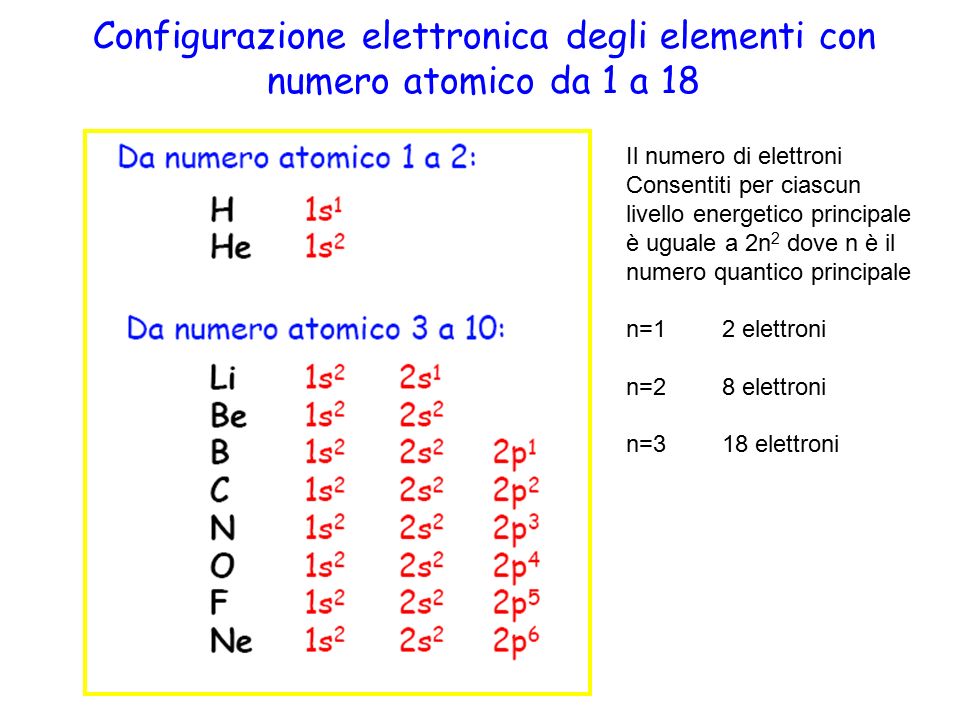
- Chimica: Prevedere le reazioni chimiche e la formazione di composti.
- Scienza dei Materiali: Progettare nuovi materiali con proprietà specifiche.
- Elettronica: Sviluppare dispositivi elettronici basati sulla conduzione degli elettroni nei materiali semiconduttori.
- Spettroscopia: Interpretare gli spettri atomici e molecolari, che forniscono informazioni sulla struttura elettronica delle sostanze.
Ad esempio, quando si bilancia una reazione chimica, la conoscenza della valenza degli elementi (determinata dalla loro configurazione elettronica e dal numero di elettroni di valenza) è essenziale. Inoltre, la comprensione del legame chimico, come il legame covalente e il legame ionico, dipende direttamente dalla conoscenza di come gli elettroni si distribuiscono tra gli atomi per raggiungere una configurazione elettronica stabile (spesso un ottetto, cioè 8 elettroni nel livello di valenza, ad eccezione dell'idrogeno e dell'elio che tendono a raggiungere una configurazione a due elettroni simile a quella dell'elio).
In conclusione, il concetto di numero massimo di elettroni in un orbitale è un pilastro fondamentale della chimica e della fisica moderna. La sua comprensione approfondita è essenziale per gli studenti per acquisire una solida base nella struttura della materia e nelle sue proprietà.