Il modello atomico di Bohr, proposto da Niels Bohr nel 1913, rappresenta un passo fondamentale nell'evoluzione della comprensione della struttura atomica. Superando le limitazioni del modello di Rutherford, introduceva la quantizzazione dell'energia degli elettroni, spiegando in modo convincente lo spettro di emissione dell'idrogeno. Una mappa concettuale del modello di Bohr ci permette di visualizzare e comprendere meglio i suoi concetti chiave, le sue assunzioni e le sue implicazioni.
Punti Chiave del Modello Atomico di Bohr
1. Orbite Quantizzate
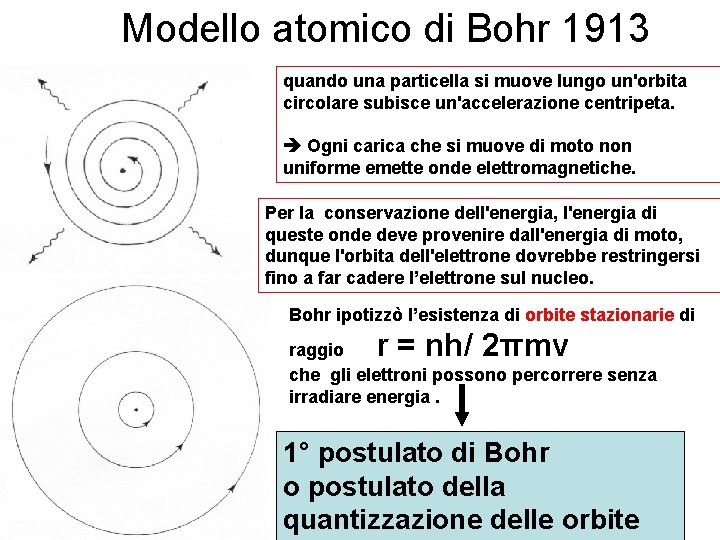
L'innovazione principale del modello di Bohr risiede nell'introduzione del concetto di orbite quantizzate. A differenza del modello di Rutherford, dove gli elettroni potevano orbitare il nucleo a qualsiasi distanza, Bohr postulò che gli elettroni potessero esistere solo in orbite specifiche, a distanze ben definite dal nucleo. Queste orbite corrispondono a livelli di energia discreti, o quantizzati. Ogni orbita è caratterizzata da un numero quantico principale, n, che assume valori interi positivi (n = 1, 2, 3, ...). Maggiore è il valore di n, maggiore è l'energia dell'elettrone e maggiore è la distanza dell'orbita dal nucleo.
L'assunzione della quantizzazione fu rivoluzionaria perché spiegava perché gli elettroni non irradiavano energia e non spiraleggiavano verso il nucleo, un problema insormontabile per il modello di Rutherford basato sulla fisica classica. Secondo la teoria classica, una carica accelerata, come un elettrone in orbita, avrebbe dovuto emettere radiazione elettromagnetica, perdendo energia e collassando infine sul nucleo.
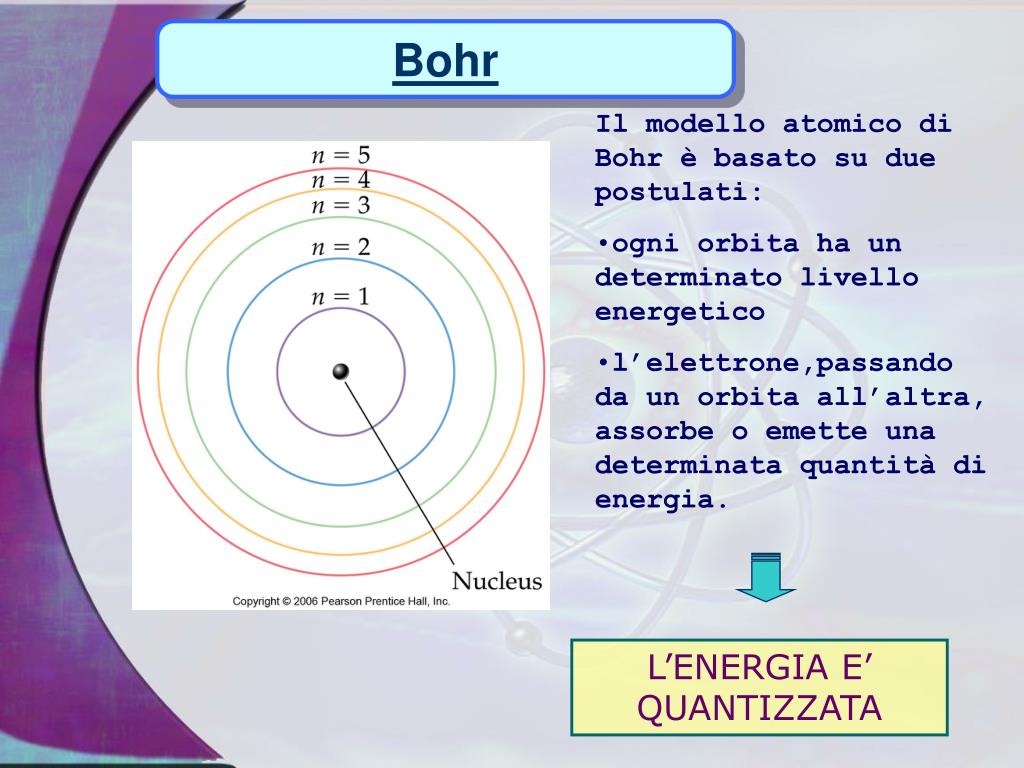
2. Transizioni Elettroniche e Spettri Atomici
Un altro aspetto cruciale del modello di Bohr è la spiegazione degli spettri atomici. Bohr propose che gli elettroni potessero transire tra le orbite quantizzate assorbendo o emettendo energia sotto forma di fotoni. Quando un elettrone salta da un'orbita a un'altra con energia inferiore (transizione di emissione), emette un fotone con un'energia pari alla differenza di energia tra le due orbite. Viceversa, quando un elettrone assorbe un fotone con l'energia appropriata, può saltare a un'orbita con energia superiore (transizione di assorbimento).
La frequenza (e quindi il colore) del fotone emesso o assorbito è determinata dalla differenza di energia tra le orbite, secondo la relazione di Planck: E = hν, dove E è l'energia, h è la costante di Planck e ν è la frequenza. Questo spiega perché gli atomi emettono o assorbono luce solo a frequenze specifiche, dando origine a spettri atomici discreti, caratteristici di ciascun elemento.
Bohr riuscì a calcolare con precisione le frequenze delle linee spettrali dell'idrogeno, utilizzando una formula derivata dalle sue assunzioni. Questo successo fu una forte convalida del suo modello.
3. Il Modello di Bohr per l'Idrogeno
Il modello di Bohr ottenne il suo successo maggiore nello spiegare lo spettro dell'atomo di idrogeno, l'atomo più semplice con un solo protone e un solo elettrone. La formula di Bohr per l'energia degli elettroni nell'idrogeno è:
En = -RH/n2
dove En è l'energia dell'elettrone nell'orbita n, RH è la costante di Rydberg (circa 13.6 eV) e n è il numero quantico principale. Questa formula predice con accuratezza le energie delle orbite dell'idrogeno e le frequenze dei fotoni emessi o assorbiti nelle transizioni elettroniche.

La serie di Lyman, Balmer, Paschen, ecc., nello spettro dell'idrogeno corrispondono a transizioni elettroniche verso orbite specifiche (n=1, n=2, n=3, rispettivamente). Ad esempio, la serie di Balmer, che cade nella regione visibile dello spettro, corrisponde a transizioni verso l'orbita con n=2.
4. Limitazioni del Modello di Bohr
Nonostante il suo successo nello spiegare lo spettro dell'idrogeno, il modello di Bohr presentava delle limitazioni significative. Non era in grado di spiegare gli spettri di atomi più complessi con più di un elettrone. Inoltre, il modello assumeva che gli elettroni si muovessero in orbite circolari ben definite, il che si rivelò un'approssimazione troppo semplicistica. Infine, non teneva conto dell'effetto Zeeman (la divisione delle linee spettrali in presenza di un campo magnetico) e dell'effetto Stark (la divisione delle linee spettrali in presenza di un campo elettrico) in modo accurato.
Il principio di indeterminazione di Heisenberg, sviluppato successivamente, dimostrò che non è possibile conoscere simultaneamente la posizione e la quantità di moto di un elettrone con precisione arbitraria. Questo metteva in discussione l'idea di orbite ben definite.
L'introduzione della meccanica quantistica, con l'equazione di Schrödinger, fornì un modello più accurato e completo della struttura atomica, superando le limitazioni del modello di Bohr. La meccanica quantistica descrive gli elettroni non come particelle puntiformi che si muovono in orbite, ma come onde di probabilità (orbitali) che circondano il nucleo.
Mappa Concettuale del Modello di Bohr
Una mappa concettuale visualizza le relazioni tra i concetti chiave del modello di Bohr. Al centro della mappa si trova il concetto principale: "Modello Atomico di Bohr". Da questo centro si diramano i seguenti concetti:
- Postulati di Bohr: Orbite quantizzate, transizioni elettroniche, frequenza del fotone.
- Spettri Atomici: Linee spettrali, serie di Lyman, Balmer, Paschen.
- Idrogeno: Formula dell'energia, costante di Rydberg.
- Limitazioni: Atomi polielettronici, orbite circolari, effetto Zeeman, principio di indeterminazione.
Ogni concetto è collegato agli altri attraverso frecce che indicano le relazioni tra di essi. Ad esempio, "Postulati di Bohr" porta a "Spettri Atomici" perché i postulati spiegano l'origine degli spettri. "Idrogeno" è collegato a "Spettri Atomici" perché il modello di Bohr spiega con successo lo spettro dell'idrogeno. "Limitazioni" è collegato a tutti gli altri concetti perché le limitazioni del modello hanno portato allo sviluppo di modelli più avanzati.
Real-World Examples and Data
Spettroscopia: The most direct application of Bohr's model is in the field of spectroscopy. Spectroscopic analysis of light emitted from different elements is used in astronomy to determine the composition of stars and nebulae. The unique spectral fingerprints of each element, explained by Bohr's transitions, allow astronomers to identify elements in distant celestial objects.

Lasers: Lasers are based on the principle of stimulated emission, which is closely related to Bohr's model of atomic transitions. When atoms are excited to higher energy levels and then stimulated to emit photons, they release light of a specific wavelength. This is a practical application of the concept of quantized energy levels and transitions.
Fireworks: The bright colors in fireworks come from heating different metal salts. When heated, the metal atoms become excited and then release photons of specific wavelengths when electrons fall back to lower energy levels. These wavelengths correspond to specific colors.
Conclusione
Il modello atomico di Bohr, pur con le sue limitazioni, rappresenta un'importante pietra miliare nella storia della fisica. Introducendo il concetto di quantizzazione dell'energia, ha fornito una spiegazione convincente degli spettri atomici e ha aperto la strada allo sviluppo della meccanica quantistica. La sua importanza storica è innegabile, e la sua comprensione è fondamentale per apprezzare i progressi successivi nella fisica atomica. Studiando il modello di Bohr, impariamo l'importanza di formulare teorie audaci, anche se imperfette, per spiegare i fenomeni naturali, e come queste teorie possano essere affinate e superate da modelli più accurati.
Approfondire la meccanica quantistica: Studiare il modello di Bohr è un ottimo punto di partenza, ma per una comprensione più completa della struttura atomica è necessario approfondire la meccanica quantistica e il modello atomico moderno, che descrive gli elettroni non come particelle che orbitano il nucleo, ma come onde di probabilità che occupano gli orbitali atomici.