
La tavola periodica degli elementi è un pilastro fondamentale della chimica, organizzando gli elementi conosciuti in base alle loro proprietà atomiche e chimiche. Una delle distinzioni più importanti all'interno di questa tavola è quella tra metalli e non metalli. Questa divisione, sebbene apparentemente semplice, rivela differenze profonde nel comportamento e nelle applicazioni di questi elementi.
Distinzione Fondamentale: Metalli vs. Non Metalli
La linea di demarcazione tra metalli e non metalli non è netta, ma piuttosto una zona di transizione. Tuttavia, le proprietà generali che distinguono i due gruppi sono ben definite. I metalli tendono ad essere lucenti, malleabili, duttili e buoni conduttori di calore ed elettricità. I non metalli, al contrario, sono spesso opachi, fragili (allo stato solido, se presenti), e cattivi conduttori. La loro abilità di formare ioni è cruciale per capire le loro interazioni chimiche.
Proprietà Fisiche Distintive
Una delle proprietà più evidenti dei metalli è la loro lucentezza, dovuta alla capacità degli elettroni di superficie di assorbire e riemettere luce. Questo è evidente nell'oro (Au), nell'argento (Ag) e nel rame (Cu), tutti ampiamente utilizzati in gioielleria ed elettronica proprio per questa caratteristica e per la loro conduttività. La malleabilità e la duttilità, ovvero la capacità di essere modellati in lamine sottili e fili, sono altre caratteristiche chiave, essenziali per la fabbricazione di cavi, tubi e altri componenti metallici.
I non metalli, d'altra parte, spesso si presentano come gas (come l'ossigeno (O2) e l'azoto (N2)), liquidi (come il bromo (Br2)) o solidi fragili (come lo zolfo (S) e il carbonio (C) nella forma del diamante). La loro scarsa conduttività termica ed elettrica li rende utili come isolanti.
Proprietà Chimiche Differenziate
Le differenze nelle proprietà fisiche riflettono le differenze nelle proprietà chimiche. I metalli tendono a perdere elettroni durante le reazioni chimiche, formando ioni positivi (cationi). Questo è dovuto alla loro bassa energia di ionizzazione e alla bassa affinità elettronica. Ad esempio, il sodio (Na) reagisce violentemente con l'acqua, perdendo un elettrone e formando lo ione Na+.
I non metalli, al contrario, tendono ad acquistare elettroni durante le reazioni chimiche, formando ioni negativi (anioni). La loro alta affinità elettronica e l'elevata elettronegatività li rendono avidi di elettroni. Il cloro (Cl), ad esempio, reagisce con il sodio per formare cloruro di sodio (NaCl), dove il cloro acquista un elettrone per formare lo ione Cl-.

Posizione nella Tavola Periodica e Tendenze
I metalli si trovano principalmente sul lato sinistro e al centro della tavola periodica. I metalli alcalini (gruppo 1) e i metalli alcalino-terrosi (gruppo 2) sono tra i metalli più reattivi. I metalli di transizione (gruppi 3-12) mostrano una varietà di proprietà e sono spesso utilizzati come catalizzatori. I lantanidi e gli attinidi, situati nella parte inferiore della tavola, sono metalli con proprietà uniche, molti dei quali sono radioattivi.
I non metalli si trovano principalmente sul lato destro della tavola periodica. Gli alogeni (gruppo 17) sono non metalli molto reattivi che formano facilmente anioni. I gas nobili (gruppo 18) sono non metalli inerti, con gusci elettronici completi, e quindi scarsa tendenza a reagire.
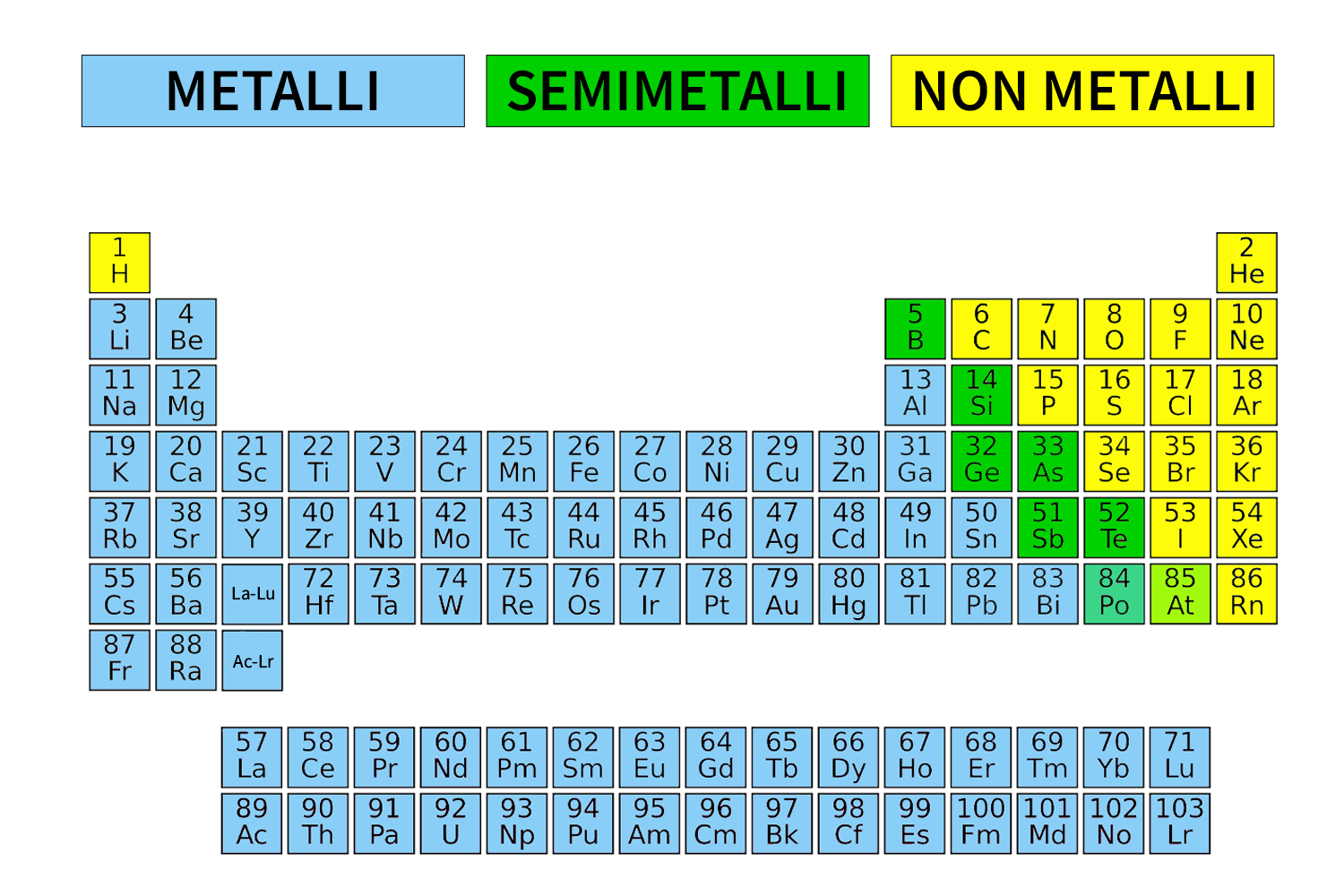
Metalli, Non Metalli e Semimetalli (Metalloidi)
Oltre ai metalli e ai non metalli, esiste una categoria intermedia chiamata semimetalli o metalloidi. Questi elementi (come il silicio (Si), il germanio (Ge), l'arsenico (As) e l'antimonio (Sb)) possiedono proprietà intermedie tra metalli e non metalli. La loro conduttività elettrica, ad esempio, può essere modificata controllando le impurità presenti nel materiale, rendendoli fondamentali nell'industria dei semiconduttori.
Esempi Concreti e Applicazioni
La comprensione delle proprietà dei metalli e dei non metalli è cruciale per numerose applicazioni tecnologiche e industriali.

Metalli: Applicazioni Estese
Ferro (Fe): Il ferro è il metallo più utilizzato al mondo, principalmente sotto forma di leghe come l'acciaio. L'acciaio è impiegato nell'edilizia, nella costruzione di macchinari, nei trasporti e in molti altri settori. La sua resistenza e relativamente basso costo lo rendono un materiale insostituibile.
Alluminio (Al): L'alluminio è leggero, resistente alla corrosione e buon conduttore. È ampiamente utilizzato nell'industria aerospaziale, nell'imballaggio alimentare (lattine), nei trasporti e nell'edilizia.
Rame (Cu): Il rame è un eccellente conduttore di elettricità ed è quindi utilizzato in cavi elettrici, motori, trasformatori e altri componenti elettrici ed elettronici. Le tubature in rame sono utilizzate per il trasporto di acqua e gas.
Oro (Au) e Argento (Ag): L'oro e l'argento sono metalli nobili, resistenti alla corrosione e ottimi conduttori. Sono utilizzati in gioielleria, elettronica (contatti elettrici), odontoiatria e come riserva di valore.
Non Metalli: Ruoli Essenziali
Ossigeno (O2): L'ossigeno è essenziale per la respirazione e per la combustione. È utilizzato in medicina, nell'industria metallurgica e in molti processi chimici.
Azoto (N2): L'azoto è il componente principale dell'atmosfera terrestre. È utilizzato nella produzione di fertilizzanti (ammoniaca), esplosivi (nitroglicerina) e come gas inerte per proteggere materiali sensibili all'ossidazione.
Carbonio (C): Il carbonio è l'elemento base della chimica organica. Si presenta in diverse forme allotropiche, tra cui il diamante (duro e trasparente) e la grafite (morbida e conduttiva). Il carbonio è fondamentale per la vita e per l'industria chimica.
Silicio (Si): Il silicio è un semimetallo cruciale nell'industria dei semiconduttori. È utilizzato nella produzione di microchip, transistor e celle solari. La sua abbondanza e le sue proprietà semiconduttive lo rendono un materiale indispensabile per l'elettronica moderna.

Tendenze Periodiche e Comportamento Chimico
La tavola periodica permette di prevedere alcune tendenze nel comportamento dei metalli e dei non metalli. L'elettronegatività, l'energia di ionizzazione e l'affinità elettronica aumentano generalmente da sinistra a destra e dal basso verso l'alto nella tavola periodica. Questo significa che i non metalli tendono ad essere più elettronegativi e ad avere una maggiore affinità elettronica rispetto ai metalli.
La reattività dei metalli (la loro tendenza a perdere elettroni) aumenta generalmente scendendo lungo un gruppo, mentre la reattività dei non metalli (la loro tendenza ad acquistare elettroni) aumenta generalmente salendo lungo un gruppo.
Conclusione
La distinzione tra metalli e non metalli nella tavola periodica è una semplificazione utile per comprendere le proprietà e il comportamento degli elementi. Sebbene esistano zone di transizione e comportamenti anomali, la conoscenza delle proprietà generali dei metalli e dei non metalli è essenziale per la chimica, la fisica dei materiali e molte applicazioni tecnologiche. Comprendere queste differenze ci permette di progettare nuovi materiali e di ottimizzare processi industriali.
Per approfondire ulteriormente, si consiglia di consultare testi di chimica generale e inorganica, e di esplorare risorse online interattive sulla tavola periodica. La curiosità e l'apprendimento continuo sono fondamentali per apprezzare la bellezza e la complessità della chimica!