
Capita a tutti di sentirsi persi di fronte a concetti scientifici complessi. La chimica, in particolare, può sembrare un labirinto di regole e formule. Ma non scoraggiarti! Anche la legge delle proporzioni multiple di Dalton, che a prima vista può apparire ostica, può essere compresa e padroneggiata con il giusto approccio. In fondo, la scienza è un viaggio alla scoperta del mondo che ci circonda, e ogni passo, anche il più piccolo, è un successo.
Cos'è la Legge delle Proporzioni Multiple? Un'Analisi Dettagliata
La legge delle proporzioni multiple, formulata da John Dalton all'inizio del XIX secolo, è una pietra miliare nella storia della chimica. Cerchiamo di capire insieme di cosa si tratta, passo dopo passo. In sostanza, la legge afferma che:
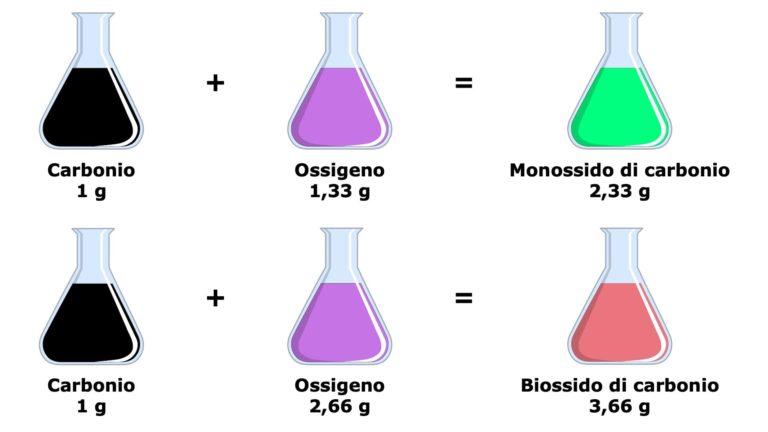
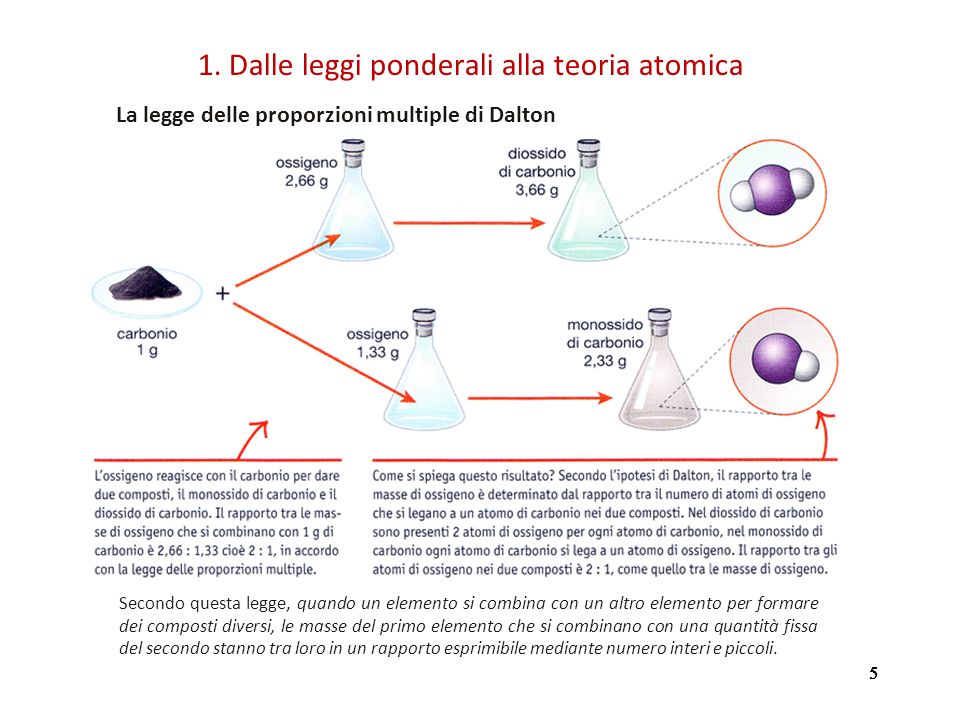
Quando due elementi formano più di un composto, le masse di un elemento che si combinano con una massa fissa dell'altro elemento stanno tra loro in rapporti di numeri interi piccoli.
Sembra complicato? Scomponiamolo. Immagina di avere due elementi, chiamiamoli A e B. Questi due elementi possono combinarsi in modi diversi, formando composti diversi. La legge ci dice che se prendiamo una quantità fissa di A e vediamo quanto B si combina con essa in ciascun composto, le quantità di B in questi composti saranno in un rapporto semplice, fatto di numeri interi piccoli (come 1:2, 2:3, 1:4, ecc.).
Esempio pratico: Consideriamo l'azoto (N) e l'ossigeno (O). Questi elementi possono formare diversi ossidi di azoto, come N2O (protossido di azoto), NO (ossido di azoto), NO2 (biossido di azoto) e N2O5 (pentossido di azoto).

Se fissiamo la massa di azoto a, ad esempio, 28 grammi (che corrisponde a 2 moli di azoto atomico), possiamo osservare le masse di ossigeno che si combinano con questa quantità fissa di azoto nei diversi composti:
- N2O: 16 grammi di ossigeno
- NO: 32 grammi di ossigeno
- NO2: 64 grammi di ossigeno
- N2O5: 80 grammi di ossigeno
Notiamo che le masse di ossigeno (16, 32, 64, 80) sono in un rapporto di numeri interi piccoli: 1:2:4:5. Questo conferma la legge delle proporzioni multiple.
Perché questa legge è importante?
La legge di Dalton è stata fondamentale per lo sviluppo della teoria atomica. Ha fornito un'ulteriore prova dell'esistenza degli atomi e ha suggerito che gli elementi si combinano in rapporti ben definiti per formare composti. Ha permesso di razionalizzare i dati sperimentali disponibili all'epoca e ha spianato la strada per la comprensione della composizione chimica della materia.

Superare le Difficoltà: Strategie per l'Apprendimento
Molti studenti trovano difficile afferrare la legge delle proporzioni multiple. Ecco alcuni motivi comuni e come affrontarli:
- Difficoltà con i concetti di base: Una solida comprensione dei concetti di elemento, composto, atomo, molecola e massa atomica è essenziale. Se questi concetti non sono chiari, è importante rivederli prima di affrontare la legge di Dalton.
- Difficoltà con i calcoli: La legge implica la comprensione dei rapporti e delle proporzioni. Esercitarsi con esempi numerici è fondamentale per acquisire familiarità con i calcoli necessari.
- Astrazione: La legge di Dalton è un concetto astratto. Utilizzare analogie e modelli visivi può aiutare a renderla più concreta.
- Mancanza di esempi pratici: Vedere come la legge si applica a composti reali aiuta a comprenderne il significato.
Consigli pratici per studenti:
- Concentrati sui fondamenti: Assicurati di avere una solida base di chimica di base prima di addentrarti nella legge di Dalton.
- Risolvi molti esercizi: Più ti eserciti, più facile diventerà applicare la legge. Inizia con esercizi semplici e poi passa a quelli più complessi.
- Cerca spiegazioni alternative: Se non capisci una spiegazione, cercane un'altra. Ci sono molte risorse online e libri di testo che possono aiutarti.
- Chiedi aiuto: Non aver paura di chiedere aiuto al tuo insegnante, a un tutor o a un compagno di studi.
- Crea mappe concettuali: Le mappe concettuali possono aiutarti a visualizzare le relazioni tra i diversi concetti.
Consigli per insegnanti e genitori:
- Usa esempi concreti: Spiega la legge utilizzando esempi di composti comuni, come l'acqua (H2O) e il perossido di idrogeno (H2O2).
- Utilizza analogie: Confronta la legge di Dalton con situazioni della vita reale, come le ricette di cucina.
- Incoraggia la discussione: Chiedi agli studenti di spiegare la legge con le proprie parole.
- Fornisci feedback positivo: Incoraggia gli studenti a persistere, anche se all'inizio fanno fatica.
- Utilizza risorse visive: Utilizza diagrammi, animazioni e video per rendere la legge più comprensibile.
- Promuovi l'apprendimento attivo: Incoraggia gli studenti a porre domande e a partecipare alle discussioni.
- Valuta la comprensione concettuale: Non limitarti a valutare la capacità di risolvere problemi. Valuta anche la comprensione dei concetti sottostanti.
Dalton e la Teoria Atomica: Un Legame Indissolubile
La legge delle proporzioni multiple è stata un tassello fondamentale nella formulazione della teoria atomica di Dalton. La sua teoria, presentata nel 1803, postulava che:
- La materia è costituita da particelle indivisibili chiamate atomi.
- Tutti gli atomi di un dato elemento sono identici in massa e proprietà.
- Gli atomi di elementi diversi differiscono in massa e proprietà.
- I composti sono formati dalla combinazione di atomi di elementi diversi in rapporti di numeri interi piccoli.
- Durante le reazioni chimiche, gli atomi non vengono creati né distrutti, ma semplicemente riorganizzati.
La legge delle proporzioni multiple supporta direttamente il punto 4 della teoria di Dalton. Il fatto che le masse degli elementi si combinino in rapporti di numeri interi piccoli suggerisce che gli atomi si combinano in numeri interi per formare molecole.
È importante notare che, sebbene la teoria di Dalton fosse rivoluzionaria per l'epoca, presentava alcune limitazioni. Ad esempio, Dalton credeva che gli atomi fossero indivisibili, il che si è rivelato falso con la scoperta delle particelle subatomiche (protoni, neutroni ed elettroni). Tuttavia, la teoria di Dalton ha fornito una base solida per lo sviluppo della chimica moderna.
Oltre la Teoria: L'Importanza della Pratica
Comprendere la legge delle proporzioni multiple non significa solo memorizzare una definizione. Significa essere in grado di applicarla a problemi concreti e di utilizzarla per interpretare i dati sperimentali. Ecco alcuni esempi di come la legge può essere applicata nella pratica:
- Determinazione della formula empirica di un composto: Conoscendo le masse degli elementi in un composto, è possibile utilizzare la legge delle proporzioni multiple per determinare la sua formula empirica (la formula che indica il rapporto più semplice tra gli atomi degli elementi).
- Verifica della purezza di un composto: Confrontando le masse degli elementi in un campione con le masse teoriche previste dalla formula chimica, è possibile valutare la purezza del composto.
- Previsione delle proprietà di un composto: Conoscendo la composizione chimica di un composto, è possibile prevedere alcune delle sue proprietà fisiche e chimiche.
Esercizio: Due ossidi di rame contengono rispettivamente il 79.9% e l'88.8% di rame. Dimostra che questi dati sono in accordo con la legge delle proporzioni multiple.
Soluzione: Calcoliamo la percentuale di ossigeno in ciascun ossido: nel primo ossido, l'ossigeno è il 20.1% (100% - 79.9%); nel secondo ossido, l'ossigeno è l'11.2% (100% - 88.8%). Fissiamo la massa di rame a 100 grammi. Nel primo ossido, 100 grammi di rame si combinano con 20.1/79.9 * 100 = 25.15 grammi di ossigeno. Nel secondo ossido, 100 grammi di rame si combinano con 11.2/88.8 * 100 = 12.61 grammi di ossigeno. Il rapporto tra le masse di ossigeno è 25.15 / 12.61 = 1.99 ≈ 2:1. Questo dimostra che i dati sono in accordo con la legge delle proporzioni multiple.
Un Viaggio Continuo: Alla Scoperta della Chimica
La legge delle proporzioni multiple è solo una delle tante tappe nel tuo viaggio alla scoperta della chimica. Non scoraggiarti se all'inizio ti sembra difficile. Con impegno, perseveranza e le giuste strategie, puoi superare qualsiasi ostacolo. Ricorda, la chimica è ovunque intorno a noi, e comprendere i suoi principi ti aprirà le porte a un mondo di meraviglie. Continua a esplorare, a sperimentare e a porre domande. La scienza è un'avventura che vale la pena vivere!