Quante volte ti sei chiesto cosa tiene insieme la materia? Perché l'acqua è liquida a temperatura ambiente mentre il sale è un solido cristallino? La risposta a queste domande risiede nei legami chimici, le forze invisibili che governano il comportamento degli atomi e delle molecole. Comprendere i legami chimici può sembrare un compito arduo, un labirinto di concetti complessi riservato agli scienziati. Ma in realtà, le basi sono sorprendentemente accessibili e una volta comprese, aprono una finestra sul mondo che ci circonda. Questo articolo si propone di spiegare i legami chimici in modo semplice e chiaro, fornendoti gli strumenti per decifrare la "lingua" della chimica. Immagina di poter "vedere" come gli atomi si uniscono per formare ogni cosa, dal tuo smartphone al tuo corpo! Non è magia, è chimica, e con la giusta guida, è alla portata di tutti.
Cosa Sono i Legami Chimici?
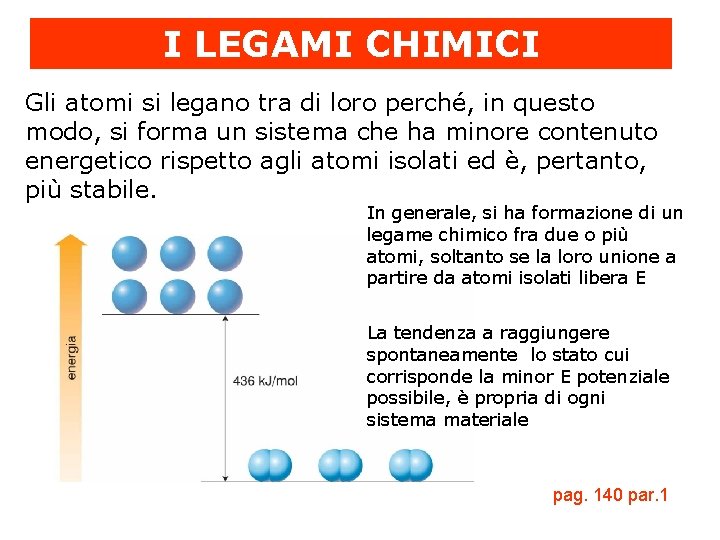
In parole semplici, un legame chimico è una forza di attrazione che tiene uniti due o più atomi. Pensa a un magnete: avvicinandolo a un oggetto di metallo, si attraggono e si uniscono. I legami chimici funzionano in modo simile, ma l'attrazione è tra le cariche positive del nucleo atomico e le cariche negative degli elettroni.
Gli atomi non si uniscono a caso. Tendono a formare legami per raggiungere una configurazione elettronica stabile, simile a quella dei gas nobili (elio, neon, argon, ecc.). Questi gas sono particolarmente stabili e inerti, e gli altri atomi "desiderano" imitarli acquisendo o perdendo elettroni, o condividendoli.
Esistono diversi tipi di legami chimici, ognuno con le sue caratteristiche e proprietà. I principali sono: il legame ionico, il legame covalente e il legame metallico.
Il Legame Ionico
Il legame ionico si forma quando un atomo cede uno o più elettroni a un altro atomo. L'atomo che cede gli elettroni diventa uno ione positivo (catione), mentre l'atomo che li riceve diventa uno ione negativo (anione). Questi ioni di carica opposta si attraggono fortemente, creando un legame ionico. Un esempio classico è il cloruro di sodio (NaCl), il comune sale da cucina.
Esempio pratico: Il sodio (Na) ha un elettrone in più rispetto a una configurazione stabile, mentre il cloro (Cl) ne ha uno in meno. Il sodio cede il suo elettrone al cloro, formando uno ione Na+ e uno ione Cl-. L'attrazione elettrostatica tra questi ioni crea il legame ionico, dando origine al sale da cucina.

I composti ionici sono generalmente solidi a temperatura ambiente, con elevati punti di fusione ed ebollizione. Sono anche buoni conduttori di elettricità quando disciolti in acqua, perché gli ioni si muovono liberamente.
Il Legame Covalente
Il legame covalente si forma quando due atomi condividono uno o più elettroni. Invece di cedere o acquisire elettroni, gli atomi mettono in comune i loro elettroni di valenza per raggiungere una configurazione elettronica stabile. L'acqua (H2O) è un esempio perfetto di composto con legami covalenti.
Esempio pratico: L'atomo di ossigeno (O) ha bisogno di due elettroni per completare il suo guscio di valenza, mentre ogni atomo di idrogeno (H) ne ha bisogno di uno. Ogni atomo di idrogeno condivide un elettrone con l'ossigeno, formando un legame covalente. L'ossigeno condivide a sua volta un elettrone con ogni idrogeno, completando il suo guscio di valenza. In questo modo, si formano due legami covalenti tra l'ossigeno e i due idrogeni, creando la molecola d'acqua.
I legami covalenti possono essere singoli, doppi o tripli, a seconda del numero di coppie di elettroni condivise. Più elettroni vengono condivisi, più forte è il legame.

I composti covalenti hanno proprietà diverse dai composti ionici. Spesso sono gas, liquidi o solidi a basso punto di fusione. La loro conducibilità elettrica è generalmente bassa, a meno che non siano polari (cioè, con una distribuzione di carica asimmetrica).
Il Legame Metallico
Il legame metallico è un tipo di legame che si trova nei metalli. In un metallo, gli atomi sono disposti in un reticolo cristallino e gli elettroni di valenza sono delocalizzati, cioè non appartengono a un singolo atomo ma sono liberi di muoversi in tutto il metallo. Questa "nuvola" di elettroni negativi tiene uniti gli ioni metallici positivi.
Esempio pratico: Pensa a un pezzo di rame. Gli atomi di rame sono disposti in un reticolo, e gli elettroni di valenza si muovono liberamente tra gli atomi. Questa mobilità degli elettroni è responsabile della buona conducibilità elettrica e termica dei metalli.
Il legame metallico è responsabile di molte delle proprietà caratteristiche dei metalli, come la lucentezza, la malleabilità (la capacità di essere deformati senza rompersi) e la duttilità (la capacità di essere tirati in fili).

Forze Intermolecolari: Legami Deboli ma Importanti
Oltre ai legami chimici che tengono uniti gli atomi all'interno di una molecola, esistono anche forze intermolecolari, che sono attrazioni più deboli tra molecole diverse. Queste forze influenzano le proprietà fisiche delle sostanze, come il punto di ebollizione e la tensione superficiale.
Le principali forze intermolecolari sono:
* Forze di Van der Waals: Sono forze deboli che si formano tra molecole non polari a causa di fluttuazioni temporanee nella distribuzione degli elettroni. * Forze dipolo-dipolo: Si formano tra molecole polari, dove c'è una distribuzione di carica asimmetrica. * Legame idrogeno: È un tipo particolarmente forte di forza dipolo-dipolo che si forma tra un atomo di idrogeno legato a un atomo molto elettronegativo (come ossigeno, azoto o fluoro) e un altro atomo elettronegativo. Il legame idrogeno è cruciale per le proprietà dell'acqua e per la struttura delle proteine e del DNA.Perché Conoscere i Legami Chimici è Importante?
Comprendere i legami chimici non è solo un esercizio teorico. Ha applicazioni pratiche in molti campi, tra cui:

Risorse Utili per Approfondire
Se desideri approfondire ulteriormente la tua conoscenza dei legami chimici, ecco alcune risorse utili:
* Libri di testo di chimica: I libri di testo di chimica generale sono un'ottima fonte di informazioni dettagliate sui legami chimici. * Siti web di chimica: Esistono molti siti web che offrono spiegazioni chiare e concise sui legami chimici, spesso accompagnate da animazioni e video. * Documenti PDF: Puoi trovare online documenti PDF che riassumono i concetti chiave dei legami chimici. Cerca "Legami Chimici Spiegati In Modo Semplice Pdf" su un motore di ricerca. * Video tutorial: Piattaforme come YouTube offrono numerosi video tutorial che spiegano i legami chimici in modo visivo e coinvolgente.In Conclusione
I legami chimici sono le fondamenta della materia. Comprendere come gli atomi si uniscono per formare molecole ci permette di svelare i segreti del mondo che ci circonda. Che tu sia uno studente, un appassionato di scienza o semplicemente curioso di capire come funziona l'universo, la conoscenza dei legami chimici è un investimento prezioso. Non lasciarti intimidire dalla complessità apparente: con un po' di impegno e le giuste risorse, puoi padroneggiare i concetti chiave e aprire una porta su un mondo affascinante.