
La reazione di neutralizzazione è una reazione chimica che avviene tra un acido e una base. Il prodotto principale di questa reazione è un sale e, nella maggior parte dei casi, acqua. Questo processo è fondamentale per comprendere molti fenomeni chimici che osserviamo quotidianamente e riveste un'importanza cruciale in diversi campi, dalla chimica analitica alla biologia.
Cos'è la Reazione di Neutralizzazione?
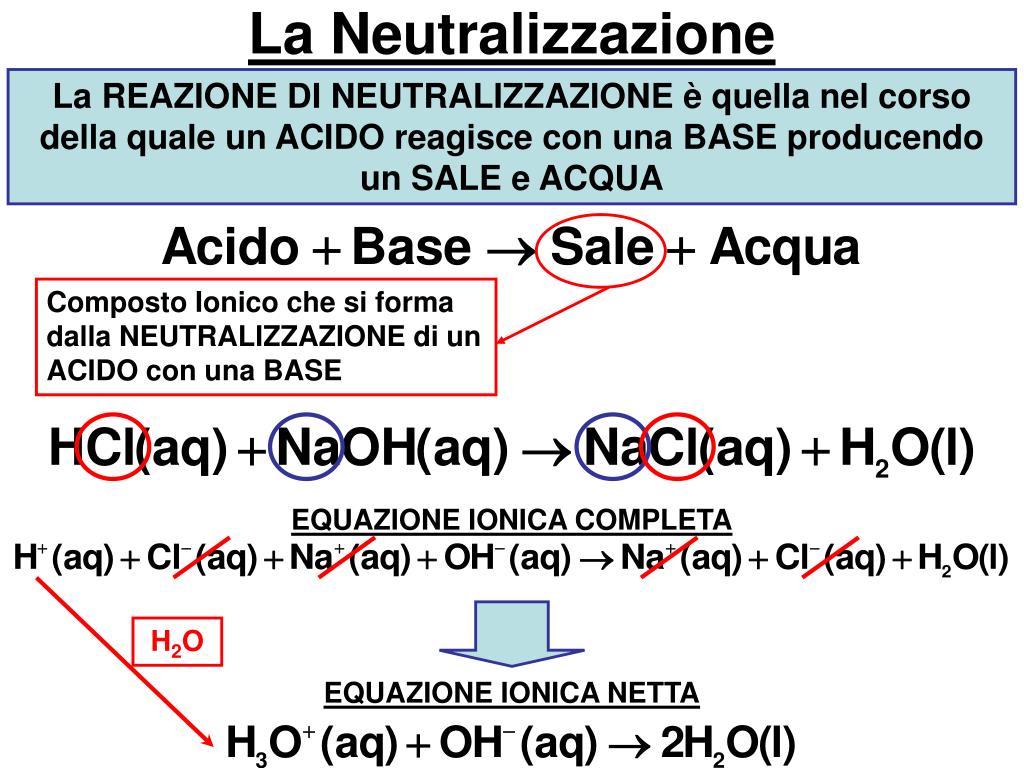
La reazione di neutralizzazione, a livello ionico, comporta la combinazione di ioni idronio (H3O+ o, semplificando, H+) provenienti dall'acido, con ioni idrossido (OH-) provenienti dalla base. Questa reazione produce acqua (H2O). La formazione del sale dipende invece dagli ioni rimanenti nell'acido e nella base dopo la neutralizzazione degli ioni H+ e OH-. Ad esempio, la reazione tra acido cloridrico (HCl) e idrossido di sodio (NaOH) produce cloruro di sodio (NaCl), il comune sale da cucina, e acqua.
In termini più formali, si può definire una reazione di neutralizzazione come quella in cui l'effetto di un acido e di una base si annullano a vicenda, portando ad una soluzione con un pH tendenzialmente neutro (pH ≈ 7). Tuttavia, è importante notare che non tutte le reazioni di neutralizzazione producono soluzioni perfettamente neutre. La natura acida o basica del sale formato può influenzare il pH finale della soluzione. Questo concetto è strettamente legato all'idrolisi salina.
Perché è Importante Studiare la Neutralizzazione?
La reazione di neutralizzazione è un concetto pilastro della chimica. La sua comprensione è essenziale per una solida base in chimica acido-base, titolazioni, e per capire i processi chimici che avvengono in ambienti naturali e industriali. Senza una buona comprensione di questo processo, gli studenti potrebbero avere difficoltà ad affrontare concetti chimici più avanzati.
Come afferma Linus Pauling, premio Nobel per la chimica, "La comprensione delle reazioni chimiche è essenziale per la comprensione del mondo che ci circonda." La neutralizzazione, in particolare, è ovunque, dalle reazioni che avvengono nel nostro stomaco durante la digestione, fino ai processi di trattamento delle acque reflue.
Come Influisce sugli Studenti?
Molti studenti trovano inizialmente difficile la distinzione tra acidi e basi, e la comprensione del meccanismo della reazione di neutralizzazione. Spesso, la difficoltà risiede nel visualizzare il movimento degli ioni e nel comprendere come la forza relativa dell'acido e della base influenzi il pH della soluzione risultante. Per superare queste difficoltà, è cruciale utilizzare esempi concreti e dimostrazioni di laboratorio. L'uso di indicatori di pH, come il tornasole o la fenolftaleina, può rendere visibile il processo di neutralizzazione e facilitare la comprensione.
Un approccio pratico può includere la realizzazione di semplici titolazioni in laboratorio, utilizzando ad esempio aceto (acido acetico) e bicarbonato di sodio (una base). Gli studenti possono misurare il pH della soluzione durante l'aggiunta graduale della base all'acido, osservando come il pH si avvicina al valore neutro. Questo tipo di esperienza pratica rende il concetto di neutralizzazione più tangibile e memorabile.

Applicazioni Pratiche nella Scuola e nella Vita Quotidiana
Le applicazioni pratiche della neutralizzazione sono numerose. In ambito scolastico, la neutralizzazione è utilizzata per esperimenti di chimica analitica, come le titolazioni acido-base. Queste titolazioni permettono di determinare la concentrazione di una soluzione acida o basica sconosciuta. Inoltre, la neutralizzazione è coinvolta nella preparazione di alcuni prodotti chimici utilizzati nei laboratori scolastici.
Nella vita quotidiana, la neutralizzazione è presente in molti processi. Ad esempio, l'uso di antiacidi per alleviare il bruciore di stomaco si basa sul principio della neutralizzazione: gli antiacidi contengono basi deboli che neutralizzano l'acido cloridrico presente nello stomaco. Inoltre, la neutralizzazione è utilizzata nel trattamento delle acque reflue per rimuovere sostanze acide o basiche che potrebbero danneggiare l'ambiente.
Comprendere la reazione di neutralizzazione è quindi fondamentale per gli studenti non solo per superare gli esami di chimica, ma anche per acquisire una consapevolezza maggiore dei processi chimici che avvengono nel mondo che li circonda. In definitiva, una solida base in chimica acido-base permette di affrontare con maggiore sicurezza e competenza le sfide scientifiche del futuro.