Capita a tutti di sentirsi un po' persi quando si affronta il mondo degli orbitali atomici. Non siete soli! La chimica quantistica, con i suoi numeri e concetti astratti, può sembrare un labirinto. Ma non temete, la chiave per sbloccare questo labirinto sta nel comprendere i tre numeri quantici che definiscono ogni orbitale. Una volta capito questo, la strada diventa molto più chiara e, vi assicuro, incredibilmente affascinante!
I Tre Moschettieri degli Orbitali: Una Panoramica
Ogni orbitale atomico è descritto univocamente da tre numeri quantici. Questi numeri, come un codice identificativo, ci forniscono informazioni cruciali sulla forma, l'energia e l'orientamento spaziale dell'orbitale stesso. Pensateli come le coordinate GPS di un elettrone: ci dicono dove è più probabile trovarlo attorno al nucleo.
I tre numeri quantici sono:
- Numero quantico principale (n)
- Numero quantico secondario o angolare (l)
- Numero quantico magnetico (ml)
Analizziamoli uno per uno.
1. Il Numero Quantico Principale (n): Il Livello Energetico
Il numero quantico principale, indicato con la lettera n, è il più facile da capire. Rappresenta il livello energetico principale dell'elettrone e può assumere solo valori interi positivi: 1, 2, 3, e così via. Un valore di n più alto indica un livello energetico maggiore e un orbitale più distante dal nucleo. Immaginate che il nucleo sia il sole e gli orbitali i pianeti: più alto è "n", più lontano è il pianeta dal sole e maggiore è la sua energia potenziale.
Ad esempio:
- n = 1: Livello energetico più basso (primo guscio elettronico)
- n = 2: Secondo livello energetico (secondo guscio elettronico)
- n = 3: Terzo livello energetico (terzo guscio elettronico)
Consiglio pratico per gli studenti: Visualizzate i livelli energetici come piani di un palazzo. Il piano terra (n=1) è più vicino all'ingresso e richiede meno energia per essere raggiunto. I piani superiori richiedono più energia.
2. Il Numero Quantico Secondario o Angolare (l): La Forma dell'Orbitale
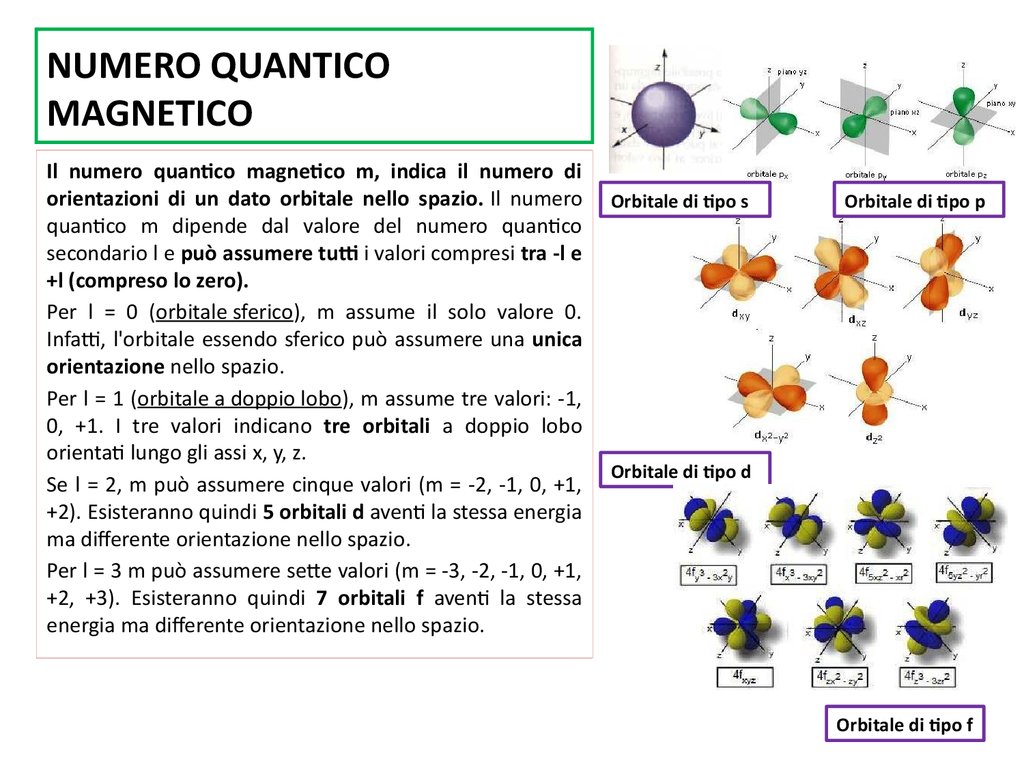
Il numero quantico secondario, o angolare, indicato con la lettera l, descrive la forma dell'orbitale. Per un dato valore di n, l può assumere valori interi da 0 a (n-1). Ogni valore di l corrisponde a una forma orbitale specifica, spesso indicata con una lettera:
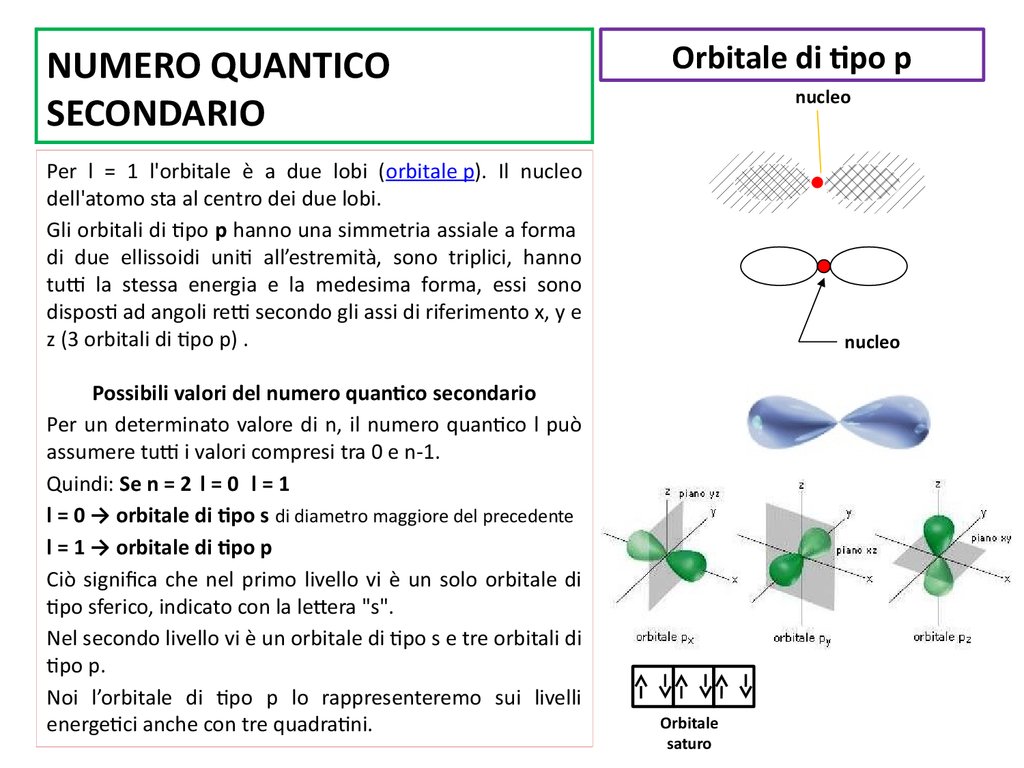
- l = 0: Orbitale s (forma sferica)
- l = 1: Orbitale p (forma a "manubrio" o "dumbbell")
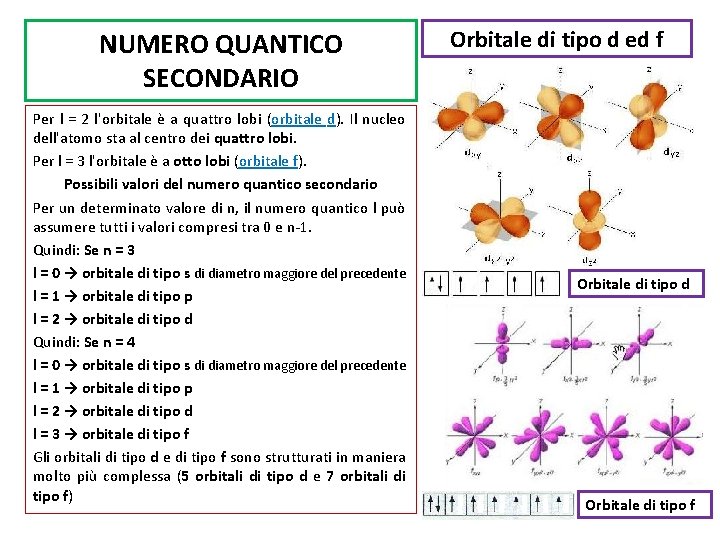
- l = 2: Orbitale d (forme più complesse)
- l = 3: Orbitale f (forme ancora più complesse)
Ad esempio, se n = 2, allora l può essere 0 o 1. Questo significa che nel secondo livello energetico (n=2) troviamo orbitali s (l=0) e orbitali p (l=1). Il numero di orbitali con una data forma (cioè, con un dato valore di l) aumenta all'aumentare di n.
Ricerca educativa: Studi hanno dimostrato che l'utilizzo di modelli tridimensionali degli orbitali (anche virtuali) aiuta enormemente gli studenti a visualizzare le diverse forme e a comprendere il significato del numero quantico secondario. (Johnstone, A. H. (1993). The development of chemistry teaching: A changing response to changing demand.)
Consiglio pratico per gli insegnanti: Utilizzate argilla o plastilina per far costruire agli studenti i diversi orbitali. Questo approccio "hands-on" rende l'apprendimento molto più coinvolgente e memorabile.
3. Il Numero Quantico Magnetico (ml): L'Orientamento nello Spazio
Il numero quantico magnetico, indicato con la lettera ml, descrive l'orientamento spaziale dell'orbitale. Per un dato valore di l, ml può assumere tutti i valori interi da -l a +l, incluso lo zero. Il numero totale di valori possibili di ml per un dato l è (2l + 1). Questo significa che:
- Se l = 0 (orbitale s), ml = 0 (un solo orientamento)
- Se l = 1 (orbitale p), ml = -1, 0, +1 (tre orientamenti: px, py, pz)
- Se l = 2 (orbitale d), ml = -2, -1, 0, +1, +2 (cinque orientamenti)
Quindi, un orbitale p non è solo "a forma di manubrio", ma può orientarsi lungo tre assi diversi nello spazio (x, y, z). Questo orientamento spaziale è fondamentale per capire come gli atomi si legano tra loro per formare molecole.
Esempio pratico: Gli orbitali p sono come tre manubri, ognuno orientato lungo una diversa direzione: uno sull'asse x, uno sull'asse y e uno sull'asse z. Questo permette all'atomo di formare legami in tre dimensioni.
Consiglio pratico per i genitori: Quando aiutate i vostri figli a studiare, incoraggiateli a disegnare gli orbitali p con i loro diversi orientamenti. Questo li aiuterà a visualizzare il concetto e a memorizzarlo meglio.
Mettiamola Insieme: Un Esempio Concreto
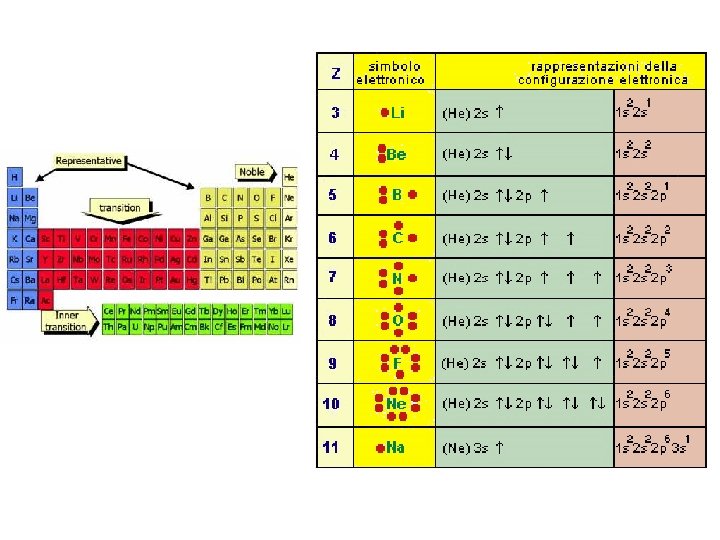
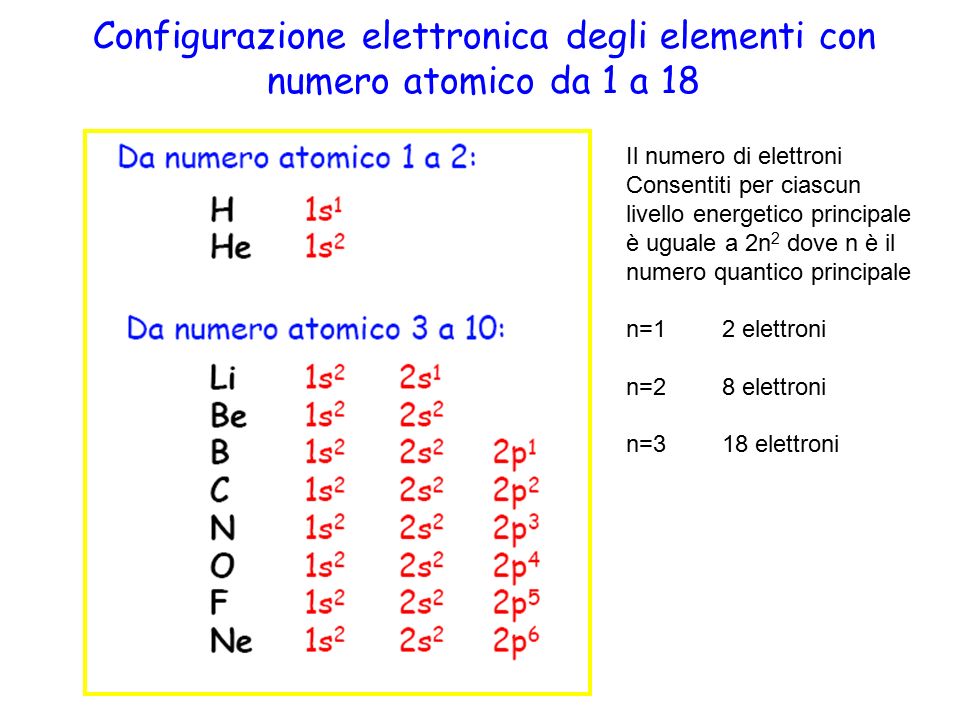
Prendiamo l'atomo di azoto (N), che ha 7 elettroni. La sua configurazione elettronica è 1s² 2s² 2p³. Vediamo come i numeri quantici descrivono questi orbitali:
- 1s²: n=1, l=0, ml=0 (due elettroni nell'orbitale s del primo livello energetico)
- 2s²: n=2, l=0, ml=0 (due elettroni nell'orbitale s del secondo livello energetico)
- 2p³: n=2, l=1, ml=-1, 0, +1 (tre elettroni negli orbitali p del secondo livello energetico)
Questo ci dice che l'atomo di azoto ha due elettroni nell'orbitale s più vicino al nucleo, altri due nell'orbitale s del secondo livello, e tre elettroni distribuiti tra i tre orbitali p del secondo livello. Questa comprensione ci permette di prevedere il comportamento chimico dell'azoto, come la sua capacità di formare tre legami covalenti.
Oltre i Numeri: L'Importanza Concettuale
Comprendere i numeri quantici non è solo una questione di memorizzazione. Si tratta di capire come gli elettroni si organizzano attorno al nucleo e come questa organizzazione determina le proprietà chimiche degli elementi. Questo è il fondamento della chimica e ci permette di prevedere come le sostanze reagiscono tra loro, di progettare nuovi materiali e di comprendere i processi biologici.
Citazione ispiratrice: "La scienza non è solo una collezione di fatti, ma un modo per pensare." – Carl Sagan
Ricordate, la chimica è come un puzzle. I numeri quantici sono solo alcuni dei pezzi, ma sono fondamentali per completare l'immagine. Con un po' di pazienza e dedizione, potrete padroneggiare questi concetti e scoprire la bellezza e la potenza della chimica quantistica!
Non abbiate paura di fare domande, di cercare spiegazioni alternative e di sperimentare con modelli e simulazioni. L'apprendimento è un processo continuo, e ogni passo, anche il più piccolo, vi avvicina alla comprensione di questo affascinante mondo.