
Capita a tutti, studenti, genitori e insegnanti, di sentirsi sopraffatti di fronte alla chimica. Nomi complicati, formule astruse, concetti che sembrano sfuggire... Uno di questi è sicuramente la Legge di Proust, anche nota come Legge delle Proporzioni Definite. Ma non temete! In questo articolo, cercheremo di rendere questo argomento non solo comprensibile, ma anche interessante e applicabile nella vita di tutti i giorni.
Cos'è questa Legge di Proust?
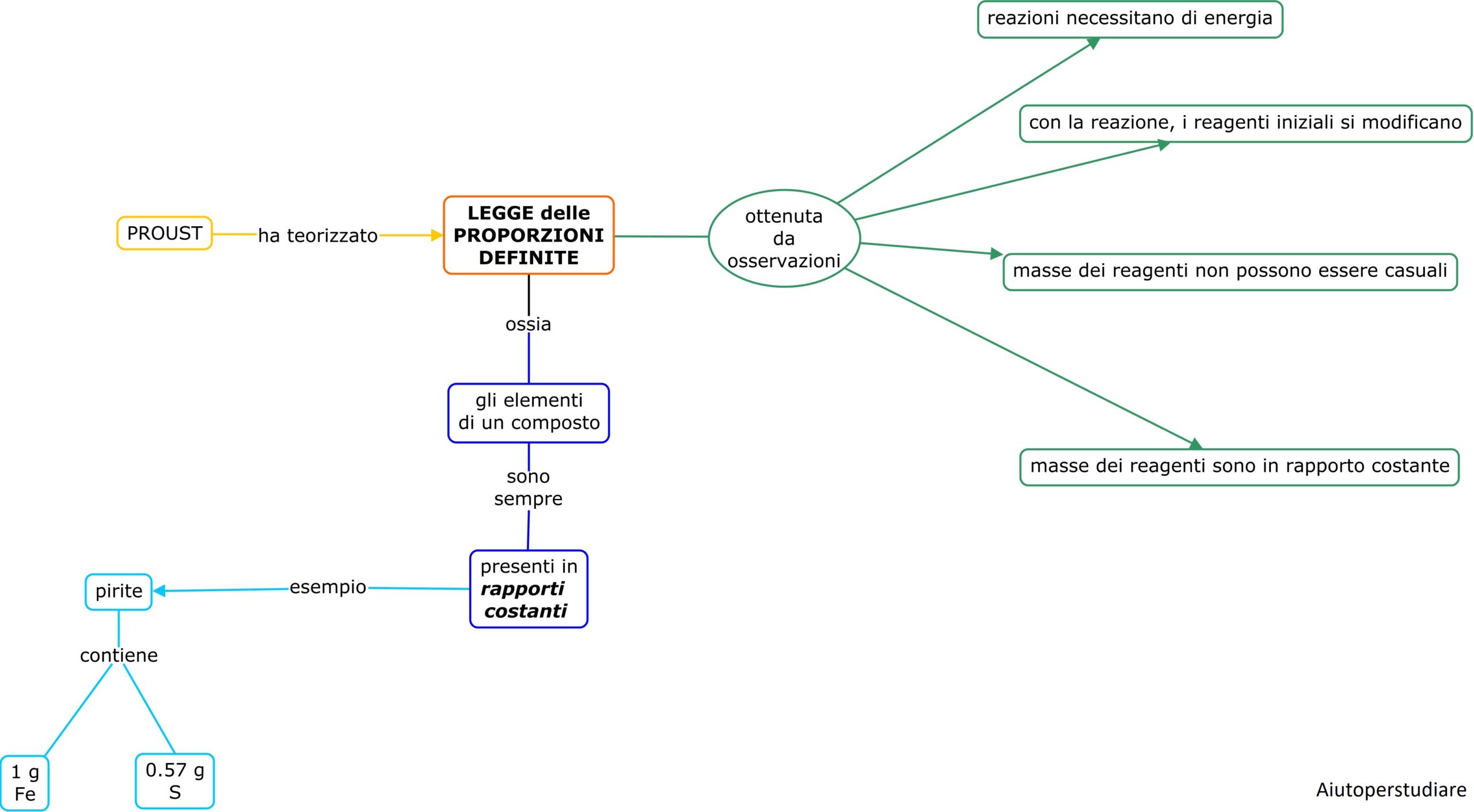
Immaginate di preparare una torta. Avete bisogno di una quantità precisa di farina, zucchero, uova... Se cambiate le proporzioni, la torta potrebbe venire troppo secca, troppo dolce, o semplicemente non lievitare. La Legge di Proust, in termini chimici, è un po' come questa ricetta: ci dice che un composto chimico è sempre formato dagli stessi elementi, combinati nello stesso rapporto di peso, indipendentemente da come è stato preparato.
In altre parole, se prendiamo dell'acqua (H2O), essa sarà sempre composta da due atomi di idrogeno e uno di ossigeno, con un rapporto di peso ben preciso tra i due elementi. Che l'acqua provenga da un fiume, da un ghiacciaio o sia stata prodotta in laboratorio, la sua composizione rimarrà invariata.
Chi era Proust e perché è importante?
Joseph Louis Proust, chimico francese vissuto tra il XVIII e il XIX secolo, è stato il primo a formulare questa legge, basandosi su numerosi esperimenti. Prima di Proust, si pensava che la composizione di un composto potesse variare a seconda del metodo di preparazione. Proust, con la sua rigorosa sperimentazione, ha dimostrato il contrario, ponendo una pietra miliare nella chimica quantitativa.
La sua legge è fondamentale perché ha permesso di stabilire una base solida per la comprensione della composizione dei composti e per lo sviluppo di nuove tecniche di analisi chimica.
La Legge di Proust in Pratica: Esempi Concreti
Per rendere il concetto più chiaro, vediamo alcuni esempi pratici, facilmente replicabili in classe o a casa.
L'Ossido di Magnesio: Un Esperimento Semplice
Un esperimento classico per dimostrare la Legge di Proust è la sintesi dell'ossido di magnesio (MgO). Si può bruciare del nastro di magnesio in aria, ottenendo una polvere bianca: l'ossido di magnesio. Misurando con precisione la massa del magnesio iniziale e la massa dell'ossido ottenuto, si può calcolare il rapporto tra le masse di magnesio e ossigeno. Ripetendo l'esperimento più volte, si noterà che il rapporto rimane costante, indipendentemente dalla quantità di magnesio utilizzata.
Materiali necessari: Nastro di magnesio, crogiolo, becco di Bunsen, bilancia di precisione.
Procedura:
- Pesare il nastro di magnesio.
- Bruciare il nastro nel crogiolo.
- Pesare l'ossido di magnesio ottenuto.
- Calcolare il rapporto tra la massa del magnesio e la massa dell'ossigeno (ottenuta per differenza tra la massa dell'ossido e quella del magnesio).

Risultato atteso: Il rapporto massa(Magnesio)/massa(Ossigeno) dovrebbe essere circa 1.5.
Il Solfato di Rame Idratato: Un Cristallo Perfetto
Un altro esempio interessante è rappresentato dal solfato di rame idratato (CuSO4·5H2O). Questo sale forma dei cristalli blu molto belli. La percentuale di acqua presente nel cristallo è sempre la stessa, indipendentemente dalla dimensione del cristallo stesso. Se si riscalda il solfato di rame idratato, l'acqua evapora, lasciando un residuo bianco: il solfato di rame anidro (CuSO4). Misurando la massa iniziale del cristallo idratato e la massa del residuo anidro, si può calcolare la quantità di acqua persa e verificare che il rapporto tra la massa dell'acqua e la massa del solfato di rame sia costante.
Materiali necessari: Solfato di rame idratato, crogiolo, becco di Bunsen, bilancia di precisione.
Procedura:
- Pesare il solfato di rame idratato.
- Riscaldare il sale nel crogiolo fino a completa disidratazione.
- Pesare il solfato di rame anidro ottenuto.
- Calcolare la massa dell'acqua persa per differenza.
- Calcolare il rapporto tra la massa dell'acqua e la massa del solfato di rame anidro.

Risultato atteso: Il rapporto massa(Acqua)/massa(Solfato di rame anidro) dovrebbe essere circa 0.56.
Oltre l'Esperimento: Implicazioni e Curiosità
La Legge di Proust non è solo un concetto teorico o un esperimento da laboratorio. Ha implicazioni importanti in diversi campi, dalla farmacia all'industria alimentare. Ad esempio, la produzione di farmaci richiede un controllo rigoroso delle proporzioni degli ingredienti per garantire l'efficacia e la sicurezza del prodotto. Allo stesso modo, nell'industria alimentare, la Legge di Proust è fondamentale per garantire la riproducibilità e la qualità dei prodotti.
Attenzione alle eccezioni: I Composti Non Stechiometrici
È importante notare che esistono alcune eccezioni alla Legge di Proust. Si tratta dei cosiddetti composti non stechiometrici, in cui il rapporto tra gli elementi non è esattamente un numero intero. Questi composti, spesso presenti in minerali o semiconduttori, presentano difetti nella loro struttura cristallina che permettono una leggera variazione nella composizione. Tuttavia, la Legge di Proust rimane una regola generale valida per la maggior parte dei composti chimici.

Curiosità Storica: La Battaglia con Berthollet
La formulazione della Legge di Proust non fu priva di controversie. Proust dovette affrontare una lunga e accesa disputa con il chimico francese Claude Louis Berthollet, che sosteneva che la composizione dei composti potesse variare in un intervallo continuo. La vittoria di Proust in questa battaglia scientifica segnò un momento cruciale nella storia della chimica e contribuì a consolidare le basi della chimica moderna.
Come Insegnare la Legge di Proust in Modo Efficace
Per rendere l'insegnamento della Legge di Proust più efficace, è importante adottare un approccio pratico e coinvolgente.
- Utilizzare esempi concreti: Come abbiamo visto, gli esempi della torta, dell'ossido di magnesio e del solfato di rame sono molto efficaci per illustrare il concetto.
- Sperimentare in laboratorio: Coinvolgere gli studenti in esperimenti pratici è fondamentale per far loro comprendere la legge in modo tangibile.
- Utilizzare analogie: Paragonare la legge a concetti familiari, come le ricette di cucina, può rendere il concetto più accessibile.
- Promuovere la discussione: Incoraggiare gli studenti a porre domande e a discutere le implicazioni della legge può favorire una comprensione più profonda.
Ricordate, la chimica può sembrare complessa, ma con un approccio graduale e l'utilizzo di esempi concreti, anche concetti apparentemente difficili come la Legge di Proust possono diventare comprensibili e persino affascinanti.
In sintesi: La Legge di Proust è una legge fondamentale della chimica che afferma che un composto chimico è sempre formato dagli stessi elementi, combinati nello stesso rapporto di peso. Comprendere questa legge è essenziale per capire la composizione dei composti e per lo sviluppo di nuove tecniche di analisi chimica. Attraverso esperimenti pratici e esempi concreti, è possibile rendere questo concetto accessibile e interessante per studenti di ogni livello.