Ammettiamolo, la tavola periodica può sembrare un labirinto di simboli e numeri, soprattutto quando ci si avvicina per la prima volta. Genitori, insegnanti e soprattutto studenti, si trovano spesso a lottare per comprendere i suoi segreti. Quante volte vi siete chiesti: "Cosa significano veramente questi gruppi e periodi? E perché sono così importanti?" Non siete soli! Molti studenti, secondo diverse ricerche, trovano la tavola periodica un argomento ostico, legato a concetti astratti e difficili da visualizzare. Ma non temete, perché oggi vi guiderò attraverso questo affascinante mondo in modo chiaro, semplice e, spero, anche divertente.
Immaginate la tavola periodica come una grande mappa del tesoro, dove ogni elemento chimico è una gemma preziosa con le sue proprietà uniche. Per trovare il tesoro, però, bisogna saper leggere la mappa! E la chiave per leggere questa mappa sono proprio i gruppi e i periodi.
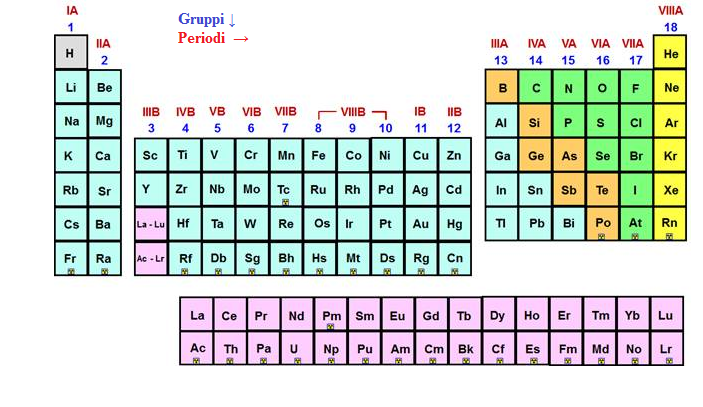
Gruppi: Famiglie Chimiche con Proprietà Simili
Un gruppo nella tavola periodica è una colonna verticale di elementi. Gli elementi all'interno dello stesso gruppo condividono proprietà chimiche simili perché hanno lo stesso numero di elettroni nel loro guscio di valenza, ovvero il guscio più esterno. Questi elettroni sono cruciali perché determinano come un atomo interagisce con altri atomi, formando legami chimici.
Pensate ai gruppi come a delle famiglie: i membri di una famiglia, pur essendo individui diversi, condividono spesso tratti somatici e caratteristiche comportamentali. Allo stesso modo, gli elementi di un gruppo hanno reattività e comportamenti simili.
Esempi di Gruppi Importanti:
- Metalli Alcalini (Gruppo 1): Litio (Li), Sodio (Na), Potassio (K), Rubidio (Rb), Cesio (Cs), Francio (Fr). Sono metalli molto reattivi, tanto che non si trovano mai in natura allo stato puro, ma sempre combinati con altri elementi. Reagiscono violentemente con l'acqua, formando idrogeno e idrossido. Un esempio pratico? Il sodio metallico (Na) immerso in acqua crea una reazione esplosiva.
- Metalli Alcalino-Terrosi (Gruppo 2): Berillio (Be), Magnesio (Mg), Calcio (Ca), Stronzio (Sr), Bario (Ba), Radio (Ra). Meno reattivi dei metalli alcalini, ma comunque reattivi. Il magnesio (Mg) è fondamentale per la fotosintesi clorofilliana nelle piante. Il calcio (Ca) è essenziale per la formazione delle ossa e dei denti.
- Alogeni (Gruppo 17): Fluoro (F), Cloro (Cl), Bromo (Br), Iodio (I), Astato (At). Sono non metalli molto reattivi. Il cloro (Cl) è usato come disinfettante in piscine e nell'acqua potabile. Il fluoro (F) è aggiunto al dentifricio per prevenire la carie.
- Gas Nobili (Gruppo 18): Elio (He), Neon (Ne), Argon (Ar), Kripton (Kr), Xenon (Xe), Radon (Rn). Sono gas inerti, ovvero estremamente poco reattivi. Questo perché hanno il guscio di valenza completamente pieno, il che li rende molto stabili. L'elio (He) è usato nei palloni aerostatici. Il neon (Ne) è usato nelle insegne luminose.
Come ricordare i gruppi? Usate delle filastrocche o delle associazioni mentali. Ad esempio: "Napoli, Kalma, Rboma, Csenza, Frignano" per ricordare i metalli alcalini.

Periodi: Livelli Energetici e Aumento delle Proprietà
Un periodo nella tavola periodica è una riga orizzontale di elementi. Gli elementi in un periodo hanno lo stesso numero di gusci elettronici occupati. Man mano che ci si sposta da sinistra a destra lungo un periodo, il numero atomico (ovvero il numero di protoni nel nucleo) aumenta, e quindi anche il numero di elettroni.
Le proprietà degli elementi variano in modo sistematico lungo un periodo. In generale, si osserva un passaggio graduale dalle proprietà metalliche a sinistra, a quelle non metalliche a destra. L'elettronegatività (la capacità di un atomo di attrarre elettroni) aumenta da sinistra a destra, mentre il raggio atomico diminuisce (inizialmente). L'energia di ionizzazione (l'energia necessaria per rimuovere un elettrone) aumenta anch'essa da sinistra a destra.

Esempi di Variazioni nei Periodi:
Prendiamo ad esempio il terzo periodo: Sodio (Na), Magnesio (Mg), Alluminio (Al), Silicio (Si), Fosforo (P), Zolfo (S), Cloro (Cl), Argon (Ar).
- Il sodio (Na) è un metallo molto reattivo.
- Il magnesio (Mg) è meno reattivo del sodio, ma comunque un metallo.
- L'alluminio (Al) è un metallo con proprietà sia metalliche che non metalliche (anfotero).
- Il silicio (Si) è un metalloide, con proprietà intermedie tra metalli e non metalli. È un semiconduttore molto importante nell'elettronica.
- Il fosforo (P) e lo zolfo (S) sono non metalli.
- Il cloro (Cl) è un non metallo molto reattivo.
- L'argon (Ar) è un gas nobile, estremamente inerte.
Notate come, spostandosi da sinistra a destra, si passa gradualmente da un comportamento metallico a un comportamento non metallico. Questo cambiamento è legato all'aumento della carica nucleare effettiva, che attrae sempre più gli elettroni.

Come sfruttare questo in classe o a casa:
Per rendere lo studio più interattivo, potete creare una tavola periodica "vivente". Assegnate a ogni studente un elemento e chiedetegli di preparare una breve presentazione sulle sue proprietà, usi e curiosità. Poi, disponeteli in ordine, seguendo la tavola periodica, per visualizzare concretamente i gruppi e i periodi.
Un'altra attività utile è la "caccia all'elemento". Date agli studenti degli indizi sulle proprietà di un elemento e chiedetegli di individuarlo nella tavola periodica. Questo li aiuta a mettere in pratica le conoscenze acquisite e a sviluppare il pensiero critico.

Consigli Pratici per l'Apprendimento
- Non abbiate paura di semplificare: Iniziate concentrandovi sui gruppi e i periodi principali (1, 2, 17, 18) e poi approfondite gradualmente gli altri.
- Usate risorse visive: Schemi, diagrammi e video possono rendere i concetti più chiari e memorizzabili.
- Fate pratica: Risolvete esercizi e quiz per mettere alla prova le vostre conoscenze.
- Connettete la teoria alla pratica: Cercate esempi concreti di come gli elementi chimici vengono utilizzati nella vita di tutti i giorni. Ad esempio, il litio nelle batterie, il silicio nei computer, il calcio nel latte.
- Siate curiosi: La chimica è ovunque intorno a noi. Cercate di capire come funziona il mondo a livello atomico e molecolare.
Secondo alcuni studi, l'apprendimento basato sull'esperienza (experiential learning) aumenta significativamente la memorizzazione e la comprensione dei concetti scientifici. Quindi, non limitatevi a leggere libri di testo, ma cercate di sperimentare, osservare e toccare con mano (ovviamente, in modo sicuro e supervisionato!).
La tavola periodica non è solo un elenco di elementi, ma una mappa che svela i segreti della materia. Comprendere i gruppi e i periodi è il primo passo per decifrare questa mappa e aprire le porte a un mondo di scoperte affascinanti. Non scoraggiatevi di fronte alle difficoltà, ma affrontate questo percorso con curiosità e impegno. E ricordate, la chimica è dappertutto! Quindi, iniziate a osservare il mondo che vi circonda con occhi nuovi.
Spero che questa guida vi sia stata utile. In bocca al lupo per il vostro viaggio nel mondo della chimica!