+calcola+la+quantità+di+anidride+carbonica+prodotta+dalla+reazione+tra+1%2C000Kg+di+metano+e+1%2C000Kg+di+ossigeno.jpg)
Ti sei mai trovato a cucinare una ricetta, convinto di avere tutti gli ingredienti, per poi scoprire che te ne manca uno cruciale? Magari hai abbastanza farina e uova per una torta, ma sei a corto di cioccolato. Il risultato? Non otterrai la torta che avevi in mente, perché la quantità di cioccolato limita il risultato finale. In chimica, questo concetto si chiama reagente limitante ed è fondamentale per capire come le reazioni avvengono realmente.
Molti studenti si bloccano di fronte agli esercizi sul reagente limitante e in eccesso. Sembrano complessi, pieni di numeri e calcoli strani. Ma non disperare! Questo articolo è pensato proprio per te, per spiegarti in modo chiaro e pratico come affrontare questi esercizi, partendo dalle basi e arrivando a esempi concreti.
Capire i Concetti Chiave
Prima di lanciarci negli esercizi, è cruciale comprendere i concetti fondamentali:
- Reagente Limitante: È il reagente che si consuma per primo in una reazione chimica. La quantità di prodotto che si forma dipende esclusivamente dalla quantità di reagente limitante presente. Una volta esaurito, la reazione si ferma, anche se gli altri reagenti sono ancora presenti.
- Reagente in Eccesso: È il reagente presente in quantità superiore rispetto a quella necessaria per reagire completamente con il reagente limitante. Una parte di questo reagente rimarrà intatta alla fine della reazione.
- Stechiometria: È lo studio delle relazioni quantitative tra i reagenti e i prodotti in una reazione chimica. Si basa sulla legge di conservazione della massa e utilizza i coefficienti stechiometrici dell'equazione chimica bilanciata per determinare le quantità relative delle sostanze coinvolte.
Immagina di costruire delle biciclette. Per ogni bicicletta, hai bisogno di 2 ruote e 1 telaio. Se hai 10 ruote e 3 telai, quante biciclette complete puoi costruire? Solo 3, perché i telai sono il "reagente limitante". Ti avanzerebbero 4 ruote, che sono il "reagente in eccesso".
Come Identificare il Reagente Limitante
Ecco il metodo passo-passo per identificare il reagente limitante:
- Scrivi e bilancia l'equazione chimica: Questo è il punto di partenza. Senza un'equazione bilanciata, i calcoli saranno errati. Assicurati che il numero di atomi di ciascun elemento sia lo stesso su entrambi i lati della freccia.
- Converti le masse in moli: Generalmente, negli esercizi ti vengono fornite le masse dei reagenti in grammi. Devi convertirle in moli usando la massa molare di ciascun reagente (che puoi trovare sulla tavola periodica). La formula è: moli = massa (g) / massa molare (g/mol)
- Calcola il rapporto molare: Dividi il numero di moli di ciascun reagente per il suo coefficiente stechiometrico nell'equazione bilanciata.
- Identifica il reagente limitante: Il reagente con il rapporto molare più piccolo è il reagente limitante.
Esempio:
Considera la reazione tra azoto (N₂) e idrogeno (H₂) per formare ammoniaca (NH₃):
N₂(g) + 3H₂(g) → 2NH₃(g)
Supponiamo di avere 28 g di N₂ e 6 g di H₂. Qual è il reagente limitante?
- L'equazione è già bilanciata.
- Calcoliamo le moli:
- Moli di N₂ = 28 g / 28 g/mol = 1 mole
- Moli di H₂ = 6 g / 2 g/mol = 3 moli
- Calcoliamo il rapporto molare:
- N₂: 1 mole / 1 = 1
- H₂: 3 moli / 3 = 1
- In questo caso, i rapporti molari sono uguali. Questo significa che entrambi i reagenti si consumano completamente contemporaneamente. Non c'è un reagente limitante o in eccesso in senso stretto. Le quantità sono stechiometriche.
Se avessimo avuto, ad esempio, 4 g di H₂, le moli di H₂ sarebbero state 4 g / 2 g/mol = 2 moli. Il rapporto molare per H₂ sarebbe stato 2 moli / 3 = 0.67. In questo caso, H₂ sarebbe stato il reagente limitante perché ha il rapporto molare più basso.
Esercizi Pratici
Ora, proviamo a risolvere alcuni esercizi per consolidare la tua comprensione:
Esercizio 1:
Data la seguente reazione:
2Al(s) + 3Cl₂(g) → 2AlCl₃(s)

Se si fanno reagire 5.4 g di alluminio (Al) con 10.65 g di cloro (Cl₂), qual è il reagente limitante e quanti grammi di cloruro di alluminio (AlCl₃) si formano?
Soluzione:
- L'equazione è già bilanciata.
- Calcola le moli:
- Moli di Al = 5.4 g / 27 g/mol = 0.2 moli
- Moli di Cl₂ = 10.65 g / 71 g/mol = 0.15 moli
- Calcola il rapporto molare:
- Al: 0.2 moli / 2 = 0.1
- Cl₂: 0.15 moli / 3 = 0.05
- Cl₂ è il reagente limitante perché ha il rapporto molare più basso.
Ora, calcoliamo quanti grammi di AlCl₃ si formano. Poiché Cl₂ è il reagente limitante, useremo le sue moli per il calcolo. Secondo l'equazione bilanciata, 3 moli di Cl₂ producono 2 moli di AlCl₃. Quindi, 0.15 moli di Cl₂ produrranno (2/3) * 0.15 = 0.1 moli di AlCl₃.
La massa molare di AlCl₃ è 27 + (3 * 35.5) = 133.5 g/mol.
Massa di AlCl₃ = 0.1 moli * 133.5 g/mol = 13.35 g

Quindi, si formano 13.35 g di cloruro di alluminio.
Esercizio 2:
Data la seguente reazione:
CuO(s) + H₂(g) → Cu(s) + H₂O(g)
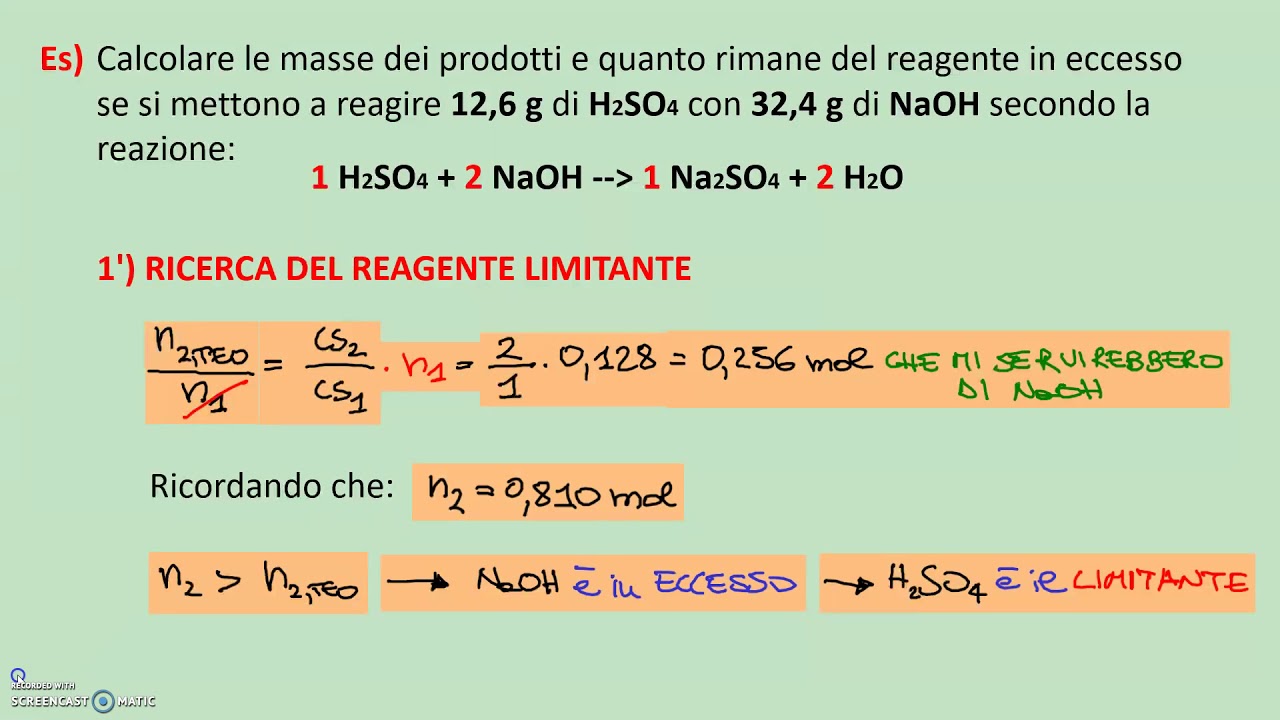
Se si fanno reagire 7.95 g di ossido di rame(II) (CuO) con 2 g di idrogeno (H₂), qual è il reagente limitante e quanti grammi di rame (Cu) si formano?
Soluzione:
- L'equazione è già bilanciata.
- Calcola le moli:
- Moli di CuO = 7.95 g / 79.5 g/mol = 0.1 moli
- Moli di H₂ = 2 g / 2 g/mol = 1 mole
- Calcola il rapporto molare:
- CuO: 0.1 moli / 1 = 0.1
- H₂: 1 mole / 1 = 1
- CuO è il reagente limitante perché ha il rapporto molare più basso.
Ora, calcoliamo quanti grammi di Cu si formano. Poiché CuO è il reagente limitante, useremo le sue moli per il calcolo. Secondo l'equazione bilanciata, 1 mole di CuO produce 1 mole di Cu. Quindi, 0.1 moli di CuO produrranno 0.1 moli di Cu.
La massa molare di Cu è 63.5 g/mol.
Massa di Cu = 0.1 moli * 63.5 g/mol = 6.35 g
Quindi, si formano 6.35 g di rame.
Trucchi e Consigli
- Controlla sempre l'equazione bilanciata: Un errore nell'equazione bilanciata invalida tutti i calcoli successivi.
- Sii preciso con le unità di misura: Assicurati di usare le unità di misura corrette (g/mol per la massa molare, grammi per la massa, ecc.).
- Scrivi tutti i passaggi: Scrivere tutti i passaggi ti aiuta a evitare errori e a tenere traccia dei tuoi calcoli. Inoltre, facilita la revisione del problema.
- Esercitati regolarmente: La pratica rende perfetti! Più esercizi fai, più diventerai bravo a identificare il reagente limitante e a risolvere problemi stechiometrici.
- Non aver paura di chiedere aiuto: Se ti blocchi, chiedi aiuto al tuo insegnante, ai tuoi compagni di classe o cerca risorse online.
Conclusione
Comprendere il concetto di reagente limitante è essenziale per padroneggiare la stechiometria e risolvere problemi di chimica. Seguendo i passaggi descritti in questo articolo e facendo pratica con gli esercizi, sarai in grado di affrontare con sicurezza qualsiasi problema ti venga proposto. Ricorda, la chiave è la pratica costante e la comprensione dei concetti fondamentali. Non arrenderti di fronte alle difficoltà e continua a esercitarti. Buono studio!