
I metalli costituiscono una parte preponderante degli elementi presenti nella tavola periodica, distinguendosi per proprietà fisiche e chimiche peculiari. La loro localizzazione all'interno della tavola periodica non è casuale, ma riflette la loro configurazione elettronica e, di conseguenza, il loro comportamento chimico.
Dove Si Trovano i Metalli?
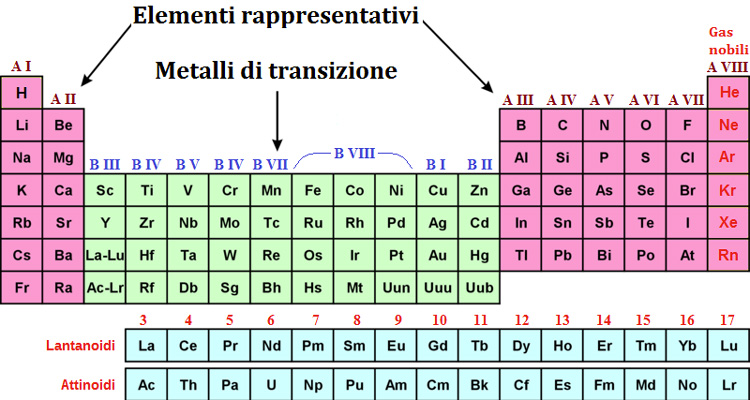
La maggior parte degli elementi della tavola periodica sono metalli. Generalmente, si trovano sul lato sinistro e al centro della tavola. Una linea diagonale, che si snoda dal boro (B) al polonio (Po), separa grosso modo i metalli dai non metalli. Gli elementi che si trovano vicino a questa linea sono spesso chiamati metalloidi o semimetalli, poiché possiedono proprietà intermedie tra i metalli e i non metalli.
Metalli Alcalini e Alcalino-Terrosi
Nel gruppo 1 (escluso l'idrogeno) si trovano i metalli alcalini (litio, sodio, potassio, rubidio, cesio e francio). Questi metalli sono estremamente reattivi e si combinano facilmente con altri elementi. Nel gruppo 2 si trovano i metalli alcalino-terrosi (berillio, magnesio, calcio, stronzio, bario e radio), anch'essi reattivi, ma meno dei metalli alcalini.
Metalli di Transizione
I metalli di transizione occupano la parte centrale della tavola periodica, nei gruppi dal 3 al 12. Sono caratterizzati dalla capacità di formare diversi stati di ossidazione e composti colorati. Esempi comuni includono ferro, rame, oro e argento. La loro importanza è fondamentale in molti processi industriali e biologici.
Altri Metalli
Dopo i metalli di transizione, troviamo altri metalli, spesso chiamati metalli del blocco p o post-transizionali. Questi includono alluminio, gallio, indio, stagno, tallio, piombo e bismuto. Hanno proprietà intermedie tra i metalli di transizione e i non metalli.
Perché È Importante Conoscerli?
Comprendere la posizione dei metalli nella tavola periodica e le loro proprietà è cruciale per gli studenti per diversi motivi:
- Prevedere il Comportamento Chimico: La posizione di un elemento nella tavola periodica fornisce indizi importanti sulla sua reattività e sulla sua tendenza a formare legami chimici.
- Comprendere le Proprietà dei Materiali: Molte delle proprietà dei materiali che utilizziamo quotidianamente dipendono dalla presenza e dalle caratteristiche dei metalli.
- Studiare le Reazioni Chimiche: La conoscenza delle proprietà dei metalli è essenziale per comprendere e prevedere il risultato delle reazioni chimiche.
Applicazioni Pratiche nella Scuola e nella Vita Quotidiana
La conoscenza dei metalli e della tavola periodica trova applicazioni pratiche sia in ambito scolastico che nella vita quotidiana degli studenti.

- Laboratorio di Chimica: Durante gli esperimenti di laboratorio, gli studenti utilizzano metalli e composti metallici per osservare le reazioni chimiche e studiare le loro proprietà.
- Tecnologia: I dispositivi elettronici, come smartphone e computer, contengono numerosi metalli, tra cui rame, oro e argento.
- Ambiente: La conoscenza dei metalli è importante per comprendere l'inquinamento ambientale causato dai metalli pesanti e per sviluppare strategie di bonifica.
- Salute: Alcuni metalli, come il ferro e il calcio, sono essenziali per la salute umana.
Come affermato da Linus Pauling, premio Nobel per la chimica, "La tavola periodica è una guida essenziale per comprendere la chimica e le proprietà degli elementi."
In conclusione, la localizzazione dei metalli nella tavola periodica non è solo un elemento di conoscenza teorica, ma una base fondamentale per comprendere il mondo che ci circonda e le sue molteplici applicazioni pratiche. Un solido fondamento in questo ambito permette agli studenti di affrontare con maggiore consapevolezza e successo le sfide del mondo scientifico e tecnologico.