Vi ricordate quella volta che provammo a fare la torta della nonna, ma ci siamo persi a metà strada? Eravamo lì, con la farina sparsa ovunque, le uova che rischiavano di rotolare giù dal tavolo, e il ricettario che sembrava scritto in geroglifici. Beh, la chimica a volte mi ricorda proprio quel momento. Soprattutto quando si parla di titolazioni, e in particolare della titolazione di un acido debole con una base forte. Sembra una roba da scienziati pazzi, vero? Ma fidatevi, una volta capito il meccanismo, è meno complicato di quanto sembri. Anzi, è quasi... affascinante.
Pensateci un attimo: stiamo mescolando due cose diverse, un acido che non è proprio "aggressivo" (il nostro acido debole) e una base che invece è una vera forza della natura (la nostra base forte). E vogliamo capire quanta di questa "forza" ci serve per neutralizzare perfettamente la "debolezza" dell'acido. È un po' come cercare il punto esatto in cui la dolcezza della torta incontra l'acidità giusta del limone, senza che una prenda il sopravvento sull'altra. Capito il parallelo? Spero di sì, perché questo è il cuore della questione!
Il Dottor Jekyll e Mr. Hyde della Chimica
Allora, mettiamoci comodi e parliamo un po' di questi protagonisti. Da una parte abbiamo l'acido debole. Pensate all'acido acetico, quello dell'aceto. Non è che vi corrode la mano, giusto? Si scioglie in acqua, ma non si rompe completamente in ioni H+. Diciamo che è un po' timido, si tiene strette le sue molecole. Rappresenta una parte di sé, un po' come il tranquillo Dottor Jekyll. Solo una piccola parte si trasforma in ioni H+ pronti all'azione. La maggior parte rimane come tale, in attesa.
Dall'altra parte, ecco la base forte. Qui siamo nel regno di Mr. Hyde. Una base forte, come l'idrossido di sodio (NaOH), è esplosiva! Quando la metti in acqua, si divide subito in ioni Na+ e ioni OH-. E sono proprio questi ioni OH- a creare scompiglio, a cercare subito qualcosa con cui reagire. Sono molto reattivi, desiderosi di trovare un acido con cui fare pace. Non hanno esitazioni, si scindono completamente.
E cosa succede quando mettiamo insieme il timido Jekyll e il focoso Hyde? Una reazione! L'OH- (Mr. Hyde) è subito attratto dall'H+ (la parte "coraggiosa" di Jekyll). Si incontrano, si abbracciano stretti stretti e formano acqua (H2O). In questa reazione, l'acido debole viene neutralizzato, piano piano.
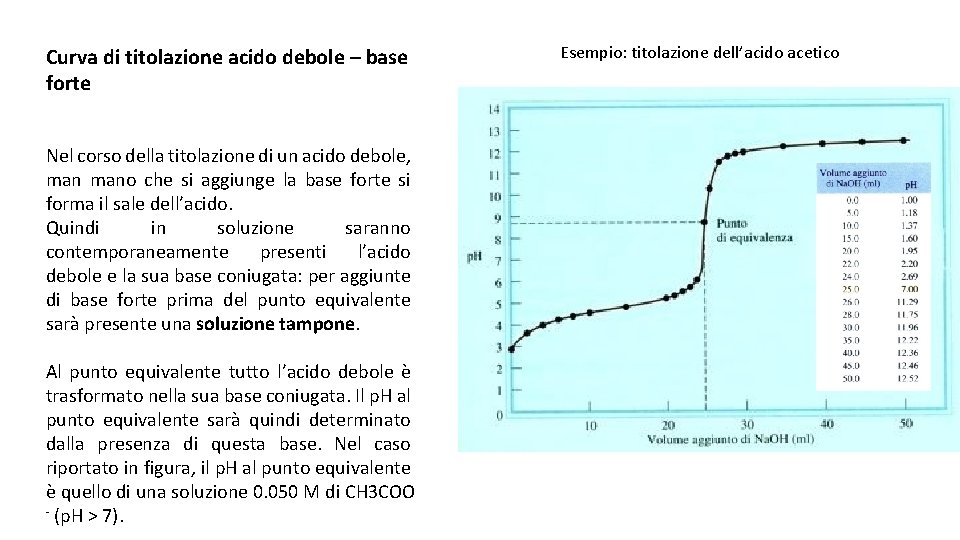
Ma non è una neutralizzazione banale. Qui sta il bello, e a volte il "terrore" del chimico alle prime armi. La curva di titolazione è la nostra mappa del tesoro che ci mostra cosa succede passo dopo passo.
La Trama della Curva: un Viaggio Emotivo (dei pH)
Immaginate una linea tracciata su un grafico. Sull'asse delle ascisse (quello orizzontale), mettiamo il volume di base forte aggiunto. Sull'asse delle ordinate (quello verticale), invece, abbiamo il pH. Il pH, quel numero che ci dice quanto è acido o basico una soluzione. Un pH basso vuol dire acido forte, un pH alto vuol dire base forte, e 7 è la neutralità, dove tutto è in perfetto equilibrio. O quasi.

Iniziamo! All'inizio, nel nostro becher, abbiamo solo il nostro acido debole. Il pH sarà basso, perché è acido, ma non altissimo, perché è debole. Ci aspettiamo un valore, diciamo, intorno a 3 o 4. La maggior parte delle molecole di acido debole sono intatte, solo una piccola percentuale si è dissociata rilasciando H+.
Ora iniziamo ad aggiungere goccia a goccia la base forte. Ogni goccia che cade porta con sé i suoi potentissimi ioni OH-. Cosa fanno questi ioni? Attaccano immediatamente gli ioni H+ rilasciati dall'acido debole. È una battaglia, ma una battaglia che favorisce la base. L'acido debole, vedendo sparire i suoi H+, è costretto a dissociarsi ancora di più per cercare di mantenere una certa concentrazione di H+. È come se, per compensare la perdita, dicesse: "Ok, mi arrendo un po' e mi dissocio di più per ripristinare un minimo di H+!".
E qui arriva la prima sorpresa, il primo tratto "strano" della nostra curva. Il pH non sale vertiginosamente. Sale, certo, ma con una certa... lentiggine. Perché? Perché ogni volta che aggiungiamo una molecola di base forte (che porta un OH-), questa reagisce con un H+ proveniente dall'acido debole. Ma il vero "trucco" è che l'acido debole si sta trasformando in qualcos'altro: la sua base coniugata. L'acido HA, perdendo un H+, diventa A-. E questo A- insieme all'acido non dissociato HA, forma una soluzione tampone.
La Magia della Soluzione Tampone
Ah, la soluzione tampone! Sentite che parola importante? Una soluzione tampone è come uno scudo. Ha la capacità di resistere ai cambiamenti di pH quando vengono aggiunti piccole quantità di acido o base. Pensateci, nel nostro caso, l'acido debole HA e la sua base coniugata A- lavorano insieme. Se aggiungiamo ancora un po' di base forte (OH-), l'A- reagisce con esso per formare HA e acqua. Se, per assurdo, aggiungessimo un po' di acido, l'HA reagirebbe con esso. È un meccanismo di difesa incredibile!
Quindi, mentre siamo nel pieno della "zona tampone", il pH cambia molto lentamente. Aggiungiamo base forte, ma la soluzione tampone "assorbe" l'urto. La curva qui è quasi piatta, con una pendenza molto dolce. È la parte più "calma" del nostro viaggio, ma è anche quella dove si nasconde la magia chimica.

E poi c'è quel punto, quel momento magico, chiamato punto di semiequivalenza. Avete presente quando siete a metà di una ricetta e sentite che le cose stanno prendendo la giusta piega? Ecco, il punto di semiequivalenza è proprio quello. Succede quando abbiamo aggiunto esattamente la metà della base forte necessaria per neutralizzare tutto l'acido debole.
Cosa succede qui? La concentrazione dell'acido debole (HA) è uguale alla concentrazione della sua base coniugata (A-). E questo, amici miei, significa che il pH in quel punto è esattamente uguale al pKa dell'acido debole. Il pKa è una proprietà intrinseca dell'acido debole, che ci dice quanto è forte o debole. Se il pKa è basso, l'acido è più forte (anche se sempre debole rispetto a un acido forte). Se il pKa è alto, è ancora più debole. Trovando questo punto sulla curva, possiamo addirittura stimare il pKa del nostro acido! Non è pazzesco? È come trovare la "personalità" esatta del nostro acido guardando come si comporta durante una "litigata" controllata.
Il Salto Finale: Il Punto di Equivalenza
Dopo il punto di semiequivalenza, continuiamo ad aggiungere la base forte. La concentrazione dell'acido debole diminuisce sempre di più, e quella della sua base coniugata aumenta. La soluzione tampone si sta esaurendo. La "difesa" del nostro acido si sta indebolendo.
E poi, BAM! Arriva il punto di equivalenza. Questo è il momento in cui abbiamo aggiunto esattamente la quantità stechiometrica di base forte necessaria per reagire con tutto l'acido debole. Tutta la forma HA si è trasformata in A-.
Qui succede una cosa fondamentale: non c'è più acido debole HA presente in quantità significative. E non c'è più base forte OH- in eccesso (perché l'abbiamo aggiunta solo fino all'equivalenza). Cosa rimane nella soluzione? Principalmente la base coniugata (A-) e gli ioni provenienti dalla base forte (come Na+).

E ora, la sorpresa numero uno per molti: il pH al punto di equivalenza NON è 7! Se fosse stata la titolazione di un acido forte con una base forte, il pH sarebbe stato 7 (o molto vicino). Ma qui abbiamo un acido debole e una base forte. La base coniugata (A-) è, per definizione, una base debole. E le basi deboli, quando sono in acqua, tendono a reagire con l'acqua stessa (idrolisi) per produrre ioni OH-.
Quindi, al punto di equivalenza, la nostra soluzione contiene principalmente la base coniugata A-, che si comporta come una base debole. Di conseguenza, il pH sarà maggiore di 7. La curva, che prima era quasi piatta, ora fa un salto brusco verso l'alto. Questo è il tratto più ripido della curva, dove il pH cambia molto rapidamente anche per l'aggiunta di piccolissime quantità di base forte.
Il punto di equivalenza si identifica graficamente proprio in questo salto verticale. È il centro del "gomito" della curva.
Dopo il Salto: Quando la Base Forte Prende il Sopravvento
E dopo il punto di equivalenza? Continuiamo ad aggiungere base forte. Ora nella soluzione c'è la base coniugata A- (che è già una base debole) e un eccesso di ioni OH- che provengono dalla base forte che stiamo aggiungendo.
A questo punto, la concentrazione di ioni OH- che stiamo aggiungendo supera di gran lunga quelli prodotti dall'idrolisi della base coniugata A-. La soluzione diventa decisamente basica. Il pH continua a salire, ma questa volta la curva diventa molto più piatta, molto simile a quella che si otterrebbe titolando acqua con una base forte. Perché? Perché la maggior parte del contributo al pH ora proviene dall'eccesso di base forte, e la sua concentrazione cambia in modo più lineare con l'aggiunta.
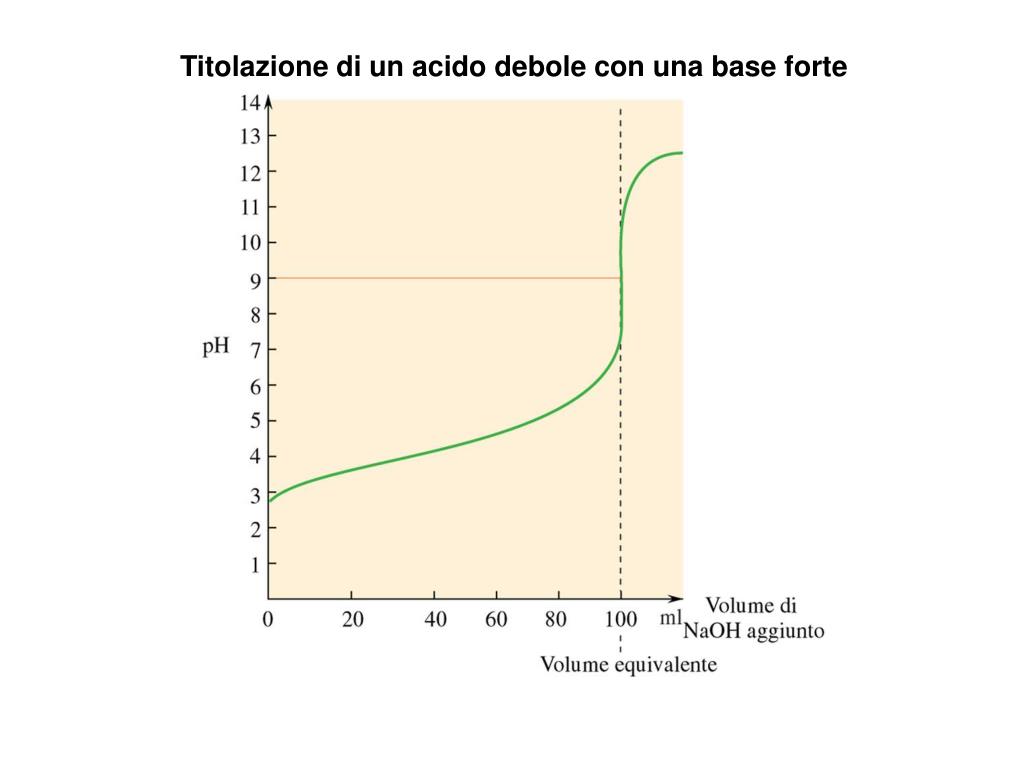
Pensateci: all'inizio, il pH era dettato dall'acido debole. Poi, nella zona tampone, era una lotta tra acido e base coniugata. Al punto di equivalenza, era il pH della base coniugata. Dopo il punto di equivalenza, è il pH dettato dalla base forte in eccesso.
E questo è il quadro completo! La curva di titolazione di un acido debole con una base forte ci racconta una storia affascinante: una storia di equilibri, di trasformazioni, di difese (la soluzione tampone) e di un punto di svolta cruciale.
Perché È Importante Capire Questa Curva?
Ok, ok, lo so. Sembra tutto molto teorico. Ma questo è uno strumento fondamentale in chimica!
- Identificazione dell'acido debole: Come abbiamo detto, dal punto di semiequivalenza possiamo risalire al pKa dell'acido. Questo ci aiuta a capire di che acido si tratta, dato che ogni acido debole ha un pKa caratteristico.
- Determinazione della concentrazione: Il punto di equivalenza ci dice esattamente quanta base forte ci serve per neutralizzare una data quantità di acido debole. Sapendo la concentrazione della base forte, possiamo calcolare la concentrazione dell'acido debole iniziale. È un metodo di analisi quantitativa super preciso.
- Scelta dell'indicatore: Gli indicatori acido-base cambiano colore in un certo intervallo di pH. Per fare una titolazione efficace, dobbiamo scegliere un indicatore che cambi colore proprio intorno al pH del punto di equivalenza. Nel caso di un acido debole/base forte, dove il pH al punto di equivalenza è maggiore di 7, sceglieremo indicatori come la fenolftaleina (che cambia colore in un intervallo di pH 8.2-10). Se scegliessimo un indicatore che cambia colore a pH 3, sarebbe un disastro! Non vedremmo il vero punto di equivalenza.
Insomma, questa curva è molto più di un semplice disegno su un foglio. È una roadmap che ci guida attraverso una reazione chimica complessa, rivelando i segreti nascosti nei cambiamenti di pH.
La prossima volta che vedrete una curva del genere, spero non vi sembrerà più un mostro incomprensibile. Pensate alla storia del Dottor Jekyll e Mr. Hyde, al viaggio delle emozioni del pH, alla magia della soluzione tampone e al salto finale verso la basicità. È un piccolo mondo chimico racchiuso in un grafico, pronto per essere scoperto. E voi, con un po' di pratica, sarete dei veri esploratori!