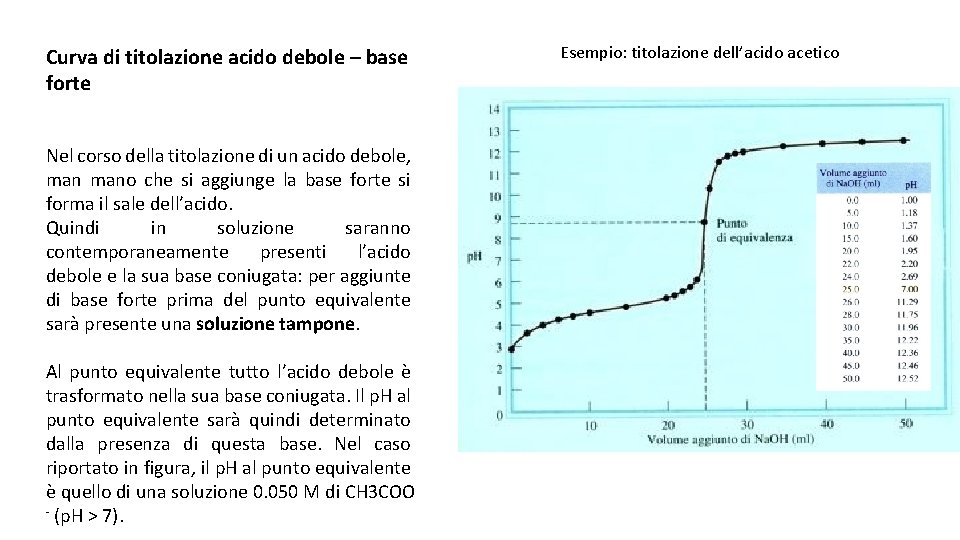
La titolazione, o titrimetria, è una tecnica analitica quantitativa fondamentale in chimica. Essa permette di determinare la concentrazione di una soluzione (l'analita) facendola reagire con una soluzione a concentrazione nota (il titolante). La curva di titolazione è la rappresentazione grafica del pH della soluzione durante l'aggiunta progressiva del titolante, e fornisce informazioni cruciali sulla reazione che avviene. Questo articolo si concentrerà in particolare sulla curva di titolazione di un acido debole con una base forte, analizzandone le caratteristiche distintive e fornendo esempi concreti.
Punti Chiave di una Titolazione Acido Debole - Base Forte
Equilibrio di Dissociazione dell'Acido Debole
A differenza degli acidi forti, che si dissociano completamente in soluzione acquosa, gli acidi deboli si dissociano solo parzialmente. Questo è governato da una costante di dissociazione acida, Ka, che esprime l'equilibrio tra l'acido indissociato (HA) e i suoi prodotti di dissociazione, lo ione idronio (H3O+) e la base coniugata (A-):
HA + H2O ⇌ H3O+ + A-
Ka = [H3O+][A-] / [HA]
Un Ka piccolo indica che l'acido è debole e che la dissociazione è limitata. Questo equilibrio è fondamentale per comprendere il comportamento della curva di titolazione.
La Regione Tampone
La regione tampone è una zona cruciale della curva di titolazione di un acido debole con una base forte. Si verifica prima del punto di equivalenza ed è caratterizzata da una resistenza al cambiamento di pH quando si aggiunge una piccola quantità di acido o base. Questo fenomeno si verifica perché in questa regione, la soluzione contiene quantità apprezzabili sia dell'acido debole (HA) che della sua base coniugata (A-). La relazione che descrive il pH in questa regione è l'equazione di Henderson-Hasselbalch:
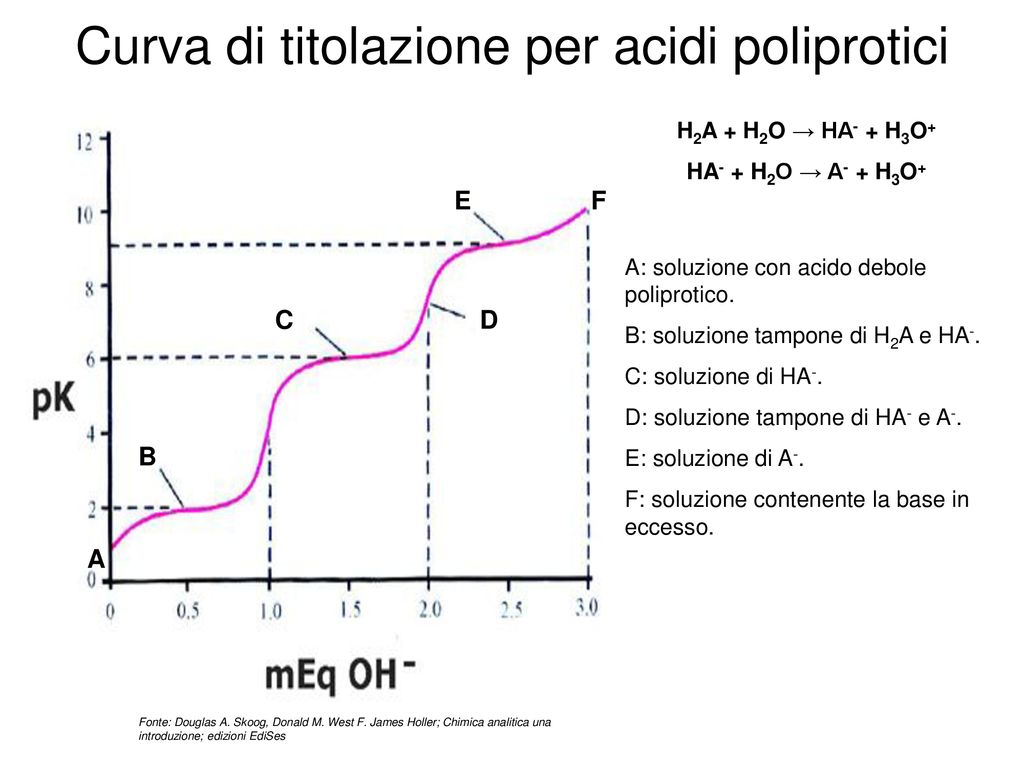
pH = pKa + log ([A-] / [HA])
Dove pKa è il logaritmo negativo di Ka. Quando [A-] = [HA], pH = pKa. Questo punto è spesso indicato come il punto di semi-equivalenza.
Il Punto di Equivalenza
Il punto di equivalenza è il punto in cui la quantità di base forte aggiunta è stechiometricamente equivalente alla quantità di acido debole inizialmente presente. In altre parole, tutta l'acido debole HA è stato neutralizzato e convertito nella sua base coniugata A-. A differenza delle titolazioni acido forte-base forte, il pH al punto di equivalenza non è neutro (pH = 7). Questo perché la base coniugata A- reagisce con l'acqua (idrolisi), producendo ioni idrossido (OH-) e aumentando il pH:
A- + H2O ⇌ HA + OH-

Pertanto, il pH al punto di equivalenza sarà superiore a 7.
Dopo il Punto di Equivalenza
Dopo il punto di equivalenza, l'aggiunta di ulteriore base forte provoca un rapido aumento del pH. La soluzione contiene principalmente la base forte in eccesso, che determina il pH. La curva di titolazione si appiattisce gradualmente man mano che il pH si avvicina al pH della soluzione di base forte utilizzata.
Caratteristiche Distintive della Curva
Inizio Graduale della Curva
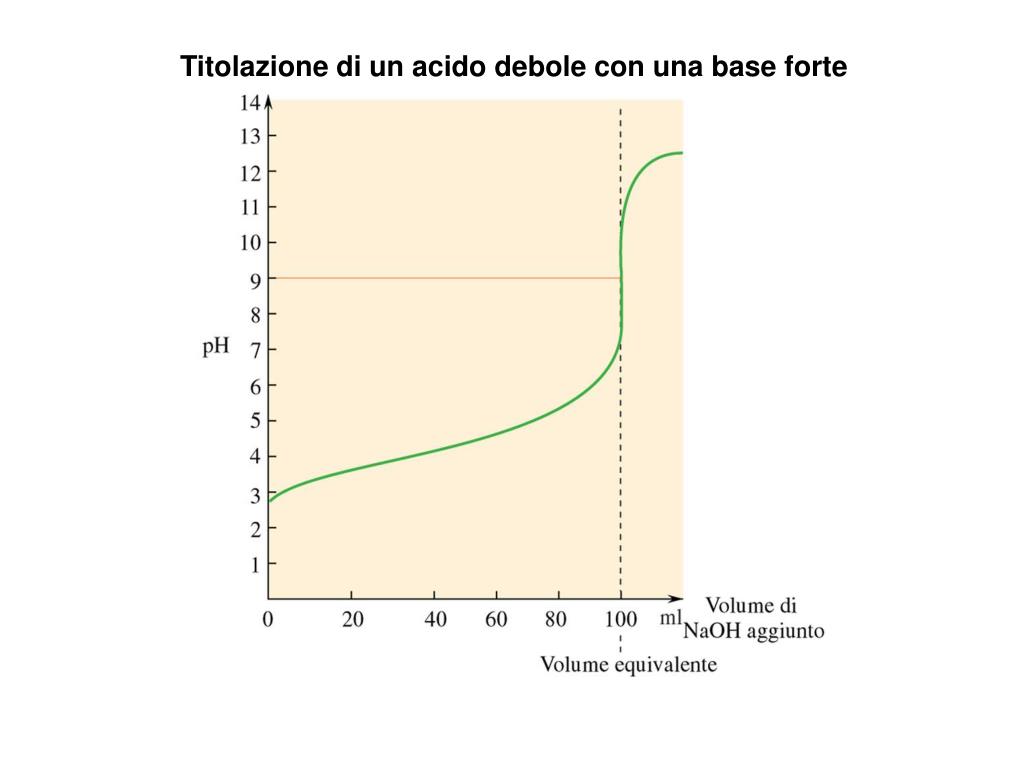
A differenza della curva di titolazione di un acido forte, dove il pH iniziale è molto basso e aumenta rapidamente con l'aggiunta delle prime gocce di base, la curva di un acido debole inizia con un pH più alto e l'aumento iniziale è più graduale. Questo riflette la parziale dissociazione dell'acido debole all'inizio della titolazione.
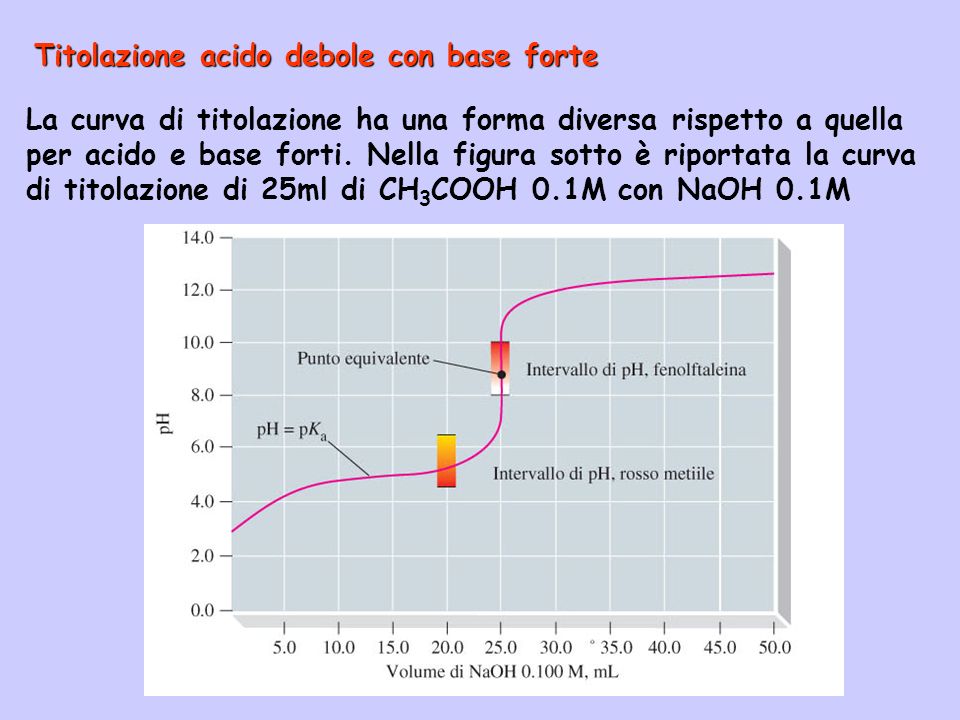
La Regione Tampone e il Punto di Semi-Equivalenza
La presenza di una regione tampone è una caratteristica distintiva. All'interno di questa regione, il pH varia molto lentamente con l'aggiunta di base. Il punto di semi-equivalenza, dove pH = pKa, è facilmente identificabile all'interno della regione tampone e fornisce un modo sperimentale per determinare la Ka dell'acido debole.
Salto di pH Meno Pronunciato al Punto di Equivalenza
Il salto di pH (la rapida variazione del pH) in corrispondenza del punto di equivalenza è meno pronunciato rispetto a quello osservato nelle titolazioni acido forte-base forte. Questo rende la scelta dell'indicatore più critica, in quanto l'intervallo di viraggio dell'indicatore deve rientrare nel salto di pH per una determinazione accurata del punto di equivalenza.
Esempi Reali e Dati
Consideriamo la titolazione di acido acetico (CH3COOH), un acido debole, con idrossido di sodio (NaOH), una base forte. L'acido acetico ha un Ka di circa 1.8 x 10-5, il che corrisponde a un pKa di circa 4.76.
- Inizio della titolazione: Una soluzione di acido acetico 0.1 M ha un pH iniziale di circa 2.87 (calcolabile considerando l'equilibrio di dissociazione).
- Regione Tampone: Durante l'aggiunta di NaOH, si forma l'acetato di sodio (CH3COONa), la base coniugata dell'acido acetico. La soluzione si comporta come un tampone. Ad esempio, quando si è aggiunta la metà della quantità di NaOH necessaria per raggiungere il punto di equivalenza (punto di semi-equivalenza), il pH sarà circa 4.76, uguale al pKa dell'acido acetico.
- Punto di Equivalenza: Al punto di equivalenza, tutto l'acido acetico è stato convertito in acetato di sodio. Il pH a questo punto è superiore a 7, tipicamente intorno a 8.7-9.0. Questo è dovuto all'idrolisi dell'acetato.
- Dopo il punto di equivalenza: L'aggiunta di ulteriore NaOH provoca un rapido aumento del pH, che poi si stabilizza man mano che aumenta la concentrazione di NaOH.
Un altro esempio comune è la titolazione dell'acido lattico, presente nel latte e nei muscoli durante l'esercizio fisico, con una base forte. Le curve di titolazione di aminoacidi, che contengono sia gruppi acidi che basici, sono ancora più complesse e mostrano multiple regioni tampone corrispondenti ai diversi gruppi funzionali.
Le curve di titolazione sono utilizzate in diversi ambiti:
- Chimica Analitica: Determinazione precisa della concentrazione di acidi o basi sconosciute.
- Biochimica: Studio del comportamento di amminoacidi, proteine e altri biomolecole.
- Scienza dell'Alimentazione: Controllo della qualità e stabilità degli alimenti.
- Farmaceutica: Analisi della purezza e concentrazione dei farmaci.
Conclusioni e Call to Action
La curva di titolazione di un acido debole con una base forte è uno strumento potente per comprendere le reazioni acido-base e le proprietà degli acidi deboli. La presenza della regione tampone, il punto di semi-equivalenza e il pH al punto di equivalenza sono caratteristiche chiave che la distinguono da altre titolazioni. Comprendere questi concetti è essenziale per chiunque lavori in chimica, biochimica o discipline correlate.
Per approfondire la tua conoscenza, ti invito a:
- Eseguire titolazioni pratiche: Metti in pratica la teoria eseguendo titolazioni di acidi deboli con basi forti in laboratorio.
- Simulare titolazioni: Utilizza software di simulazione per esplorare l'effetto di diversi parametri (Ka, concentrazione) sulla curva di titolazione.
- Approfondire la teoria: Studia i principi di equilibrio chimico e le equazioni che governano le titolazioni.
Padroneggiare la titolazione acido debole-base forte ti fornirà una solida base per affrontare sfide analitiche più complesse e contribuire a una comprensione più profonda del mondo chimico che ci circonda. La conoscenza di questi concetti è un investimento nel tuo futuro scientifico.