Ti sei mai trovato a fissare un termometro mentre l'acqua bolle, chiedendoti perché la temperatura sembra bloccarsi a 100°C? Oppure, hai mai avuto difficoltà a visualizzare cosa succede esattamente alle molecole mentre un cubetto di ghiaccio si scioglie? La curva di riscaldamento di una sostanza pura può sembrare un concetto astratto all'inizio, ma una volta compresa, apre le porte a una comprensione più profonda della termodinamica e dei cambiamenti di fase. Questo articolo ti guiderà attraverso questo argomento, rendendolo accessibile e pratico.
Cosa è una Curva di Riscaldamento?
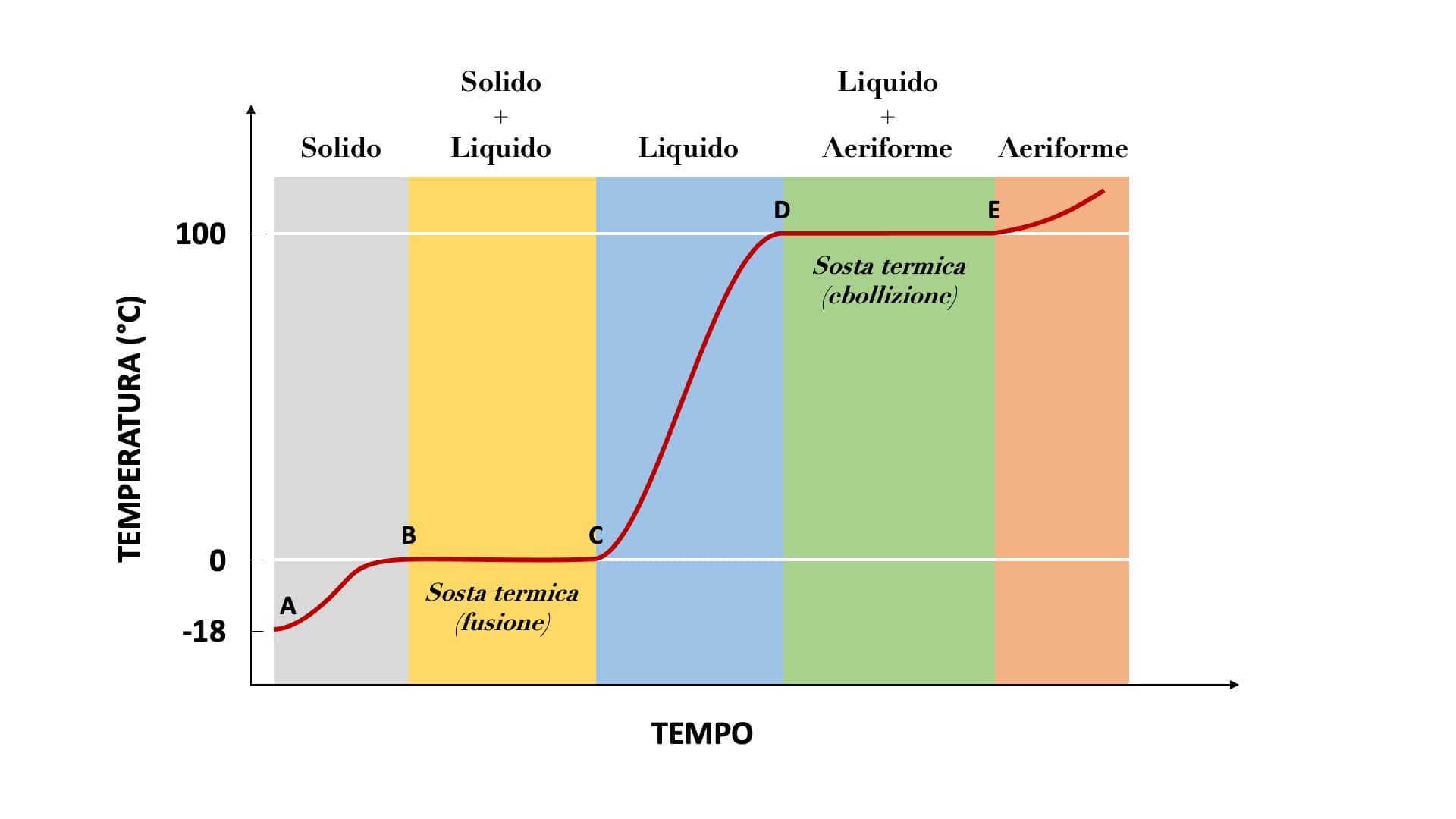
Una curva di riscaldamento è un grafico che mostra come la temperatura di una sostanza cambia nel tempo mentre viene riscaldata a un tasso costante. In pratica, immagina di prendere un blocco di ghiaccio a -20°C e di fornirgli calore in modo uniforme. La curva di riscaldamento ci mostrerà come la temperatura del ghiaccio aumenta, come si scioglie, come la temperatura dell'acqua aumenta e, infine, come l'acqua bolle.
Secondo la maggior parte dei libri di testo di chimica e fisica di base, le curve di riscaldamento sono essenziali per comprendere le proprietà termiche della materia (Atkins, P., & de Paula, J. (2010). Atkins' Physical Chemistry. Oxford University Press.).
Componenti Chiave di una Curva di Riscaldamento
Una curva di riscaldamento tipica di una sostanza pura presenta diverse sezioni distinte:
- Fase solida: La temperatura aumenta gradualmente mentre il solido assorbe calore. Le molecole vibrano più velocemente, ma rimangono nella loro posizione fissa.
- Fusione (transizione solido-liquido): La temperatura rimane costante mentre il solido si trasforma in liquido. L'energia fornita viene utilizzata per rompere i legami intermolecolari, non per aumentare l'energia cinetica delle molecole. Questo è il punto di fusione.
- Fase liquida: La temperatura aumenta nuovamente mentre il liquido assorbe calore. Le molecole hanno maggiore libertà di movimento.
- Ebollizione (transizione liquido-gas): La temperatura rimane costante mentre il liquido si trasforma in gas. L'energia viene utilizzata per superare le forze attrattive intermolecolari e permettere alle molecole di sfuggire in fase gassosa. Questo è il punto di ebollizione.
- Fase gassosa: La temperatura aumenta nuovamente mentre il gas assorbe calore. Le molecole si muovono molto rapidamente e in modo disordinato.
Perché la Temperatura Rimane Costante Durante i Cambi di Fase?
Questo è un punto cruciale. L'energia che forniamo durante la fusione o l'ebollizione non va ad aumentare l'energia cinetica delle molecole (e quindi la temperatura). Viene invece utilizzata per superare le forze intermolecolari che tengono le molecole unite. Immagina di dover rompere un mucchio di legnetti. Devi spendere energia per separarli, anche se la loro temperatura non cambia.
Questo concetto è direttamente legato al calore latente, che è l'energia richiesta per cambiare lo stato di una sostanza senza cambiare la sua temperatura (Silberberg, M. S., & Amateis, P. G. (2018). Chemistry: The Molecular Nature of Matter and Change. McGraw-Hill Education.). Ci sono due tipi principali di calore latente:
- Calore latente di fusione: L'energia necessaria per fondere una sostanza solida alla sua temperatura di fusione.
- Calore latente di vaporizzazione: L'energia necessaria per vaporizzare una sostanza liquida alla sua temperatura di ebollizione.
Come Costruire e Interpretare una Curva di Riscaldamento
Passaggi per la Costruzione
- Materiali: Procurati un campione di sostanza pura (ad esempio, acqua distillata), un becher, un termometro, una piastra riscaldante (o un bagno maria), un agitatore magnetico (opzionale), e un cronometro.
- Procedura: Metti il campione nel becher e posizionalo sulla piastra riscaldante. Inserisci il termometro nel campione, assicurandoti che non tocchi il fondo del becher. Accendi la piastra riscaldante a una potenza costante.
- Raccolta Dati: Registra la temperatura del campione a intervalli regolari (ad esempio, ogni 30 secondi o 1 minuto). Continua a registrare la temperatura finché la sostanza non è completamente passata alla fase gassosa.
- Grafico: Traccia i dati su un grafico, con il tempo sull'asse x (ascissa) e la temperatura sull'asse y (ordinata).
Interpretazione della Curva
- Segmenti Inclinati: I segmenti inclinati rappresentano le fasi in cui la temperatura sta aumentando. La pendenza di questi segmenti dipende dalla capacità termica della sostanza in quella fase. Una capacità termica più bassa significa che la temperatura aumenterà più rapidamente con la stessa quantità di calore.
- Segmenti Orizzontali: I segmenti orizzontali rappresentano i cambi di fase. La temperatura rimane costante perché l'energia viene utilizzata per superare le forze intermolecolari. La lunghezza di questi segmenti è proporzionale alla quantità di calore latente richiesta per la transizione.
- Punti di Fusione e Ebollizione: I valori di temperatura a cui si verificano i segmenti orizzontali corrispondono ai punti di fusione e di ebollizione della sostanza. Questi sono indicatori chiave dell'identità della sostanza.
Strumenti e Tecniche Utili
- Simulazioni al computer: Esistono molte simulazioni online che permettono di visualizzare le curve di riscaldamento e di sperimentare con diversi parametri. Cerca "heating curve simulation" su Google.
- Software di analisi dati: Software come Excel o Google Sheets possono essere utilizzati per creare e analizzare le curve di riscaldamento.
- Calorimetria: La calorimetria è una tecnica sperimentale che permette di misurare la quantità di calore assorbita o rilasciata durante un processo fisico o chimico. Può essere utilizzata per determinare i calori latenti di fusione e vaporizzazione.
Esempio Pratico: Curva di Riscaldamento dell'Acqua
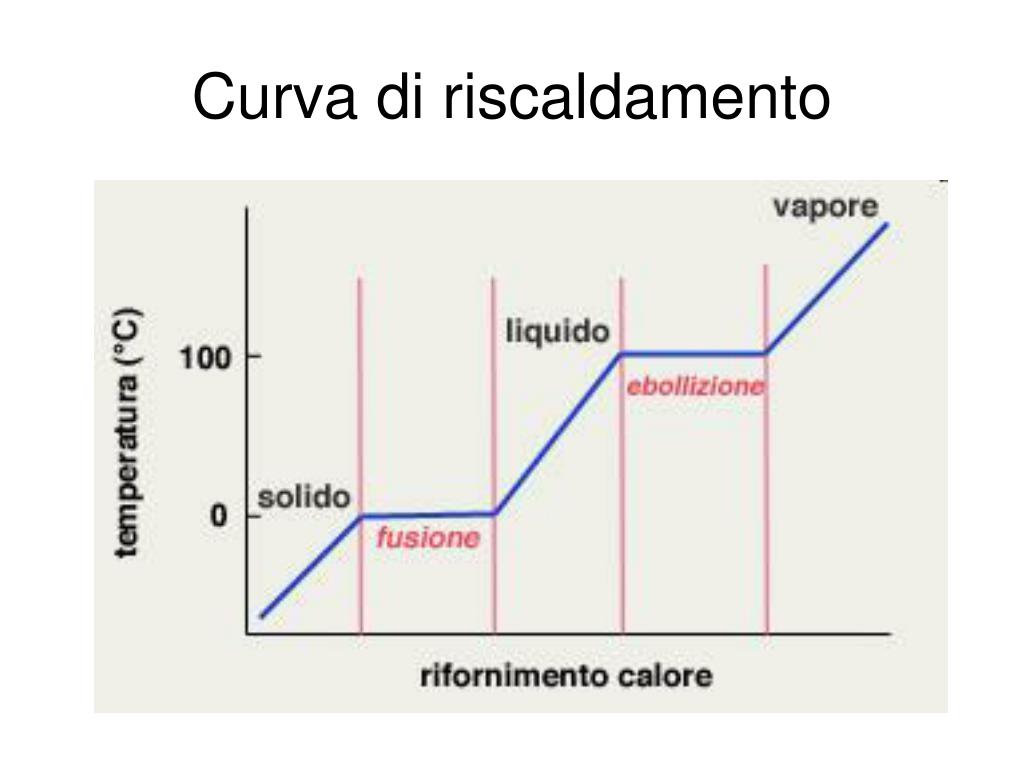
Consideriamo l'acqua (H2O). Se partiamo da ghiaccio a -20°C e lo riscaldiamo gradualmente, vedremo la seguente curva:
- Riscaldamento del ghiaccio: La temperatura del ghiaccio aumenta da -20°C a 0°C.
- Fusione del ghiaccio: La temperatura rimane costante a 0°C mentre il ghiaccio si trasforma in acqua liquida.
- Riscaldamento dell'acqua: La temperatura dell'acqua aumenta da 0°C a 100°C.
- Ebollizione dell'acqua: La temperatura rimane costante a 100°C mentre l'acqua si trasforma in vapore acqueo.
- Riscaldamento del vapore: La temperatura del vapore acqueo aumenta oltre i 100°C.
I punti di fusione (0°C) e di ebollizione (100°C) sono caratteristici dell'acqua e possono essere utilizzati per identificarla.
Applicazioni Pratiche delle Curve di Riscaldamento
La comprensione delle curve di riscaldamento ha numerose applicazioni in diversi campi:
- Scienza dei materiali: Per determinare le proprietà termiche dei materiali e progettare materiali con specifiche caratteristiche di fusione e solidificazione.
- Chimica: Per identificare sostanze pure e determinare la loro purezza. Un campione impuro avrà un punto di fusione o ebollizione più ampio.
- Ingegneria: Per progettare processi industriali che coinvolgono cambiamenti di fase, come la distillazione, la cristallizzazione e la fusione di metalli.
- Gastronomia: Comprendere come la temperatura influenza la cottura degli alimenti e i cambiamenti di fase che avvengono durante la cottura (ad esempio, la cottura di un uovo).
Errori Comuni e Come Evitarli
- Riscaldamento non uniforme: Assicurati che il campione sia riscaldato in modo uniforme per ottenere risultati accurati. Utilizza un agitatore magnetico, se disponibile.
- Termometro impreciso: Utilizza un termometro calibrato per evitare errori di misurazione.
- Perdita di calore: Isola il becher per ridurre al minimo la perdita di calore verso l'ambiente circostante.
- Non registrare i dati abbastanza frequentemente: Assicurati di registrare i dati a intervalli regolari per catturare accuratamente la forma della curva.
Conclusione
Le curve di riscaldamento sono uno strumento potente per comprendere i cambiamenti di fase e le proprietà termiche della materia. Comprendendo i principi alla base di queste curve, puoi acquisire una visione più profonda della termodinamica e delle sue numerose applicazioni pratiche. Sperimenta, esplora le simulazioni, e metti in pratica le tue conoscenze. Buon apprendimento!