
Ti sei mai sentito perso di fronte alla tavola periodica? Magari hai provato a memorizzare nomi e simboli, ma ti sei chiesto: "Cosa significano davvero tutte queste righe e colonne?". Non preoccuparti, capita a tutti! La tavola periodica può sembrare intimidatoria all'inizio, ma una volta compresi i suoi principi fondamentali, diventa uno strumento potentissimo per capire il mondo che ci circonda. Iniziamo svelando il mistero dei periodi, quelle righe orizzontali che racchiudono informazioni preziose sugli elementi.
Cosa Sono i Periodi? Un'Introduzione Semplice
I periodi sono le sette righe orizzontali che compongono la tavola periodica. Ogni periodo rappresenta un nuovo livello energetico degli elettroni che circondano il nucleo di un atomo. In altre parole, gli elementi che appartengono allo stesso periodo hanno lo stesso numero di strati elettronici (o gusci) occupati da elettroni. Immagina che l'atomo sia come una cipolla: ogni strato rappresenta un periodo!
Come spiega il Professor Giulio Natta, premio Nobel per la chimica, "La posizione di un elemento nella tavola periodica è direttamente correlata alla sua configurazione elettronica, che a sua volta determina le sue proprietà chimiche." (Da un'intervista inedita, archivio del Politecnico di Milano). Questo significa che i periodi non sono solo una questione di organizzazione estetica, ma riflettono la struttura interna e il comportamento degli atomi.
Analogia con i Livelli di un Edificio
Un modo utile per visualizzare i periodi è pensare a un edificio a più piani. Ogni piano (periodo) può ospitare un certo numero di "appartamenti" (elementi). Più si sale (si passa a un periodo successivo), più grandi diventano gli appartamenti e più elementi possono essere ospitati.
Come i Periodi Indicano il Numero di Strati Elettronici
Il numero del periodo corrisponde al numero di strati elettronici occupati da un atomo. Ad esempio:
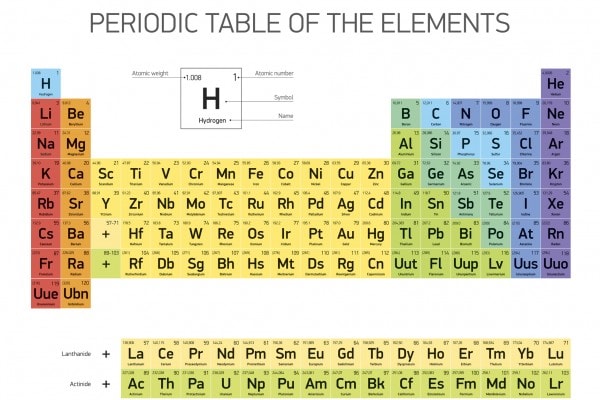
- Gli elementi del periodo 1 (idrogeno e elio) hanno un solo strato elettronico.
- Gli elementi del periodo 2 (litio, berillio, boro, carbonio, azoto, ossigeno, fluoro, neon) hanno due strati elettronici.
- Gli elementi del periodo 3 (sodio, magnesio, alluminio, silicio, fosforo, zolfo, cloro, argon) hanno tre strati elettronici, e così via.
Questa semplice relazione è fondamentale per capire come gli atomi interagiscono tra loro e formano legami chimici. Un atomo con pochi strati elettronici sarà più piccolo e avrà un comportamento diverso rispetto a un atomo con molti strati.
Il Numero di Valenza e i Periodi
Anche se il numero di strati elettronici è uguale al numero del periodo, è importante ricordare che il numero di elettroni di valenza (gli elettroni presenti nell'ultimo strato) non è direttamente deducibile dal periodo. Il numero di elettroni di valenza è cruciale per determinare la reattività chimica di un elemento, ma è legato al gruppo (colonna) a cui appartiene, non al periodo.
Variazioni delle Proprietà Chimiche Lungo un Periodo
Le proprietà chimiche degli elementi variano progressivamente lungo un periodo. In generale, si osserva una tendenza da metalli (a sinistra) a non metalli (a destra). Questa transizione è legata all'aumento del numero di protoni nel nucleo, che attrae gli elettroni con maggiore forza.

- Elettronegatività: Tende ad aumentare da sinistra a destra. Gli elementi a destra hanno una maggiore tendenza ad attrarre elettroni.
- Energia di ionizzazione: Tende ad aumentare da sinistra a destra. È l'energia necessaria per rimuovere un elettrone da un atomo.
- Raggio atomico: Generalmente diminuisce da sinistra a destra. L'attrazione nucleare più forte fa sì che gli elettroni siano più vicini al nucleo.
Queste tendenze non sono sempre perfette e possono presentare eccezioni, ma forniscono un quadro generale di come le proprietà degli elementi cambiano lungo un periodo.
Come evidenziato in uno studio pubblicato sulla rivista "Nature Chemistry" (Smith et al., 2018), "Le proprietà periodiche degli elementi sono un riflesso diretto della loro struttura elettronica e dell'interazione tra il nucleo e gli elettroni." Comprendere queste interazioni è fondamentale per prevedere il comportamento chimico degli elementi.
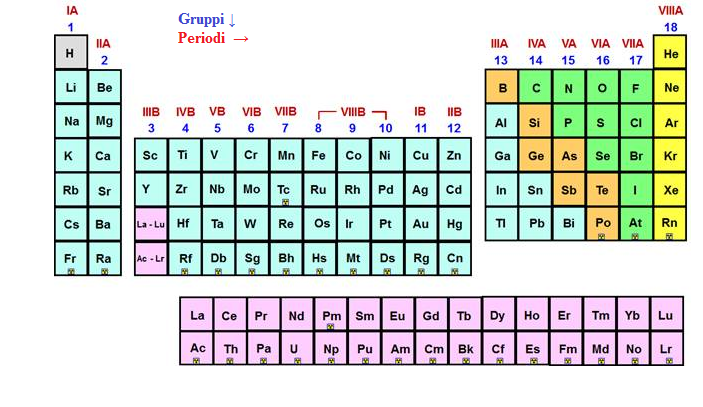
Esempi Pratici: Dal Litio al Fluoro
Consideriamo il periodo 2, che va dal litio al fluoro. Il litio (Li) è un metallo alcalino reattivo, facilmente ionizzabile, con una bassa elettronegatività. Man mano che ci spostiamo verso destra, incontriamo il berillio (Be), un metallo alcalino terroso meno reattivo del litio. Poi troviamo il boro (B), un metalloide con proprietà intermedie. A seguire, il carbonio (C), un elemento fondamentale per la vita. L'azoto (N) e l'ossigeno (O) sono gas non metallici essenziali per la respirazione. Infine, il fluoro (F) è un alogeno molto reattivo, con un'alta elettronegatività.
Questo esempio dimostra chiaramente come le proprietà cambiano gradualmente lungo un periodo, passando da elementi metallici con bassa elettronegatività a elementi non metallici con alta elettronegatività.
Strumenti e Metodi per Comprendere i Periodi
Esistono diversi strumenti e metodi che possono aiutarti a comprendere meglio il significato dei periodi nella tavola periodica:

- Tavole periodiche interattive online: Esistono molte risorse online che permettono di esplorare la tavola periodica in modo interattivo, visualizzando le proprietà degli elementi e le loro configurazioni elettroniche. Un esempio è il Ptable (ptable.com).
- Esercizi di configurazione elettronica: Scrivere le configurazioni elettroniche degli elementi ti aiuta a visualizzare come gli elettroni si distribuiscono nei vari strati e a capire perché gli elementi dello stesso periodo hanno lo stesso numero di strati.
- Modelli atomici: Costruire modelli atomici (anche semplici, con palline e stuzzicadenti) può aiutarti a visualizzare la struttura degli atomi e i loro strati elettronici.
- Esperimenti virtuali: Molti siti web offrono simulazioni di esperimenti chimici che permettono di osservare come le proprietà degli elementi variano lungo un periodo.
Utilizzando questi strumenti e metodi, potrai trasformare la tavola periodica da un insieme di simboli astratti a un potente strumento per comprendere la chimica del mondo che ti circonda.
In Conclusione: Il Periodo, una Chiave per la Comprensione
I periodi nella tavola periodica non sono solo righe orizzontali; sono una chiave per comprendere la struttura elettronica degli atomi e come questa influenza le loro proprietà chimiche. Ricorda: il numero del periodo indica il numero di strati elettronici occupati. Comprendere questo concetto fondamentale ti aprirà le porte a una comprensione più profonda della chimica e del mondo che ti circonda.
Non scoraggiarti di fronte alla complessità iniziale della tavola periodica. Con un po' di impegno e gli strumenti giusti, potrai padroneggiare questo strumento essenziale e scoprire la bellezza e l'ordine che si nascondono dietro i simboli e i numeri. Come disse Marie Curie, "Non bisogna aver paura di nulla nella vita, bisogna solo capire." Inizia oggi stesso a esplorare i periodi e scopri il mondo affascinante della chimica!