
Ciao a tutti voi, curiosi esploratori del mondo che ci circonda! Oggi facciamo un piccolo viaggio alla scoperta di qualcosa che, diciamocelo, suona un po' come un esame di chimica. Ma state tranquilli, qui non si boccia nessuno! Parliamo di quelle che gli scienziati chiamano "gruppi" nella Tavola Periodica degli Elementi.
Immaginate la Tavola Periodica come una gigantesca libreria, dove ogni libro è un elemento chimico. Ci sono libri piccolissimi, come l'Elio (quello che fa fare le vocine buffe ai palloncini!), e libri enormi, con storie complicate che solo i super esperti capiscono. Ma cosa sono questi "gruppi" di cui tanto si parla? Sono un po' come le scaffalature speciali di questa libreria.
Pensatela così: avete presente quando organizzate la vostra collezione di dischi, film o, perché no, i vostri barattoli di spezie? Magari mettete insieme tutti i CD di rock, oppure tenete vicini tutti i tipi di pasta. Ecco, i chimici hanno fatto una cosa simile con gli elementi.
I gruppi sono le colonne verticali della Tavola Periodica. Tutti gli elementi che si trovano nella stessa colonna (nella stessa "scaffalatura", per continuare la metafora) hanno un po' un carattere simile. È come se appartenessero alla stessa famiglia allargata, con parenti che si assomigliano nelle abitudini, nei modi di fare, o nelle cose che gli piacciono fare.
Perché dovremmo interessarci a queste "famiglie" chimiche?
Beh, perché sapere che un elemento appartiene a un certo gruppo ci dice un sacco di cose su di lui, senza dover studiare ogni singolo libro della libreria. È come conoscere il cognome di una persona: a volte, solo dal cognome si può intuire qualcosa sulla famiglia, sulle sue origini o magari su certe tradizioni che portano avanti da generazioni.
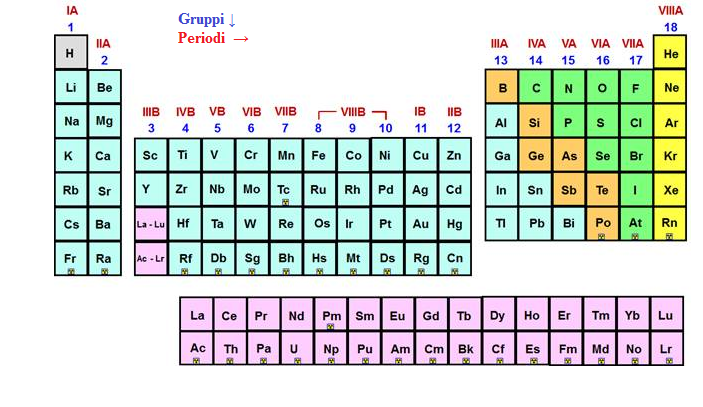
In termini chimici, questo "carattere simile" si traduce nelle proprietà chimiche. Come si comportano quando li metti a contatto con altre cose? Sono reattivi o sono timidi? Si combinano facilmente o tendono a stare per conto loro? La risposta è spesso scritta nella loro appartenenza a un gruppo.
Incontriamo alcune di queste famiglie!
Prendiamo ad esempio il Gruppo 1. Questi sono gli alcalini. Pensate al sodio (quello del sale da cucina!) o al potassio (che fa bene alle banane!). Questi elementi sono come i bambini super energetici della Tavola Periodica: molto, molto reattivi. Se provate a mettere un pezzettino di sodio o potassio in acqua... beh, meglio non provarci a casa, ma sappiate che reagiscono in modo spettacolare, quasi esplosivo! Sono così desiderosi di combinarsi con altre cose che, se li lasciate troppo esposti all'aria o all'umidità, iniziano subito a fare casino. Li teniamo custoditi con cura, quasi come tesori preziosi e un po' pericolosi!
Un altro esempio divertente è il Gruppo 17, gli alogeni. Qui troviamo elementi come il fluoro (quello che protegge i nostri denti nel dentifricio!) e il cloro (quello che purifica l'acqua delle piscine, e che fa anche parte del sale, ma attenzione: non mangiatelo puro!). Gli alogeni sono come degli “affamati di elettroni”. Hanno bisogno di un “abbraccio” da un altro elemento per sentirsi completi. Sono anche loro piuttosto reattivi, ma in modo diverso dagli alcalini. Il fluoro è talmente desideroso di catturare elettroni che è l'elemento più reattivo di tutti! È come quel compagno di classe super volenteroso che vuole sempre essere il primo a fare tutto. Il cloro, invece, è un po' più… gestibile, diciamo. Se lo incontrate nel sale da cucina (cloruro di sodio), è tranquillissimo e fondamentale per la nostra vita.

E che dire degli elementi del Gruppo 18? Questi sono i gas nobili. L'elio che fa volare i palloncini, il neon che illumina le insegne colorate, l'argon che si usa nelle lampadine per farle durare di più. Questi sono gli “introversi” della Tavola Periodica. Sono così contenti e stabili così come sono che non gli interessa quasi per niente reagire con altri elementi. Sono come le persone che sono perfettamente felici di stare per conto loro, con i loro hobby, senza bisogno di fare grandi chiacchiere o feste con sconosciuti. Sono preziosi proprio per questa loro indipendenza!
Un po' di storia e qualche aneddoto per sorridere
La Tavola Periodica non è nata dal nulla, eh! È un po' il risultato di un lavoro di squadra durato anni, con tanti scienziati che hanno contribuito a mettere ordine nel caos degli elementi scoperti. Il merito principale va a Dmitri Mendeleev, un chimico russo che, quasi per magia, nel 1869, mise gli elementi in ordine non solo per peso atomico, ma anche raggruppandoli per proprietà simili. Si racconta che Mendeleev avesse anche sognato la sua tavola! Una bella ispirazione notturna, no?
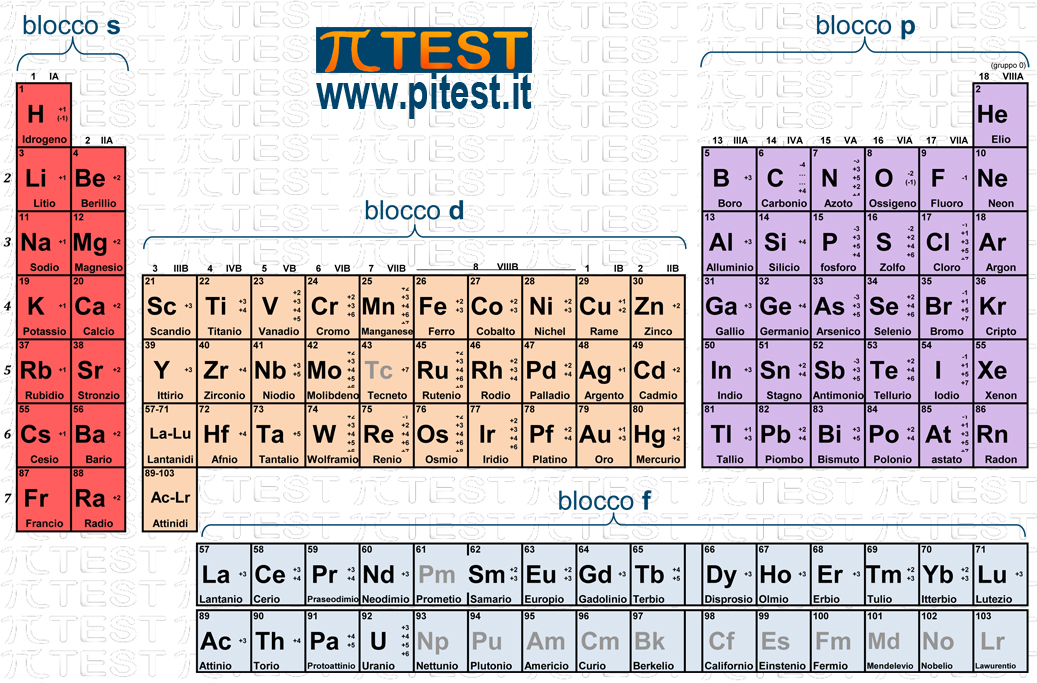
Mendeleev era così intelligente che, quando mise insieme la sua tavola, si accorse che c'erano degli spazi vuoti. Invece di dire "manca qualcosa", disse: "Ci saranno elementi che non abbiamo ancora scoperto, e saranno proprio qui!". E indovinate un po'? Aveva ragione! Ha persino predetto le proprietà di questi elementi mancanti, che poi sono stati effettivamente trovati. È un po' come dire: "So che da qualche parte in giardino c'è una rosa che ancora non ho visto, e so che avrà petali rossi e un profumo inebriante". Mica male come intuito!
E tutto questo, cosa c'entra con noi?
C'entra, c'entra eccome! Ogni volta che usiamo un medicinale, cuciniamo un piatto delizioso, guardiamo la televisione, o persino quando respiriamo, stiamo facendo i conti con gli elementi chimici e le loro proprietà. Capire i gruppi ci aiuta a capire perché certe cose funzionano come funzionano.
Per esempio, sappiamo che i metalli alcalino-terrosi (Gruppo 2) sono meno reattivi degli alcalini (Gruppo 1), ma sono comunque abbastanza reattivi da essere importanti nella costruzione di leghe metalliche resistenti per aerei o automobili. O che il calcio, membro di questo gruppo, è fondamentale per le nostre ossa.

Capire i gruppi ci aiuta anche a capire le differenze tra materiali. Perché l'oro luccica sempre e non si ossida (è un metallo nobile, piuttosto indipendente!), mentre il ferro arrugginisce in un lampo (è molto più propenso a reagire con l'ossigeno)? La risposta è anche nelle loro posizioni nella Tavola Periodica, e quindi nella loro appartenenza a determinati gruppi.
Insomma, i gruppi nella Tavola Periodica non sono solo numeri e simboli strani. Sono delle etichette preziose che ci svelano le parentele e i comportamenti degli elementi che compongono tutto ciò che vediamo e tocchiamo. Sono come i capitoli di un libro che ci guidano nella comprensione di una storia incredibilmente complessa e affascinante: quella della materia!
Quindi, la prossima volta che vedrete una Tavola Periodica, invece di pensare "che fatica!", pensate piuttosto a una grande famiglia, organizzata in comode scaffalature, dove ogni gruppo ha i suoi membri con i loro talenti unici e le loro personalità. E questo, cari amici, è un modo decisamente più divertente e accessibile di vedere il mondo che ci circonda, un atomo alla volta!