
Ciao! Come stai? Siediti comodo, prendi il tuo caffè (o tè, non giudico!), perché oggi parliamo di una cosa che potrebbe sembrarti noiosa, ma ti assicuro che è più interessante di quanto pensi. Parliamo di <solvente> e <soluto>. Ti suona familiare? Magari l'hai sentito al liceo, vero? Quel momento in cui pensavi: "Ma a cosa mi servirà mai nella vita?". Beh, fidati, serve eccome! È tipo la base di tutto, la ricetta segreta di tante cose che usiamo ogni giorno, dal caffè che stai bevendo adesso, alla medicina che ti cura il mal di testa, persino l'aria che respiri!
Pensala così: sei in cucina, devi fare qualcosa di speciale. Hai bisogno di ingredienti, giusto? Ecco, in chimica, quando mescoli le cose, di solito hai un protagonista e uno che si fa da parte. Non nel senso che viene maltrattato, eh! Solo che uno fa il grosso del lavoro e l'altro si scioglie. Tutto qui!
Ma cos'è questo "Scioglimento"?
Immagina di buttare un pizzico di zucchero nel tuo caffè. Cosa succede? Lo zucchero sparisce, vero? Non è che si è teletrasportato, si è semplicemente <sciolto>. Si è mescolato così bene con il caffè che non riesci più a vederlo. È come se fosse diventato uno con il caffè. Magico, no? Ecco, questo processo si chiama <soluzione>. E ogni soluzione ha i suoi due eroi, anzi, i suoi due partecipanti: il <solvente> e il <soluto>.
E non è solo lo zucchero nel caffè, eh! Pensa a quando lavi le mani con il sapone. Il sapone si scioglie nell'acqua. E se ti tagli e metti un cerotto con la medicazione disinfettante? Quella roba che disinfetta si è sciolta in qualcosa per poter agire. Capisci? È ovunque!
Il Solvente: Il Supereroe Discreto
Allora, chi è il nostro supereroe discreto? È il <solvente>. Pensa a lui come al "capo". È la sostanza che fa da sfondo, quella che è più abbondante nella miscela. È lui che accoglie l'altro ingrediente e lo fa sparire, lo fa diventare parte di sé. È un po' come il mare che accoglie una goccia di pioggia, o un grande abbraccio che ingloba qualcuno.
Il <solvente> è quello che, diciamo, "mantiene la casa". È lì, pronto ad accogliere chiunque abbia bisogno di una sistemata, di un posto dove stare. Ed è fantastico perché non viene consumato nel processo, rimane lì, pronto per la prossima avventura chimica!
Il Re dei Solventi: L'Acqua!
Se dovessimo nominare il re dei re dei solventi, sarebbe senza dubbio l'<acqua>! Sì, sì, quella roba trasparente e insapore che bevi. L'acqua è un solvente pazzesco. È un <solvente universale>, quasi tutto si scioglie in lei. Pensaci: sali, zuccheri, molte vitamine, persino un po' di gas! È per questo che il nostro corpo, che è fatto per la maggior parte d'acqua, è un ambiente così perfetto per le reazioni chimiche.

Senza l'acqua come solvente, molte delle cose che diamo per scontate semplicemente non esisterebbero. Dalla nostra stessa vita, alle bevande che ci dissetano, ai processi naturali che ci mantengono in vita. Un vero MVP, no?
Ma non c'è solo l'acqua!
Certo, l'acqua è la star, ma non è l'unica! Esistono un sacco di altri solventi, ognuno con le sue peculiarità. Ci sono solventi <organici>, per esempio. Pensa all'<acetone> che usi per toglierti lo smalto. Quello è un solvente! E l'<alcol>? Anche quello è un solvente! Pensa all'alcool isopropilico che si usa per pulire le lenti o per disinfettare. Scioglie via lo sporco e i grassi.
E poi ci sono solventi più "esotici", usati nell'industria, per sciogliere pitture, colle, resine. Ognuno ha il suo compito, ognuno è speciale a modo suo. È un po' come avere un set di attrezzi: a seconda del lavoro che devi fare, usi lo strumento giusto. E il solvente è proprio questo: lo strumento per sciogliere, per mescolare, per creare nuove cose.
Il Soluto: L'Ospite Speciale
E adesso, chi è l'<ospite>? È il <soluto>! Lui è quello che viene <sciolto> nel solvente. È un po' il protagonista che, per poter dare il meglio di sé, ha bisogno di un "palcoscenico" fatto dal solvente. È come l'attore che sale sul palco per recitare la sua parte, e il palco è il solvente.

Il <soluto> è la sostanza che viene dispersa nel solvente. Potrebbe essere solido, liquido o persino gassoso. La cosa importante è che, una volta sciolto, non si vede più come entità separata. Si è amalgamato. È parte integrante della soluzione.
Esempi di Soluti che Conosciamo Tutti
Torniamo al nostro caffè. Lo <zucchero> è il soluto. Il <sale> che metti nella pasta, quello è un soluto! E quando fai un tè? La bustina contiene le foglie di tè, che sono il <soluto>. Il tè, una volta sciolto nell'acqua calda, rilascia il suo sapore, il suo colore.
Pensa ai rimedi che prendi quando hai la febbre. Molte pastiglie si sciolgono in acqua. La sostanza attiva che ti fa stare meglio è il <soluto>. Viene sciolta in un solvente (l'acqua) per poter essere assorbita dal tuo corpo più facilmente. È geniale, no?
E il dentifricio? Quello che usi per lavarti i denti contiene un sacco di cose che sono disciolte in una base. Il <fluoro>, per esempio, che protegge i tuoi denti, è sciolto lì dentro. Tanti ingredienti, ognuno al suo posto, che lavorano insieme per un risultato migliore.
La Magia della Concentrazione: Quanto ce n'è?
Ora, un'altra cosa super importante è: <quanta> roba sciolta c'è? Non è che puoi buttare un sacco di zucchero nel tuo caffè e aspettarti che si sciolga tutto, vero? Arriva un punto in cui il solvente dice: "Basta! Ho fatto il mio lavoro, non posso più accogliere altro!".

Questo ci porta al concetto di <concentrazione>. È semplicemente la quantità di soluto presente in una data quantità di solvente (o di soluzione). Ci sono soluzioni molto <diluite>, dove c'è poco soluto e tanto solvente. E poi ci sono soluzioni <sature> o <supersature>, dove il soluto è al suo massimo, anzi, a volte anche oltre il limite!
Immagina di fare una limonata. Se metti poco limone e tanto zucchero, sarà dolce ma poco aspra. Se metti tanto limone e poco zucchero, sarà aspra. Se metti la quantità giusta di entrambi, avrai la limonata perfetta! Ecco, quella è la <concentrazione> che funziona per te.
Tipi di Soluzioni: Non tutte uguali!
Esistono un sacco di modi in cui solvente e soluto possono mescolarsi, o non mescolarsi. È un mondo affascinante, fidati!
- Soluzioni Vere: Queste sono quelle che abbiamo descritto finora. Il soluto è disciolto in modo così fine che non lo vedi più, neanche con un microscopio. Lo zucchero nell'acqua, il sale nell'acqua. Perfetto.
- Sospensioni: Qui le cose sono un po' più "turbolente". Il soluto è disperso, ma non è veramente disciolto. Se lasci riposare una sospensione, il soluto si deposita sul fondo. Pensa al succo di frutta con polpa, o all'acqua sporca. Se non lo agiti, la "roba" cade giù.
- Colloidi: Questa è una via di mezzo, un po' più complicata. Le particelle di soluto sono più grandi di quelle delle soluzioni vere, ma abbastanza piccole da restare sospese nell'aria o nel liquido senza depositarsi. Pensa al latte. È una sospensione di grassi e proteine nell'acqua. O al fumo. Le particelline di carbonio rimangono sospese nell'aria. Non si depositano subito.
È come organizzare una festa. Le soluzioni vere sono gli invitati che si sono mescolati perfettamente, parlano tutti tra loro. Le sospensioni sono quelli che stanno lì in un angolo, un po' separati, e se vai via, loro rimangono dov'erano. I colloidi sono quelli che ballano un po' tutti insieme, ma magari ogni tanto si spostano un po' dal centro.
Perché è Importante Sapere di Solvente e Soluto?
Ora potresti chiederti: "Ok, carino, ma a che serve tutto questo?". Beh, serve a un sacco di cose, credimi!
- In Cucina: Come abbiamo detto, dallo zucchero nel caffè al sale nella pasta, fino alla preparazione di sciroppi e conserve.
- In Medicina: I farmaci sono spesso disciolti in solventi per essere efficaci. Dalle pillole che si sciolgono in bocca, alle iniezioni, ai colliri.
- Nell'Industria: Dalle vernici, alle colle, ai cosmetici, ai prodotti per la pulizia. Tutto si basa su soluzioni.
- Nella Natura: Il sangue, la linfa delle piante, l'aria che respiriamo (anche se lì è più una miscela di gas, ma il concetto è simile).
Capire questi concetti ti aiuta a capire come funzionano le cose che ti circondano. Ti dà una prospettiva diversa sul mondo. È come avere una chiave per capire un sacco di "come" e "perché".
Un Piccolo Riassunto per Rinfrescarci la Mente
Allora, ricapitolando, in modo super semplice:
- <Soluzione>: È una miscela omogenea (cioè, ben mescolata).
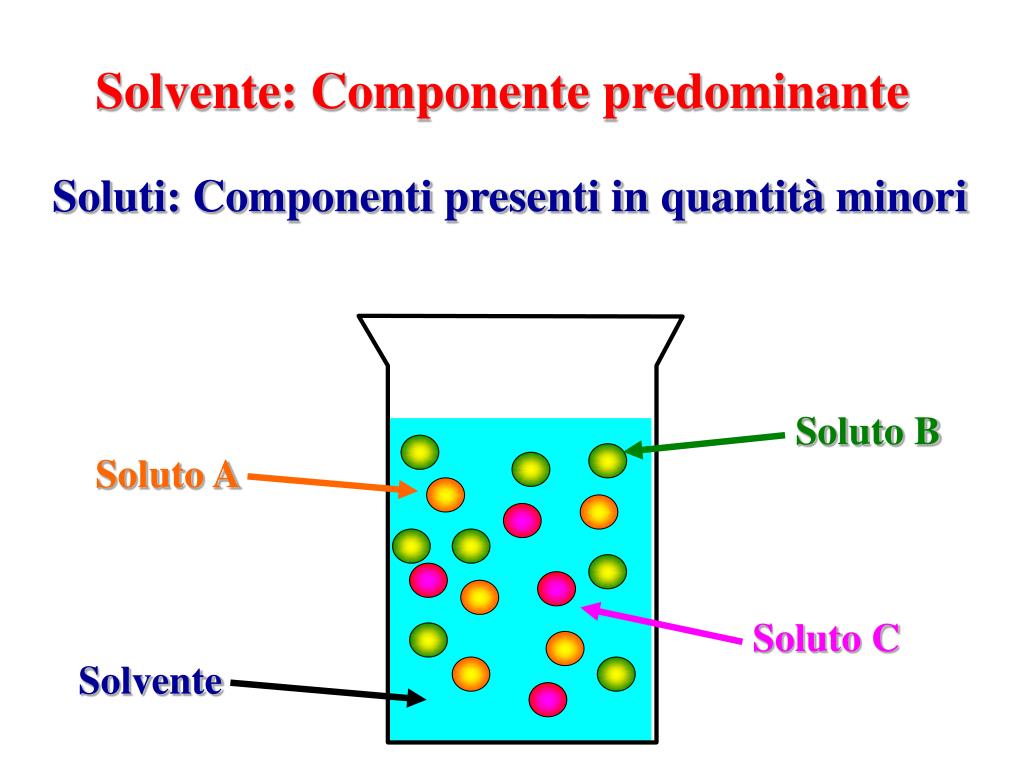
- <Solvente>: È la sostanza che fa da "casa", quella in maggiore quantità, che scioglie l'altra. L'<acqua> è il campione!
- <Soluto>: È la sostanza che viene sciolta nel solvente. Il <zucchero>, il <sale>.
È come se il solvente dicesse al soluto: "Ehi, ti va di fare un giretto insieme? Ti sciolgo un po' e poi vediamo che succede!". E succede un sacco di cose interessanti!
Spero che questa chiacchierata ti sia piaciuta e ti abbia chiarito un po' le idee. Non sono cose così complicate, vero? Sono un po' come i mattoncini LEGO della chimica. Con quelli puoi costruire un sacco di cose fantastiche! Quindi la prossima volta che ti bevi un caffè o prendi una medicina, pensa a questa bella coppia: il solvente e il soluto, che lavorano insieme per rendere la tua vita più dolce, più sana, o semplicemente più semplice. Alla prossima chiacchierata!