
Ciao! So che la configurazione elettronica può sembrare un muro insormontabile all'inizio. Numeri, lettere, frecce... può mandare in confusione! Ma non preoccuparti, siamo qui per affrontarla insieme, passo dopo passo. Ti prometto che con un po' di pazienza e i giusti strumenti, diventerà molto più chiara e gestibile.
I Fondamentali: Numeri Atomici e Orbitali
Prima di tuffarci nella configurazione elettronica vera e propria, ripassiamo due concetti chiave:
- Numero Atomico (Z): Ogni elemento ha un suo numero atomico, che indica il numero di protoni (e, di conseguenza, di elettroni in un atomo neutro) presenti nel nucleo. Lo trovi nella tavola periodica! Ad esempio, l'idrogeno (H) ha Z=1, il che significa che ha un protone e un elettrone.
- Orbitali: Pensa agli orbitali come a delle "caselle" dove gli elettroni possono stare. Ci sono diversi tipi di orbitali, con forme e livelli di energia differenti:
- s: Sferici, possono contenere fino a 2 elettroni.
- p: Hanno una forma a "doppio lobo" e possono contenere fino a 6 elettroni (3 orbitali p per ogni livello energetico).
- d: Più complessi, possono contenere fino a 10 elettroni (5 orbitali d).
- f: Ancora più complessi, possono contenere fino a 14 elettroni (7 orbitali f).
Come Riempire gli Orbitali: La Regola Principale
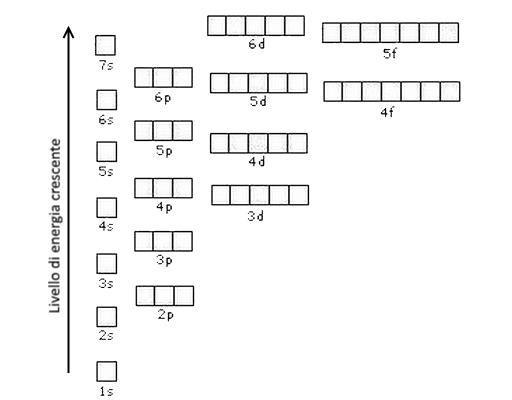
La regola fondamentale è che gli elettroni riempiono gli orbitali partendo da quelli a più bassa energia, salendo poi gradualmente. Immagina di dover riempire un hotel: inizierai dalle camere al primo piano (più economiche) prima di passare a quelle ai piani superiori (più costose).
L'ordine di riempimento degli orbitali è il seguente:
1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p, 5s, 4d, 5p, 6s, 4f, 5d, 6p, 7s, 5f, 6d, 7p
Questo ordine può sembrare difficile da ricordare, ma c'è un trucco! Puoi usare il diagramma di Madelung, una tabella visuale che ti aiuta a seguire la sequenza corretta. Cercalo su Google, ti sarà utilissimo!

Esempi Pratici: Mettiamoci alla Prova
Vediamo alcuni esempi concreti:
- Idrogeno (H, Z=1): Ha un solo elettrone, quindi la sua configurazione elettronica è 1s1.
- Elio (He, Z=2): Ha due elettroni, quindi la sua configurazione elettronica è 1s2.
- Litio (Li, Z=3): Ha tre elettroni. I primi due riempiono l'orbitale 1s, il terzo va nell'orbitale 2s: 1s2 2s1.
- Ossigeno (O, Z=8): Ha otto elettroni: 1s2 2s2 2p4.
Un Trucco per Semplificare
Quando devi scrivere la configurazione elettronica di elementi con tanti elettroni, puoi usare la configurazione abbreviata. Invece di scrivere tutta la sequenza, usi il gas nobile che precede l'elemento nella tavola periodica tra parentesi quadre, e poi scrivi solo la parte restante. Ad esempio:
- Sodio (Na, Z=11): Invece di 1s2 2s2 2p6 3s1, puoi scrivere [Ne] 3s1. (Ne è il simbolo del neon, Z=10)
Consigli Utili e Motivazione
Ricorda:
- Fai tanti esercizi! Più ti eserciti, più diventerà naturale.
- Usa la tavola periodica come guida. Ti fornisce informazioni preziose.
- Non aver paura di chiedere aiuto! Se hai dubbi, parlane con il tuo insegnante o con i tuoi compagni.
La configurazione elettronica può sembrare complessa, ma con impegno e pratica, diventerà uno strumento potentissimo per capire il comportamento degli elementi e delle molecole. Forza, ce la puoi fare! E ricorda, l'importante è non mollare mai!