
Ciao! Se sei qui, probabilmente stai cercando di capire come calcolare la massa atomica relativa. Non preoccuparti, è un argomento che può sembrare complicato all'inizio, ma con un po' di pazienza e le giuste spiegazioni, diventerà tutto molto più chiaro. Molti studenti trovano difficoltà con questo concetto, ma sono sicuro che insieme lo supereremo!
Che cos'è la Massa Atomica Relativa?
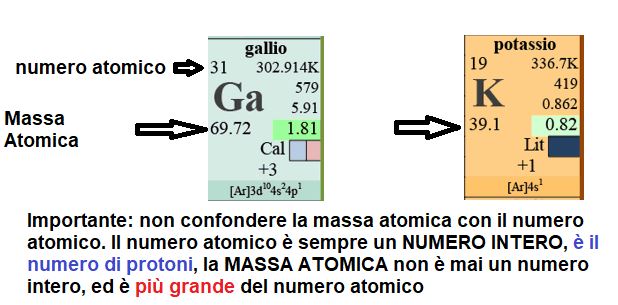
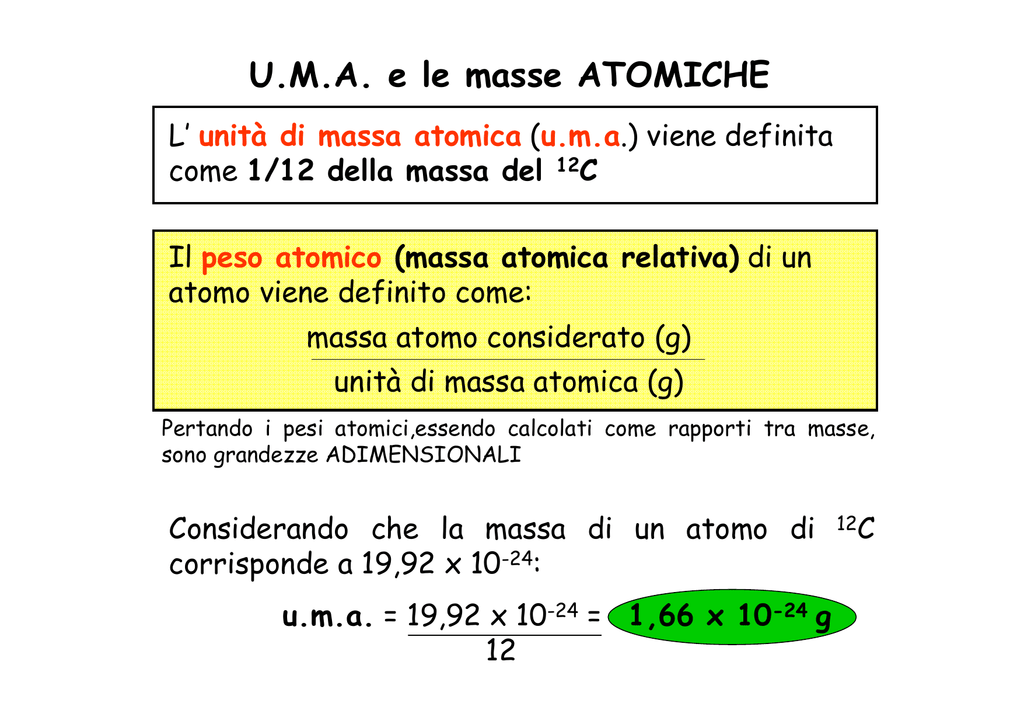
La massa atomica relativa (spesso abbreviata come Ar) è, in parole semplici, un numero che indica quanto pesa, in media, un atomo di un certo elemento rispetto a 1/12 della massa di un atomo di carbonio-12. È una massa "relativa" perché non usiamo grammi o chilogrammi, ma confrontiamo semplicemente il peso dell'atomo con un riferimento standard. Questo riferimento è il carbonio-12, a cui è stata assegnata una massa di esattamente 12 unità di massa atomica (uma).
Immagina di avere una bilancia speciale dove invece di misurare in grammi, misuri quanto un oggetto pesa rispetto a un peso standard. Questo peso standard è il nostro carbonio-12.
Come si Calcola: La Formula Magica
La formula per calcolare la massa atomica relativa è la seguente:
Ar = (Massa isotopo 1 x Abbondanza isotopo 1) + (Massa isotopo 2 x Abbondanza isotopo 2) + ...
Cosa significa tutto questo? Cerchiamo di capirlo passo dopo passo:
Cos'è un Isotopo?
Un isotopo è una variante di un elemento che ha lo stesso numero di protoni, ma un diverso numero di neutroni. Questo significa che gli isotopi di uno stesso elemento hanno masse diverse. Ad esempio, il carbonio ha diversi isotopi, come il carbonio-12, il carbonio-13 e il carbonio-14. Ognuno ha una massa leggermente diversa.
Cos'è l'Abbondanza Isotopica?
L'abbondanza isotopica è la percentuale di ciascun isotopo presente in natura. Ad esempio, il carbonio-12 è molto più abbondante del carbonio-13. Questa abbondanza è espressa come una percentuale o un decimale.
Esempio Pratico: Il Calcio
Calcoliamo la massa atomica relativa del calcio. Supponiamo che il calcio abbia due isotopi principali:
- Calcio-40 (40Ca): Massa = 39.962591 u, Abbondanza = 96.941% (0.96941)
- Calcio-44 (44Ca): Massa = 43.955481 u, Abbondanza = 2.086% (0.02086)
Applichiamo la formula:

Ar(Ca) = (39.962591 u x 0.96941) + (43.955481 u x 0.02086)
Ar(Ca) ≈ 38.74 + 0.92

Ar(Ca) ≈ 39.66 u
Quindi, la massa atomica relativa del calcio è circa 39.66 u. Nota che questo valore è approssimativo perché abbiamo considerato solo due isotopi. Nella realtà, ci sono altri isotopi del calcio, anche se presenti in quantità molto minori.
Consigli Utili e Trucchi
- Presta attenzione alle unità di misura: La massa atomica relativa è un numero adimensionale (senza unità di misura), anche se spesso viene espressa in unità di massa atomica (u).
- Controlla sempre le tabelle periodiche: La massa atomica relativa di un elemento è riportata sulla tavola periodica. Questi valori sono calcolati considerando tutti gli isotopi naturali dell'elemento e le loro abbondanze.
- Non farti spaventare dai decimali: Le masse degli isotopi e le abbondanze isotopiche possono avere molti decimali. Utilizza una calcolatrice per semplificare i calcoli.
- Esercitati: Più esercizi fai, più diventerà naturale il processo di calcolo. Cerca online esercizi sulla massa atomica relativa e mettiti alla prova!
Spero che questa guida ti sia stata utile. Ricorda, la pratica rende perfetti! Non aver paura di fare errori: sono parte del processo di apprendimento. Continua a studiare e a sperimentare, e presto padroneggerai anche questo argomento. In bocca al lupo!