
Avete mai cucinato seguendo una ricetta dove si chiedeva un "pizzico" di sale? Funziona, certo, ma non è il metodo più preciso. In chimica, abbiamo bisogno di misurazioni accurate, soprattutto quando parliamo di soluzioni. Ecco perché è fondamentale capire come calcolare la concentrazione molare, un concetto essenziale per chiunque studi chimica, lavori in laboratorio o si interessi alla preparazione di soluzioni in modo preciso. Questo articolo è rivolto a studenti di chimica, tecnici di laboratorio e a chiunque voglia approfondire le proprie conoscenze sulla preparazione di soluzioni.
Cos'è la Concentrazione Molare?
La concentrazione molare, spesso chiamata molarità, è un modo per esprimere la quantità di una sostanza (il soluto) disciolta in un determinato volume di soluzione. Più precisamente, definisce il numero di moli di soluto presenti in un litro (L) di soluzione. L'unità di misura della molarità è quindi mol/L, che spesso viene abbreviata con la lettera M. Una soluzione 1 M (1 molare) contiene una mole di soluto per ogni litro di soluzione.
Immaginate di preparare un tè. Se mettete troppo tè in poca acqua, il tè sarà molto forte (concentrato). Se mettete poco tè in tanta acqua, sarà debole (diluito). La concentrazione molare ci permette di quantificare esattamente questa "forza" della soluzione.
Perché è Importante la Concentrazione Molare?
La concentrazione molare è cruciale in molte applicazioni, tra cui:
- Reazioni chimiche: Conoscere la concentrazione dei reagenti permette di calcolare i rapporti stechiometrici e prevedere la quantità di prodotto che si otterrà.
- Analisi chimiche: La molarità è fondamentale per effettuare titolazioni, preparare standard e determinare la concentrazione di sostanze sconosciute.
- Biochimica e biologia molecolare: La preparazione di tamponi e soluzioni con concentrazioni precise è essenziale per gli esperimenti.
- Farmacia: La corretta formulazione dei farmaci richiede un'estrema precisione nelle concentrazioni dei principi attivi.
Senza una corretta comprensione e applicazione della concentrazione molare, i risultati degli esperimenti potrebbero essere errati o addirittura pericolosi.
Come si Calcola la Concentrazione Molare: La Formula
Il calcolo della concentrazione molare è relativamente semplice una volta compresi i concetti di base. La formula fondamentale è:
Molarità (M) = Numero di moli di soluto (mol) / Volume della soluzione (L)
Per utilizzare questa formula, abbiamo bisogno di conoscere due cose:

- Il numero di moli del soluto: se non lo conosciamo direttamente, possiamo calcolarlo a partire dalla massa del soluto e dal suo peso molecolare.
- Il volume totale della soluzione, espresso in litri.
Passo 1: Calcolare il Numero di Moli
Se conosciamo la massa del soluto (in grammi) e il suo peso molecolare (PM) (in g/mol), possiamo calcolare il numero di moli utilizzando la seguente formula:
Numero di moli (mol) = Massa del soluto (g) / Peso Molecolare (g/mol)
Il peso molecolare di una sostanza si trova sulla tavola periodica o può essere calcolato sommando i pesi atomici di tutti gli atomi che compongono la molecola.
Esempio: Vogliamo calcolare il numero di moli in 10 grammi di cloruro di sodio (NaCl). Il peso atomico del sodio (Na) è circa 23 g/mol e il peso atomico del cloro (Cl) è circa 35.5 g/mol. Quindi, il peso molecolare di NaCl è 23 + 35.5 = 58.5 g/mol. Il numero di moli sarà quindi 10 g / 58.5 g/mol = 0.171 mol.
Passo 2: Calcolare il Volume della Soluzione
Il volume della soluzione deve essere espresso in litri (L). Se il volume è dato in millilitri (mL), è necessario convertirlo in litri dividendo per 1000:

Volume (L) = Volume (mL) / 1000
Esempio: Se abbiamo 250 mL di soluzione, il volume in litri è 250 mL / 1000 = 0.25 L.
Passo 3: Calcolare la Concentrazione Molare
Una volta calcolati il numero di moli del soluto e il volume della soluzione in litri, possiamo inserire questi valori nella formula della molarità:
Molarità (M) = Numero di moli di soluto (mol) / Volume della soluzione (L)
Esempio: Riprendendo gli esempi precedenti, abbiamo calcolato che 10 g di NaCl corrispondono a 0.171 mol. Se questi 0.171 mol di NaCl sono disciolti in 250 mL (0.25 L) di soluzione, la molarità della soluzione sarà:

M = 0.171 mol / 0.25 L = 0.684 M
Quindi, la concentrazione molare della soluzione è 0.684 M (molare).
Esempi Pratici di Calcolo della Concentrazione Molare
Vediamo alcuni esempi più complessi per consolidare la comprensione:
Esempio 1: Preparazione di una Soluzione di Glucosio
Vogliamo preparare 500 mL di una soluzione di glucosio (C6H12O6) 0.2 M. Quanti grammi di glucosio dobbiamo pesare?
- Calcolare il volume in litri: 500 mL / 1000 = 0.5 L
- Calcolare il numero di moli necessarie: Molarità = moli / Volume => Moli = Molarità * Volume = 0.2 M * 0.5 L = 0.1 mol
- Calcolare il peso molecolare del glucosio: C6H12O6 = (6 * 12) + (12 * 1) + (6 * 16) = 72 + 12 + 96 = 180 g/mol
- Calcolare la massa di glucosio necessaria: Massa = Moli * Peso Molecolare = 0.1 mol * 180 g/mol = 18 g
Quindi, dobbiamo pesare 18 grammi di glucosio e scioglierli in acqua fino a raggiungere un volume finale di 500 mL.
Esempio 2: Diluizione di una Soluzione
Abbiamo 100 mL di una soluzione di acido cloridrico (HCl) 1 M. Vogliamo diluirla a una concentrazione di 0.1 M. Qual è il volume finale della soluzione diluita?
In questo caso, utilizziamo la formula della diluizione: M1V1 = M2V2, dove:
- M1 = Concentrazione iniziale (1 M)
- V1 = Volume iniziale (100 mL = 0.1 L)
- M2 = Concentrazione finale (0.1 M)
- V2 = Volume finale (incognito)
Inserendo i valori nella formula: 1 M * 0.1 L = 0.1 M * V2 => V2 = (1 M * 0.1 L) / 0.1 M = 1 L
Quindi, il volume finale della soluzione diluita dovrà essere di 1 litro. Per fare questo, dobbiamo aggiungere acqua alla soluzione iniziale fino a raggiungere un volume totale di 1 litro. Ciò significa aggiungere 900 mL di acqua (1000 mL - 100 mL = 900 mL).
Consigli Utili per Calcolare la Concentrazione Molare
- Utilizzare sempre le unità di misura corrette: Assicurarsi che il volume sia in litri e la massa sia in grammi.
- Controllare il peso molecolare: Verificare il peso molecolare della sostanza che si sta utilizzando.
- Essere precisi nelle misurazioni: Utilizzare bilance e vetreria volumetriche precise.
- Mescolare bene la soluzione: Assicurarsi che il soluto sia completamente disciolto per ottenere una soluzione omogenea.
- Considerare il volume finale: Quando si preparano soluzioni, aggiungere il soluto al solvente e poi portare a volume con il solvente, invece di aggiungere direttamente il volume desiderato di solvente. Questo perché il volume del soluto può influenzare il volume finale della soluzione.
Errori Comuni da Evitare
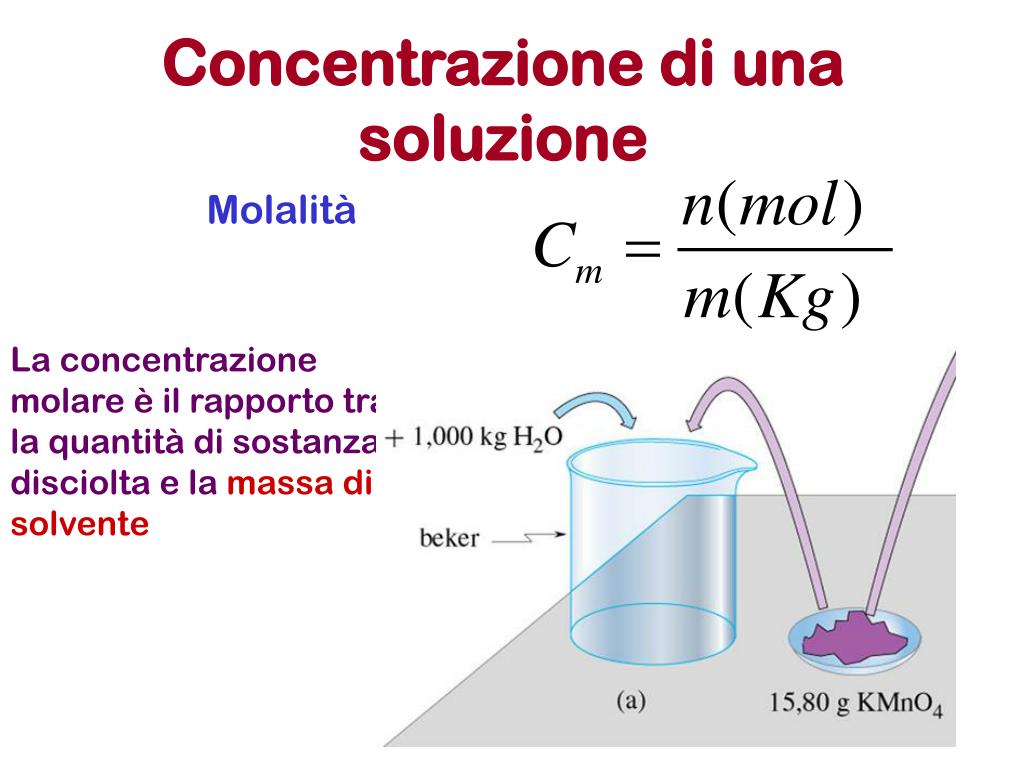
- Confondere molarità con molalità: La molarità (M) è moli di soluto per litro di soluzione, mentre la molalità (m) è moli di soluto per chilogrammo di solvente.
- Utilizzare unità di misura errate: Non convertire i millilitri in litri o i grammi in chilogrammi può portare a errori significativi.
- Non considerare il volume finale: Aggiungere semplicemente un certo volume di solvente invece di portare a volume può causare errori nella concentrazione.
- Non mescolare adeguatamente la soluzione: Una soluzione non omogenea avrà concentrazioni diverse in punti diversi.
Conclusione
La concentrazione molare è uno strumento fondamentale in chimica. Comprendere come calcolarla correttamente è essenziale per preparare soluzioni precise e ottenere risultati accurati nei vostri esperimenti. Speriamo che questa guida vi abbia fornito una solida base per affrontare i vostri futuri calcoli di molarità con sicurezza e precisione. Ricordate, la pratica rende perfetti! Continuate a esercitarvi con diversi esempi e presto sarete in grado di calcolare la concentrazione molare come dei veri professionisti!