Ciao a tutti! Oggi esploriamo un concetto affascinante della chimica: come si calcola il numero di elettroni. Può sembrare complicato all'inizio, ma vi assicuro che con un po' di impegno e disciplina, diventerà un gioco da ragazzi. E, credetemi, la soddisfazione di padroneggiare questo argomento è impagabile!
Partiamo dalle basi. Ogni atomo è composto da un nucleo, contenente protoni (cariche positive) e neutroni (neutri), e da elettroni (cariche negative) che orbitano attorno al nucleo. L'atomo, in condizioni normali, è elettricamente neutro. Questo significa che il numero di protoni è uguale al numero di elettroni. Quindi, per calcolare il numero di elettroni, dobbiamo prima individuare il numero di protoni!
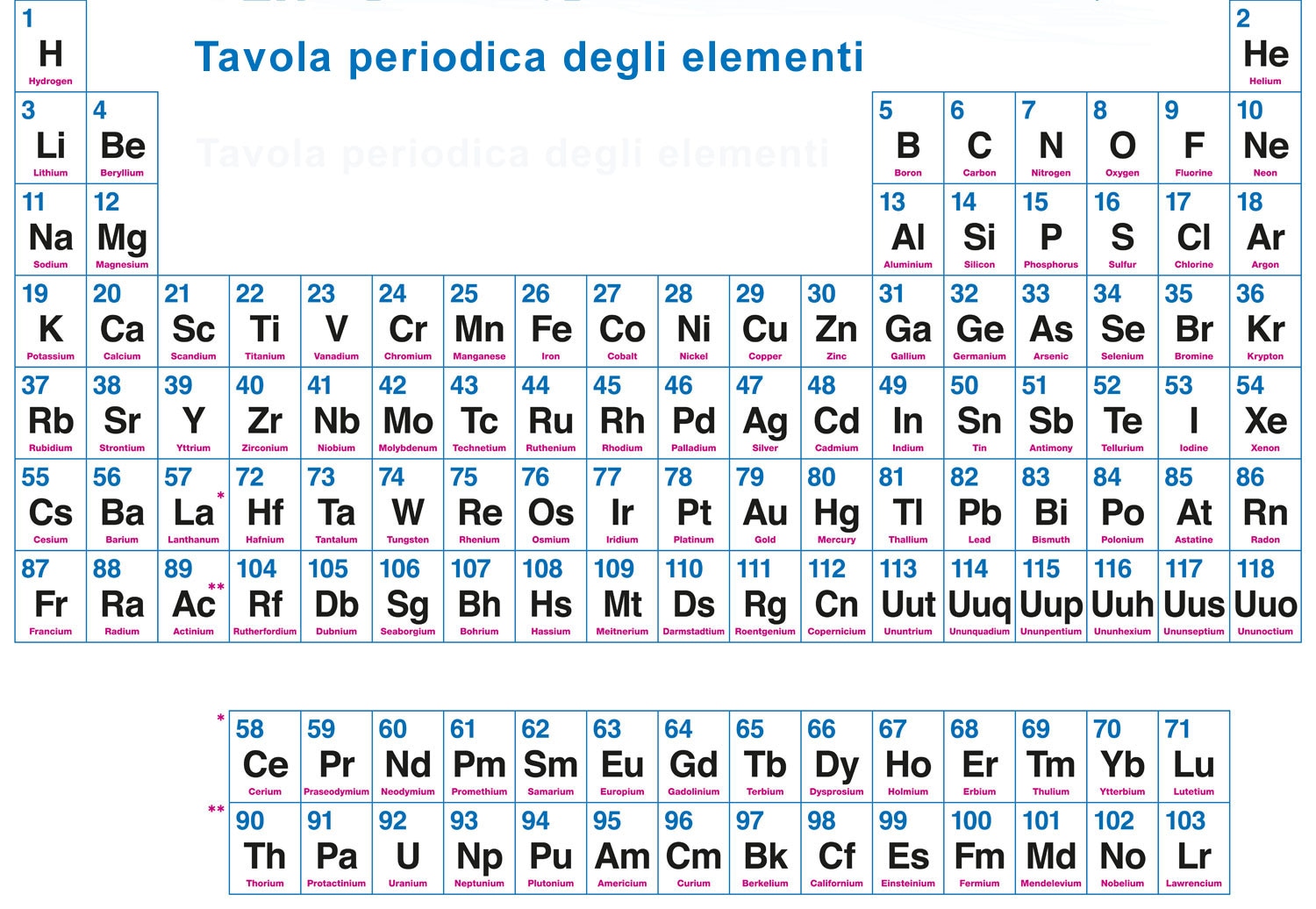
Ma come facciamo a sapere quanti protoni ha un atomo? Ecco che entra in gioco la tavola periodica, la nostra fedele alleata! Ogni elemento nella tavola periodica ha un numero atomico (solitamente indicato con la lettera Z). Questo numero atomico corrisponde esattamente al numero di protoni presenti nel nucleo dell'atomo.
Ad esempio, l'idrogeno (H) ha numero atomico 1. Ciò significa che ha 1 protone nel suo nucleo. Di conseguenza, un atomo di idrogeno neutro ha anche 1 elettrone. L'ossigeno (O) ha numero atomico 8, quindi ha 8 protoni e, di conseguenza, 8 elettroni.
Ioni: Quando Gli Atomi Guadagnano o Perdono Elettroni
Fin qui tutto bene, vero? Ma la chimica è piena di sorprese! Gli atomi non sempre rimangono neutri. A volte, possono guadagnare o perdere elettroni, formando ioni. Se un atomo guadagna elettroni, diventa uno ione negativo, chiamato anione. Se perde elettroni, diventa uno ione positivo, chiamato catione.
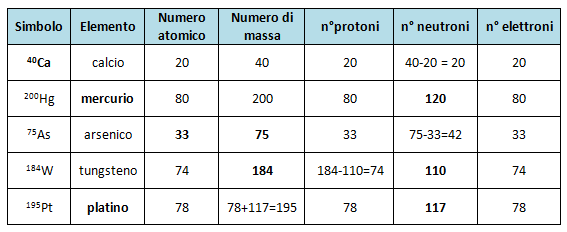
Quindi, come calcoliamo il numero di elettroni in uno ione? È semplice: partiamo dal numero atomico (che ci dà il numero di protoni) e aggiungiamo o sottraiamo il numero di elettroni guadagnati o persi.
Prendiamo l'esempio dello ione cloruro (Cl-). Il cloro (Cl) ha numero atomico 17. Questo significa che un atomo neutro di cloro ha 17 protoni e 17 elettroni. Lo ione cloruro ha una carica negativa, il che significa che ha guadagnato 1 elettrone. Quindi, il numero totale di elettroni nello ione cloruro è 17 + 1 = 18.

Applicazioni Pratiche e Motivazione
Capire come calcolare il numero di elettroni non è solo un esercizio teorico. È fondamentale per comprendere le proprietà chimiche degli elementi e delle molecole, le reazioni chimiche e i legami che tengono insieme la materia. Questo concetto è alla base di molte tecnologie che usiamo ogni giorno, dai pannelli solari alle batterie dei nostri telefoni.
Ma al di là delle applicazioni pratiche, imparare come calcolare il numero di elettroni ci insegna molto sulla disciplina, sulla perseveranza e sulla gioia della scoperta. Richiede di seguire dei passaggi logici, di prestare attenzione ai dettagli e di non arrendersi di fronte alle difficoltà. Sono tutte qualità che ci servono non solo nello studio della chimica, ma anche in ogni aspetto della nostra vita.

Quando vi sentite demotivati a scuola, ricordatevi di questa sfida. Ricordatevi della soddisfazione che proverete quando avrete finalmente compreso un concetto difficile. Ricordatevi che ogni piccolo passo che fate vi avvicina al vostro obiettivo, che sia superare un esame, realizzare un progetto ambizioso o semplicemente diventare persone più consapevoli e capaci.
Allora, cosa aspettate? Prendete la tavola periodica, un quaderno e una penna, e iniziate a esplorare il meraviglioso mondo degli elettroni! Buon lavoro e ricordatevi: l'apprendimento è un viaggio, non una destinazione!