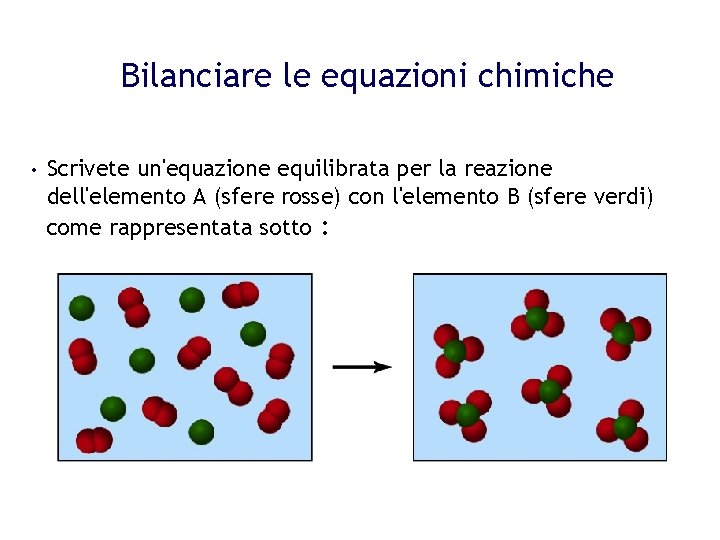
Ti sei mai trovato a fissare un'equazione chimica, sentendoti completamente perso di fronte a quelle lettere e numeri apparentemente casuali? Non sei solo! Bilanciare le reazioni chimiche può sembrare un compito arduo, un vero e proprio rompicapo matematico. Ma la verità è che, con un po' di pazienza e i giusti strumenti, chiunque può padroneggiare quest'abilità fondamentale della chimica.
Questo articolo è pensato proprio per te, che magari ti senti frustrato o intimorito di fronte a questo argomento. Cercheremo di affrontare il problema in modo chiaro, strutturato e pratico, dandoti gli strumenti necessari per bilanciare le reazioni chimiche con successo.
Perché è Importante Bilanciare le Reazioni Chimiche?
Prima di immergerci nel "come", cerchiamo di capire il "perché". Bilanciare le equazioni chimiche non è solo un esercizio di stile chimico; è una necessità, basata su una delle leggi fondamentali della natura: la legge di conservazione della massa. Questa legge, enunciata da Antoine Lavoisier, afferma che la materia non si crea né si distrugge durante una reazione chimica. In altre parole, il numero di atomi di ciascun elemento deve essere lo stesso sia nei reagenti (gli ingredienti della reazione) che nei prodotti (il risultato della reazione).
Immagina di cucinare una torta. Non puoi far sparire magicamente un uovo durante il processo di cottura! Lo stesso vale per gli atomi in una reazione chimica. Un'equazione non bilanciata implicherebbe la creazione o la distruzione di atomi, cosa che, come abbiamo detto, è impossibile secondo la legge di conservazione della massa.
Oltre a rispettare le leggi della fisica, bilanciare le equazioni è fondamentale per:
- Calcolare le quantità di reagenti necessarie per ottenere una determinata quantità di prodotto.
- Prevedere il rendimento teorico di una reazione.
- Comprendere i rapporti stechiometrici tra le diverse specie chimiche coinvolte.
In sostanza, un'equazione bilanciata è una ricetta precisa per una reazione chimica.

Metodi per Bilanciare le Reazioni Chimiche
Esistono diversi metodi per bilanciare le reazioni chimiche, ma ne vedremo due tra i più comuni e intuitivi:
1. Il Metodo dell'Ispezione (o "a tentativi")
Questo è il metodo più semplice, spesso il primo che si impara. Consiste nell'aggiungere coefficienti stechiometrici (numeri interi) davanti alle formule chimiche dei reagenti e dei prodotti, fino a quando il numero di atomi di ciascun elemento non è uguale su entrambi i lati dell'equazione. Richiede un po' di pratica e una buona dose di pazienza, ma è efficace per reazioni relativamente semplici.
Ecco i passaggi chiave:
- Identifica gli elementi presenti nell'equazione.
- Conta il numero di atomi di ciascun elemento su entrambi i lati dell'equazione.
- Inizia bilanciando gli elementi che compaiono in un solo reagente e in un solo prodotto. Questo semplifica il processo.
- Modifica i coefficienti stechiometrici per bilanciare gli elementi uno alla volta. Ricorda che cambiare un coefficiente può influenzare il numero di atomi di più elementi, quindi procedi con cautela.
- Verifica che il numero di atomi di ciascun elemento sia lo stesso su entrambi i lati dell'equazione. Se non lo è, ripeti i passaggi precedenti.
- Semplifica i coefficienti, se possibile, dividendo tutti i coefficienti per il loro massimo comun divisore.
Esempio pratico: Bilanciamo la reazione di combustione del metano (CH4) con l'ossigeno (O2) per formare anidride carbonica (CO2) e acqua (H2O).

L'equazione non bilanciata è:
CH4 + O2 → CO2 + H2O
- Identificazione elementi: Carbonio (C), Idrogeno (H), Ossigeno (O).
- Conteggio atomi (non bilanciato):
- C: 1 (sinistra), 1 (destra)
- H: 4 (sinistra), 2 (destra)
- O: 2 (sinistra), 3 (destra)
- Bilanciamento dell'idrogeno: Per bilanciare l'idrogeno, mettiamo un coefficiente 2 davanti all'acqua (H2O): CH4 + O2 → CO2 + 2H2O
- Bilanciamento dell'ossigeno: Ora abbiamo 4 atomi di ossigeno a destra (2 dalla CO2 e 2 dall'H2O). Per bilanciare l'ossigeno, mettiamo un coefficiente 2 davanti all'ossigeno (O2) a sinistra: CH4 + 2O2 → CO2 + 2H2O
- Verifica:
- C: 1 (sinistra), 1 (destra)
- H: 4 (sinistra), 4 (destra)
- O: 4 (sinistra), 4 (destra)
- Semplificazione: In questo caso, i coefficienti non possono essere ulteriormente semplificati.
L'equazione bilanciata è:

CH4 + 2O2 → CO2 + 2H2O
2. Il Metodo Algebrico
Questo metodo, leggermente più complesso, è particolarmente utile per reazioni più complicate. Invece di procedere per tentativi, si assegnano variabili algebriche (ad esempio, a, b, c, d) ai coefficienti stechiometrici, si impostano equazioni matematiche basate sul numero di atomi di ciascun elemento e si risolve il sistema di equazioni.
Ecco i passaggi chiave:
- Assegna variabili algebriche ai coefficienti stechiometrici di ciascuna specie chimica nell'equazione.
- Scrivi un'equazione algebrica per ciascun elemento presente nell'equazione chimica, uguagliando il numero di atomi di quell'elemento sui due lati dell'equazione.
- Risolvi il sistema di equazioni algebriche. In genere, si assume un valore (spesso 1) per una delle variabili e si risolvono le altre in termini di quella variabile.
- Moltiplica tutti i coefficienti per un fattore tale da ottenere numeri interi.
- Verifica che l'equazione sia bilanciata.
Esempio pratico: Bilanciamo la seguente reazione:

KMnO4 + HCl → KCl + MnCl2 + H2O + Cl2
- Assegna variabili: aKMnO4 + bHCl → cKCl + dMnCl2 + eH2O + fCl2
- Scrivi equazioni:
- K: a = c
- Mn: a = d
- O: 4a = e
- H: b = 2e
- Cl: b = c + 2d + 2f
- Risolvi: Assumiamo a = 1. Quindi c = 1 e d = 1. Da 4a = e, otteniamo e = 4. Da b = 2e, otteniamo b = 8. Infine, da b = c + 2d + 2f, otteniamo 8 = 1 + 2 + 2f, quindi f = 2.5.
- Moltiplica: Moltiplichiamo tutti i coefficienti per 2 per ottenere numeri interi: a = 2, b = 16, c = 2, d = 2, e = 8, f = 5.
- Verifica: L'equazione bilanciata è: 2KMnO4 + 16HCl → 2KCl + 2MnCl2 + 8H2O + 5Cl2
Consigli e Trucchi
Bilanciare le reazioni chimiche richiede pratica. Ecco alcuni consigli che possono aiutarti:
- Inizia con reazioni semplici. Non cercare di affrontare subito le reazioni più complesse.
- Bilancia gli elementi che compaiono in un solo reagente e in un solo prodotto per primi. Questo semplifica il processo.
- Considera i gruppi poliatomici (come SO42- o NO3-) come un'unica entità, se rimangono invariati durante la reazione.
- Non aver paura di fare errori! L'importante è imparare dai propri errori.
- Usa le risorse online. Esistono molti siti web e app che possono aiutarti a bilanciare le reazioni chimiche.
- Sii paziente. Bilanciare le reazioni chimiche può richiedere tempo, soprattutto all'inizio. Non scoraggiarti!
Ricorda che la pratica rende perfetti. Più bilanci reazioni, più diventerai bravo e più facile ti sembrerà questo compito.
Conclusione
Bilanciare le reazioni chimiche è un'abilità essenziale per chiunque studi chimica. Comprendendo i principi alla base di questo processo e utilizzando i metodi e i consigli che abbiamo discusso, sarai in grado di affrontare con successo anche le reazioni più complesse. Non aver paura di sperimentare, fare errori e imparare dai tuoi sbagli. Con un po' di pazienza e perseveranza, diventerai un maestro nel bilanciare le reazioni chimiche!