
Ciao! Capisco perfettamente. La chimica può sembrare un labirinto di concetti astratti, soprattutto quando si parla di molecole polari e apolari. Ma non preoccuparti! Non sei solo e, soprattutto, non è così difficile come sembra. In questa guida, ti accompagnerò passo dopo passo, usando un linguaggio semplice e tanti esempi pratici, per aiutarti a distinguere queste due tipologie di molecole. L'obiettivo? Renderla una passeggiata, anche se la chimica non è il tuo forte!
Perché è importante capire la polarità delle molecole?
Prima di tuffarci nel vivo dell'argomento, chiariamo perché dovresti preoccuparti di distinguere molecole polari e apolari. La polarità influenza tantissime proprietà delle sostanze, come:
* Solubilità: "Il simile scioglie il simile". Le molecole polari tendono a sciogliersi in solventi polari (come l'acqua), mentre le molecole apolari si sciolgono in solventi apolari (come l'olio). * Punto di ebollizione: Le molecole polari, avendo forze di attrazione intermolecolari più forti, hanno punti di ebollizione più alti rispetto alle apolari. * Tensione superficiale: Anche in questo caso, la polarità gioca un ruolo chiave. * Reattività chimica: La polarità di una molecola può influenzare la sua capacità di reagire con altre sostanze.In sostanza, capire la polarità ti permette di prevedere il comportamento di una sostanza in diverse situazioni. Come dice spesso la Prof.ssa Rossi, insegnante di chimica di lunga data: "Comprendere la polarità è come avere la chiave per sbloccare i segreti del mondo molecolare!"
Cos'è l'elettronegatività? La chiave per capire la polarità
Per capire se una molecola è polare o apolare, dobbiamo prima introdurre il concetto di elettronegatività. Immagina che gli atomi in una molecola stiano "tirando la fune" per accaparrarsi gli elettroni condivisi nel legame chimico. L'elettronegatività è la misura di quanto forte un atomo "tira" questi elettroni.
Ogni elemento ha un valore di elettronegatività (generalmente compreso tra 0 e 4). Più alto è il valore, più forte è l'attrazione per gli elettroni. L'ossigeno, ad esempio, è molto elettronegativo, mentre il sodio è poco elettronegativo.
Come usare l'elettronegatività per prevedere la polarità di un legame?
La differenza di elettronegatività tra due atomi legati ci dice se il legame è polare o apolare:

Esercizio: Prova a consultare una tavola periodica con i valori di elettronegatività e calcola la differenza di elettronegatività per i seguenti legami: C-H, N-H, C-O.
Molecole polari vs. Molecole apolari: La differenza chiave
Ora che abbiamo capito cos'è l'elettronegatività e come influenza i legami, possiamo finalmente distinguere le molecole polari e apolari.
Molecole polari: Un'attrazione asimmetrica
Una molecola è polare se:
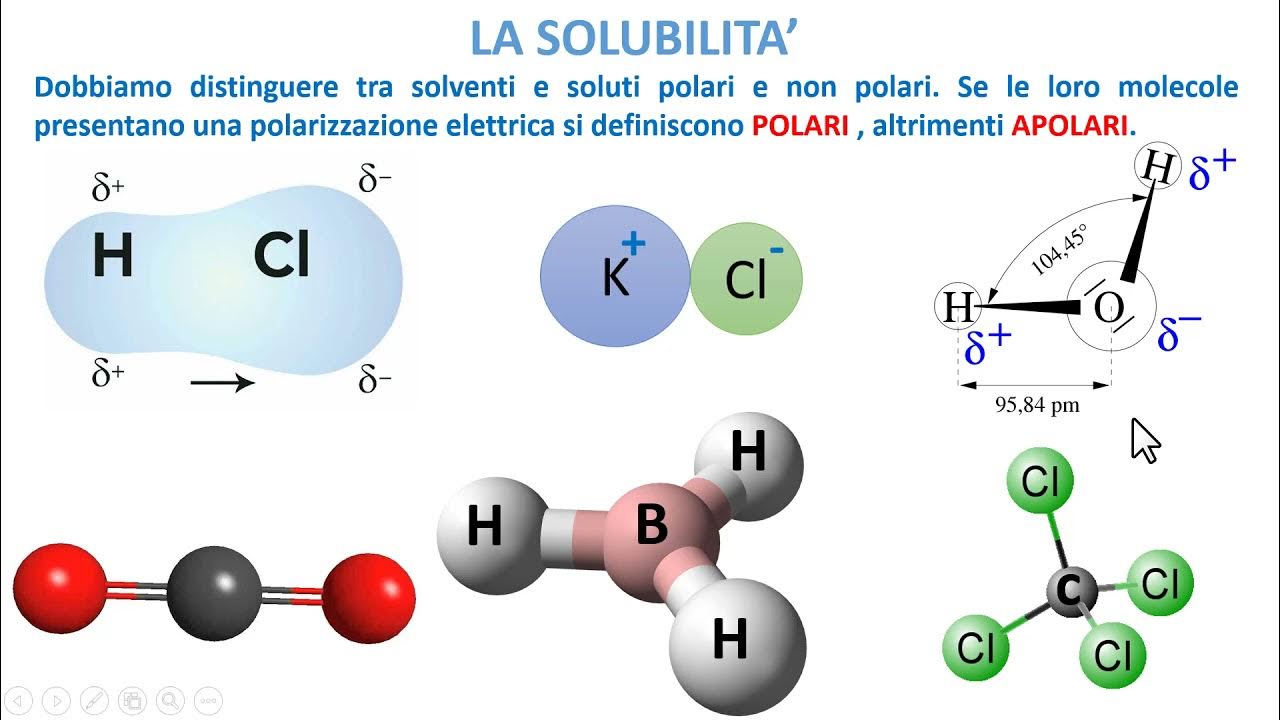
* Contiene legami polari, e * La sua forma fa sì che la distribuzione delle cariche positive e negative non sia simmetrica. In altre parole, c'è una "zona" della molecola leggermente più positiva e un'altra leggermente più negativa.Un ottimo esempio è l'acqua (H2O). Il legame O-H è polare perché l'ossigeno è molto più elettronegativo dell'idrogeno. Inoltre, la forma "piegata" della molecola fa sì che gli elettroni si concentrino attorno all'ossigeno, rendendo quella zona leggermente negativa e le zone attorno agli idrogeni leggermente positive.
Un altro esempio è l'ammoniaca (NH3). Anche qui, i legami N-H sono polari e la forma piramidale della molecola crea una distribuzione asimmetrica delle cariche.
Molecole apolari: Un'armonia di cariche
Una molecola è apolare se:
* Contiene solo legami apolari, oppure * Contiene legami polari, ma la sua forma fa sì che la distribuzione delle cariche sia simmetrica, annullando gli effetti della polarità dei singoli legami.Esempi di molecole apolari sono l'idrogeno (H2), l'ossigeno (O2) e il metano (CH4). Nel metano, i legami C-H sono leggermente polari, ma la forma tetraedrica della molecola fa sì che le cariche si annullino a vicenda, rendendo la molecola apolare.

Attenzione! Una molecola con legami polari può essere apolare se la sua geometria fa sì che i dipoli si cancellino. È fondamentale considerare sia la polarità dei legami che la forma della molecola.
Come prevedere la polarità di una molecola: Un approccio passo-passo
Ecco un metodo semplice e pratico per prevedere la polarità di una molecola:
- Disegna la struttura di Lewis: Questo ti aiuterà a visualizzare i legami e la disposizione degli atomi.
- Determina la polarità dei legami: Calcola la differenza di elettronegatività per ogni legame e stabilisci se è polare o apolare.
- Considera la geometria molecolare: Usa la teoria VSEPR (Valence Shell Electron Pair Repulsion) per prevedere la forma della molecola.
- Valuta la simmetria della distribuzione delle cariche: Se la molecola è simmetrica e i legami polari si annullano, la molecola è apolare. Se la molecola è asimmetrica e c'è una separazione netta di carica, la molecola è polare.
Consiglio di un tutor: "Non aver paura di disegnare! Visualizzare la molecola in 3D è fondamentale per capire la distribuzione delle cariche."
Esercizi pratici per mettere alla prova le tue conoscenze
Ora è il momento di mettere in pratica quello che hai imparato! Prova a determinare la polarità delle seguenti molecole, seguendo i passaggi descritti sopra:

Soluzioni (non sbirciare subito!): CO2 (apolare), CHCl3 (polare), CCl4 (apolare), HF (polare).
Polarità nella vita di tutti i giorni: Esempi concreti
La polarità non è solo un concetto astratto relegato ai libri di testo. Influenza tantissime cose che ci circondano!
* Detersivi: I detersivi contengono molecole con una parte polare (che si lega all'acqua) e una parte apolare (che si lega al grasso). Questo permette di rimuovere lo sporco dai tessuti. * Cottura: L'olio (apolare) e l'acqua (polare) non si mescolano. Per questo motivo, per emulsionare salse come la maionese, è necessario un emulsionante (come il tuorlo d'uovo), che contiene molecole sia polari che apolari. * Farmaci: La polarità di un farmaco influenza la sua capacità di essere assorbito dall'organismo e di raggiungere il suo bersaglio.Non arrenderti! Continua a esercitarti e a chiedere aiuto
Distinguere molecole polari e apolari all'inizio può sembrare complicato, ma con la pratica diventerà sempre più facile. Non aver paura di chiedere aiuto al tuo insegnante, ai tuoi compagni o a un tutor. Ci sono tantissime risorse online (video, esercizi, simulazioni) che possono aiutarti a comprendere meglio questo concetto.
Ricorda: la chimica è come un puzzle. Ogni pezzo, per quanto piccolo, è fondamentale per completare il quadro generale. E tu hai tutte le carte in regola per risolvere questo puzzle!