
Ciao a tutti! Avete presente quelle volte in cui un argomento sembra un muro insormontabile? La chimica, a volte, può dare questa impressione. Ma non temete! Oggi, parleremo di un concetto fondamentale, ma accessibile: come capire se un acido è forte o debole. Sembra difficile, ma con un po' di impegno e disciplina, diventerà tutto più chiaro.
Immaginate la chimica come un grande puzzle. Ogni pezzo, ogni concetto, si incastra con gli altri, formando un quadro più ampio. Comprendere la forza degli acidi è un pezzo importante di questo puzzle. E la cosa bella è che, una volta capito, vi aiuterà a comprendere meglio tante altre cose!
Il Segreto della Forza Acida: Ionizzazione
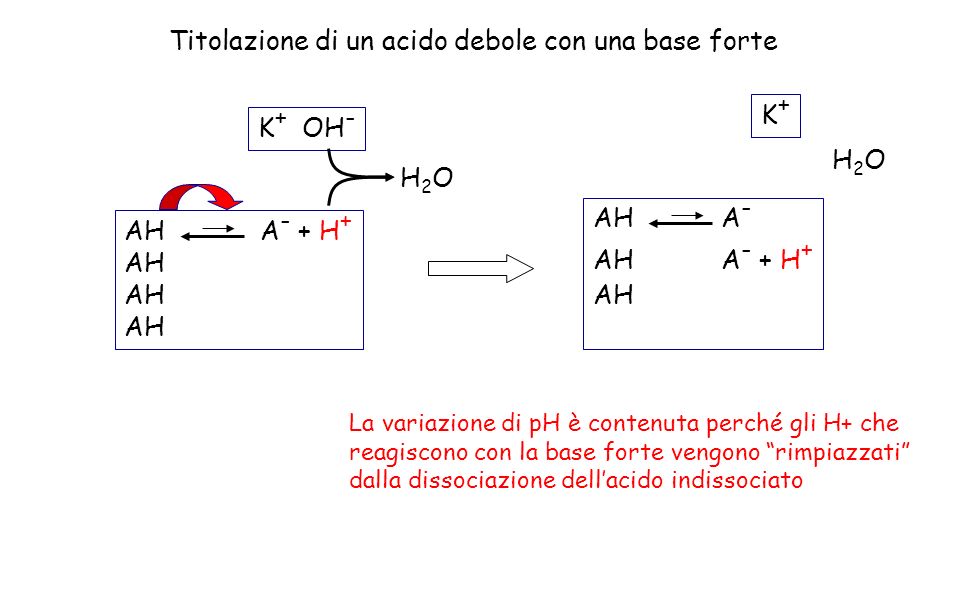
La chiave per capire se un acido è forte o debole sta nella sua capacità di ionizzarsi in acqua. Cosa significa? Immaginate un acido come una squadra di calcio. Quando un acido forte entra in acqua, si "scioglie" completamente, come se tutti i giocatori della squadra si separassero e corressero in direzioni diverse. Praticamente, si trasforma quasi completamente nei suoi ioni costituenti. Un esempio classico è l'acido cloridrico (HCl), che si trasforma in ioni idronio (H3O+) e ioni cloruro (Cl-).
Al contrario, un acido debole è come una squadra di calcio molto unita. Quando entra in acqua, solo alcuni giocatori si separano, mentre la maggior parte rimane insieme. In altre parole, si ionizza solo parzialmente. Un esempio comune è l'acido acetico (CH3COOH), presente nell'aceto. Solo una piccola parte si trasforma in ioni acetato (CH3COO-) e ioni idronio (H3O+).
Come Riconoscere gli Acidi Forti
Esistono alcuni acidi che sono considerati forti "di default". Imparare a riconoscerli è un ottimo punto di partenza. Ecco alcuni dei più comuni:
- Acido cloridrico (HCl)
- Acido bromidrico (HBr)
- Acido iodidrico (HI)
- Acido solforico (H2SO4)
- Acido nitrico (HNO3)
- Acido perclorico (HClO4)
Ricordate: questi acidi si ionizzano quasi completamente in acqua. Conoscere questa lista vi darà un vantaggio significativo!
Il Ruolo della Costante di Acidità (Ka)
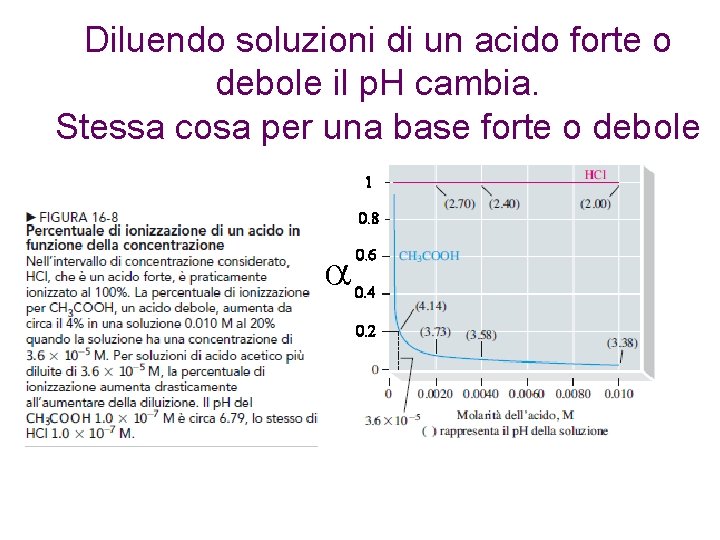
Per essere ancora più precisi, esiste un valore numerico chiamato costante di acidità (Ka) che quantifica la forza di un acido. Più alto è il valore di Ka, più forte è l'acido. Gli acidi forti hanno valori di Ka molto alti, mentre gli acidi deboli hanno valori molto bassi. Spesso, invece di Ka, si usa il valore pKa, che è il logaritmo negativo di Ka (pKa = -log Ka). Un valore di pKa basso indica un acido forte.

"La conoscenza è potere." - Francis Bacon
Questa frase è particolarmente vera quando si tratta di chimica. Più capite i concetti, più sarete in grado di affrontare problemi complessi.
Cosa Imparare da Tutto Questo?
Capire la differenza tra acidi forti e deboli non serve solo a superare un compito in classe. Ci insegna l'importanza della disciplina nello studio, la necessità di approfondire i concetti e non fermarsi alla superficie. Inoltre, ci mostra come un piccolo sforzo iniziale (imparare la lista degli acidi forti) può portare a grandi risultati.
Quando vi sentite demotivati, ricordate che ogni piccolo passo avanti è una vittoria. Come disse Marie Curie, una pioniera della scienza: "Non si deve temere nulla nella vita, si deve solo capire." E capire significa impegnarsi, studiare e non arrendersi di fronte alle difficoltà.
Applicate questo approccio non solo alla chimica, ma a tutte le materie. Ponetevi degli obiettivi, studiate con metodo e non abbiate paura di chiedere aiuto. La scuola è un'opportunità unica per crescere e imparare, e sta a voi sfruttarla al meglio!