Allora, gente, mettetevi comodi, prendete il vostro caffè (o un Aperol Spritz, non giudico!) perché oggi parliamo di una roba che suona complicata, ma che in realtà è tipo... la festa di compleanno di un atomo. Stiamo per esplorare "Che Cos'è L'Energia Di Prima Ionizzazione". Sì, lo so, il nome fa venire in mente formule chimiche che sembrano geroglifici egizi e professori che parlano con la voce di un robot annoiato. Ma fidatevi, è più divertente di così. È come scoprire il segreto per far scappare un palloncino da una stanza chiusa ermeticamente.
Immaginatevi gli atomi come dei piccoli, minuscoli pacchetti di energia. Sono pieni di roba: protoni, neutroni (dentro il nucleo, come il nocciolo di una pesca) e poi ci sono gli elettroni, che sono tipo i festaioli, che svolazzano intorno al nucleo come se fossero appena arrivati alla festa e fossero pronti a fare casino. Questi elettroni sono tenuti lì da una forza misteriosa, un po' come quella che ci tiene attaccati al divano un sabato pomeriggio. È l'attrazione tra il nucleo positivo e gli elettroni negativi.
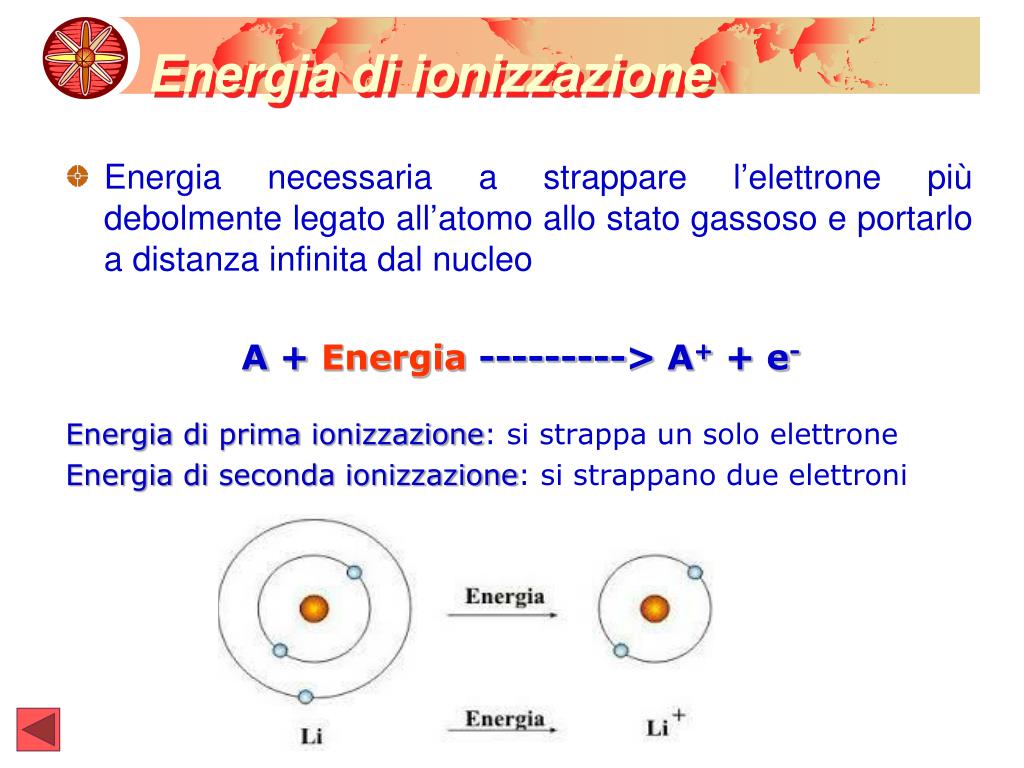
Ora, l'Energia di Prima Ionizzazione è, in soldoni, la quantità di energia che devi dare a un atomo per convincere uno di questi festaioli elettronici a mollare tutto e andarsene. Sì, avete capito bene. È come dire all'elettrone: "Hey amico, la festa è finita, prendi i tuoi popcorn e sparisci!". Solo che non gli dai un sacchetto di popcorn, gli dai dell'energia. Un po' come quando devi convincere un bambino a smettere di giocare con quel giocattolo che gli piace tanto: ci vuole una piccola "negoziazione" energetica.
Ma perché dovremmo voler far scappare un elettrone?
Ottima domanda! Non è che lo facciamo per cattiveria. La chimica è piena di gente che vuole scambiare, donare o prendere elettroni. È il modo in cui gli atomi fanno amicizia (o a volte litigano ferocemente) e creano tutte le cose meravigliose e terribili che ci circondano. Tipo l'acqua che beviamo, l'aria che respiriamo, e anche quel biscotto che state per addentare.
Pensatela così: gli atomi amano essere felici e stabili. E per essere felici, spesso cercano di avere un certo numero di elettroni che girano intorno, come se fossero un gruppo di amici ben assortito. Se un atomo ha un elettrone "in più", o uno "in meno" rispetto a quello che lo farebbe sentire al top, beh, cercherà di rimediare. L'energia di ionizzazione è il prezzo da pagare per farlo cambiare stato, per farlo diventare uno ione (cioè, un atomo con una carica elettrica, perché ha perso o guadagnato elettroni).

Più è difficile convincere un elettrone ad andarsene, più alta sarà l'energia di prima ionizzazione. È come provare a strappare un gelato a un bambino: più è attaccato, più energia ci vuole! Alcuni atomi sono tipo delle mamme affettuose con i loro elettroni, li tengono stretti stretti. Altri, invece, sono più tipo il nonno che dice "Dai, vai a giocare fuori!".
Cosa rende un elettrone più "appiccicoso"?
Qui entra in gioco la magia della tavola periodica. Ci sono un paio di fattori chiave. Primo, la distanza dal nucleo. Immaginate il nucleo come il capo della discoteca. Più gli elettroni sono vicini, più sentono la sua "presenza" e più è difficile farli allontanare. Un elettrone che è lontanissimo è tipo uno che è già sulla porta, pronto per andare a casa.
Secondo, la carica del nucleo. Più protoni ci sono nel nucleo, più è forte l'attrazione su tutti gli elettroni. È come avere un capo più autorevole: tutti stanno più attenti. Quindi, atomi con molti protoni tendono a tenere gli elettroni più stretti, e hanno un'energia di ionizzazione più alta.

E poi c'è un fattore che sembra una cosa da nerd, ma è fondamentale: la schermatura. Gli elettroni interni, quelli più vicini al nucleo, fanno un po' da "scudo" per quelli esterni. È come se gli elettroni interni dicessero agli elettroni esterni: "Tranquilli, il capo non vi vede bene, potete fare un po' i vostri comodi". Questo rende più facile far scappare gli elettroni esterni. È un po' come il gioco del "nascondino": più ostacoli ci sono, più facile è scappare.
Guardiamo la Tavola Periodica: la mappa del tesoro!
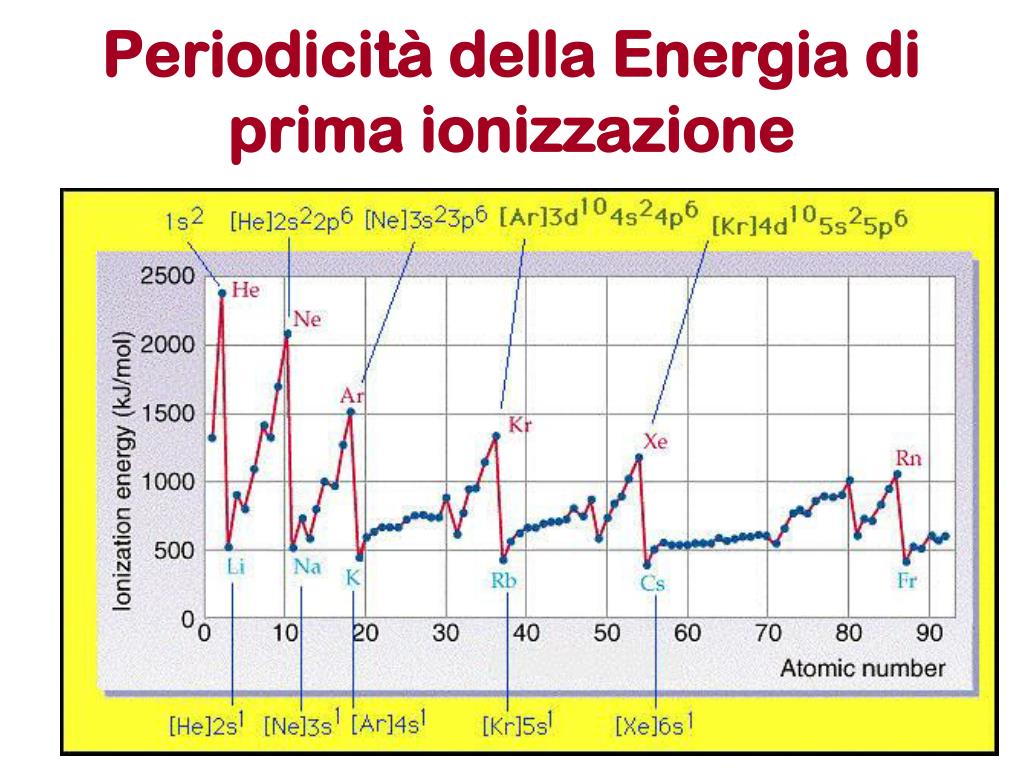
Se prendete in mano una tavola periodica (quella che vi faceva venire l'ansia a scuola, ricordate? Beh, ora è la vostra migliore amica!), noterete delle tendenze sorprendenti. Andando da sinistra verso destra, nella stessa riga (periodo), l'energia di prima ionizzazione generalmente aumenta. Perché? Perché il numero di protoni nel nucleo aumenta, rendendo l'attrazione più forte. È come andare da un gruppo di amici che chiacchierano a un gruppo di tifosi urlanti: l'intensità cresce!
E invece andando dall'alto verso il basso, nella stessa colonna (gruppo)? L'energia di prima ionizzazione generalmente diminuisce. Ah! Questo è perché gli elettroni più esterni sono più lontani dal nucleo. Sono in "piani" energetici più alti, e quindi più facili da staccare. È come se fossero su un trampolino da cui è più facile saltare via. Gli atomi in fondo alla tavola sono tipo i nonni che, ormai stanchi, lasciano andare i nipoti a giocare senza troppi problemi.
Pensate agli elementi sulla sinistra, come il Cesio o il Francio. Sono degli atomi super generosi, o forse un po' svogliati, che danno via il loro elettrone esterno con una facilità disarmante. L'energia di prima ionizzazione per loro è bassissima. È come chiedere a qualcuno se vuole un sacchetto di patatine: "Sì, certo, prendile pure!".
Dall'altra parte, sulla destra, abbiamo i gas nobili (come l'Elio, il Neon, l'Argon). Questi sono i tipi che stanno benissimo da soli, non hanno nessuna voglia di fare scambi. Hanno già il loro "set" perfetto di elettroni, sono come i guru dell'auto-sufficienza. Per farli perdere un elettrone, devi praticamente offrirgli un intero tesoro. La loro energia di prima ionizzazione è altissima. Sono quelli che ti dicono: "Grazie, ma sto benissimo così!".

Un fatto sorprendente (e un po' inquietante!)
Sapevate che la prima energia di ionizzazione più alta in assoluto appartiene all'Elio? Questo gas leggerissimo e quasi inerte richiede una quantità pazzesca di energia per strappargli via un elettrone. È così "felice" nella sua configurazione che resistere a questa energia è come cercare di svuotare il mare con un cucchiaino. Un'impresa quasi impossibile!
E poi c'è un'eccezione interessante. Nell'ossigeno, ad esempio, la seconda energia di ionizzazione è sorprendentemente più bassa della terza. Questo perché dopo aver tolto un elettrone, gli elettroni rimanenti sono un po' più vicini e "sentono" di più il nucleo positivo. Ma quando si tratta di toglierne un altro, la storia cambia leggermente a causa delle configurazioni elettroniche che si creano. È come quando hai un gruppo di amici e uno se ne va: gli altri si stringono un po', ma forse il prossimo che se ne va lo fa per motivi diversi. La chimica è piena di queste piccole "sorprese" che rendono tutto meno prevedibile e più affascinante.
Quindi, la prossima volta che sentite parlare di "Energia di Prima Ionizzazione", non immaginate formule incomprensibili. Pensate a un atomo, a un festaiolo elettronico che viene invitato a lasciare la festa. E pensate a quanta "spinta" (energia) serve per farlo. È una misura di quanto un atomo ama (o odia!) i suoi elettroni, e quanto è difficile convincerlo a cambiare idea. È un po' come la nostra vita sociale, no? A volte è facile fare nuove amicizie, altre volte ci vuole un sacco di coraggio e di energia per rompere il ghiaccio. Solo che qui stiamo parlando di roba che compone tutto l'universo. Abbastanza fico, no?