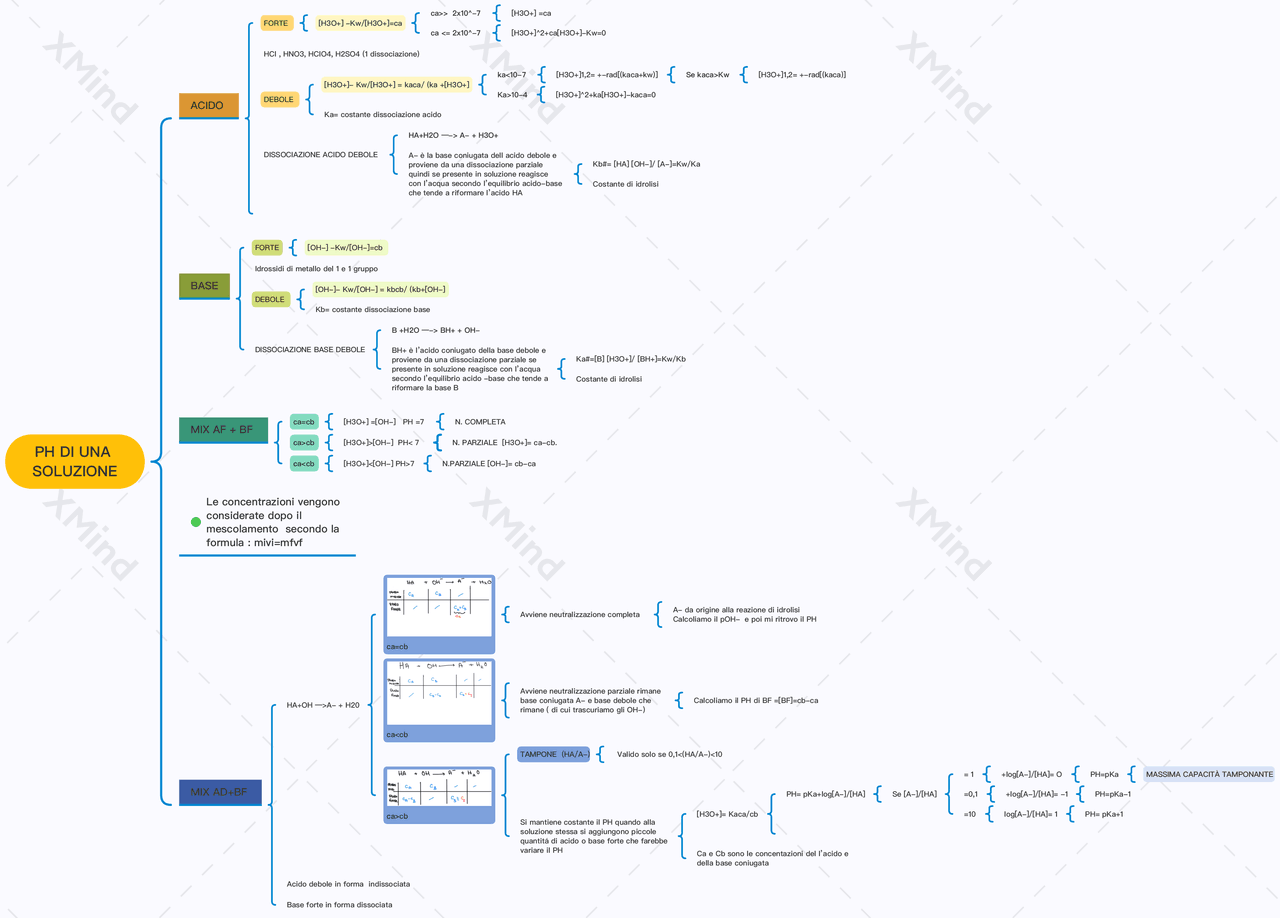
Sapete quanto sia fondamentale comprendere il pH di una soluzione per una vasta gamma di applicazioni, dalla chimica di base alla biologia, passando per l'industria e persino la cura della persona? Oggi ci immergeremo in un argomento specifico ma incredibilmente utile: il calcolo del pH di una soluzione di idrossido di calcio, noto anche come calce spenta. Se vi siete mai trovati di fronte a questo composto, o se semplicemente siete curiosi di capire come la sua natura basica influenzi l'ambiente circostante, questo articolo è pensato per voi.
Il nostro obiettivo è rendere questo calcolo chiaro e accessibile, anche se non siete chimici professionisti. Demistificheremo i concetti chiave, forniremo formule essenziali e, soprattutto, vi guideremo passo dopo passo nel processo. Che siate studenti che studiano chimica, professionisti che lavorano con materiali alcalini, o semplicemente appassionati di scienza, vi offriremo gli strumenti per affrontare questo calcolo con sicurezza e competenza.
Capire l'Idrossido di Calcio: Una Base Forte
Prima di addentrarci nei calcoli, è cruciale capire cos'è l'idrossido di calcio (Ca(OH)₂) e perché il suo pH è così rilevante. L'idrossido di calcio è un composto chimico basico, ovvero una base inorganica. Si ottiene dalla reazione dell'ossido di calcio (calce viva) con l'acqua, un processo noto come "spegnimento della calce". La sua caratteristica principale, dal punto di vista del pH, è la sua capacità di liberare ioni idrossido (OH⁻) in soluzione acquosa. Questi ioni sono proprio ciò che conferisce alla soluzione la sua natura alcalina.
La sua solubilità in acqua non è elevatissima, ma è sufficiente per creare soluzioni con un pH significativamente alcalino. Pensate all'idrossido di calcio nel contesto della vita quotidiana: viene usato nell'edilizia (malte e intonaci), nel trattamento delle acque per neutralizzare l'acidità, nell'industria alimentare come additivo (ad esempio, per la preparazione della masa harina per le tortillas), e persino in agricoltura per correggere l'acidità del suolo. In tutti questi scenari, il controllo del pH è cruciale per l'efficacia e la sicurezza del processo.
La Relazione tra Idrossido di Calcio e pH
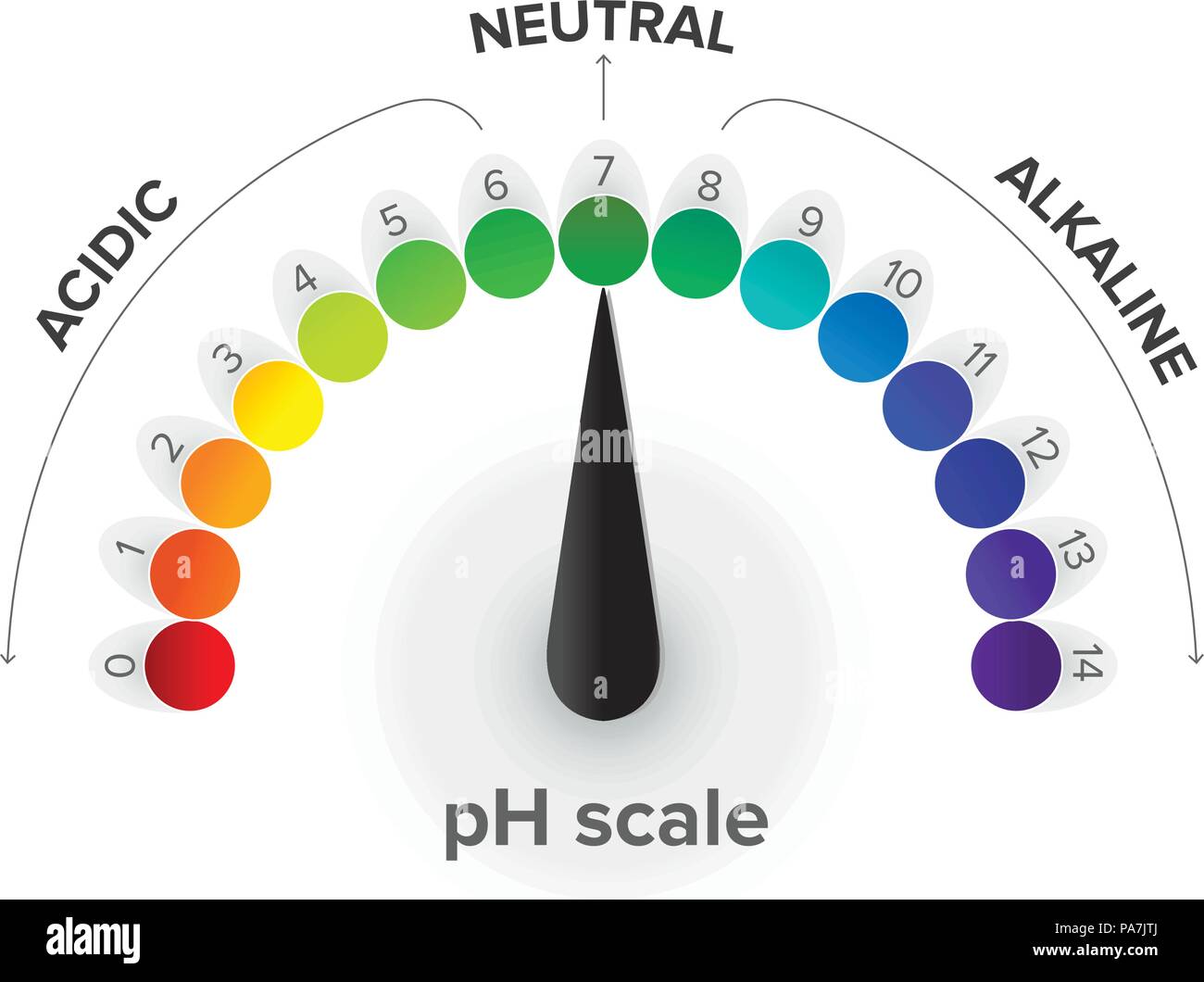
Il pH è una scala che misura il grado di acidità o basicità di una soluzione acquosa. Si basa sulla concentrazione degli ioni idrogeno (H⁺) o, in modo equivalente, degli ioni idrossido (OH⁻). In una soluzione neutra (come l'acqua pura a 25°C), la concentrazione di H⁺ è uguale a quella di OH⁻, e il pH è 7.
Le soluzioni acide hanno un pH inferiore a 7, con una maggiore concentrazione di H⁺. Le soluzioni basiche (o alcaline) hanno un pH superiore a 7, con una maggiore concentrazione di OH⁻. L'idrossido di calcio, liberando OH⁻, sposta l'equilibrio verso la basicità, aumentando il pH della soluzione.
La relazione matematica chiave che lega pH e pOH (una misura della concentrazione di OH⁻) a 25°C è:
pH + pOH = 14
E la definizione di pOH è:
pOH = -log₁₀[OH⁻]
Dove [OH⁻] è la concentrazione molare degli ioni idrossido.
Il Processo di Calcolo: Passo Dopo Passo
Ora che abbiamo una solida base teorica, passiamo al cuore del nostro articolo: il calcolo effettivo del pH di una soluzione di idrossido di calcio. Il processo richiede alcune informazioni preliminari e l'applicazione di formule specifiche.
1. Determinare la Concentrazione Molare dell'Idrossido di Calcio
Il primo passo fondamentale è conoscere la concentrazione della soluzione di idrossido di calcio. Questa viene solitamente espressa in molarità (mol/L). Se avete una concentrazione in grammi per litro (g/L), dovrete prima convertirla in moli per litro.
Per fare ciò, abbiamo bisogno della massa molare dell'idrossido di calcio. La formula chimica è Ca(OH)₂.
- Massa atomica del Calcio (Ca): circa 40.08 g/mol
- Massa atomica dell'Ossigeno (O): circa 16.00 g/mol
- Massa atomica dell'Idrogeno (H): circa 1.01 g/mol
Calcoliamo la massa molare di Ca(OH)₂:
Massa molare = (1 × Massa atomica di Ca) + (2 × Massa atomica di O) + (2 × Massa atomica di H)
Massa molare = (1 × 40.08) + (2 × 16.00) + (2 × 1.01) = 40.08 + 32.00 + 2.02 = 74.10 g/mol
Una volta nota la massa molare, potete convertire la concentrazione da g/L a mol/L:
Molarità (mol/L) = (Concentrazione in g/L) / (Massa Molare in g/mol)
2. Considerare la Dissociazione dell'Idrossido di Calcio
Qui sta un punto cruciale che distingue l'idrossido di calcio da altre basi "monoidrossilate" come NaOH o KOH. Quando l'idrossido di calcio si scioglie in acqua, si dissocia secondo l'equazione:

Ca(OH)₂(s) → Ca²⁺(aq) + 2OH⁻(aq)
Notate bene il coefficiente '2' di fronte agli ioni OH⁻. Questo significa che ogni mole di Ca(OH)₂ che si scioglie rilascia due moli di ioni idrossido in soluzione. Questa è una differenza fondamentale che influenzerà il nostro calcolo del pH.
Quindi, se la concentrazione molare iniziale dell'idrossido di calcio è CCa(OH)₂, la concentrazione molare degli ioni idrossido [OH⁻] sarà:
[OH⁻] = 2 × CCa(OH)₂
Questa è la concentrazione di OH⁻ che utilizzeremo per calcolare il pOH.
3. Calcolare il pOH
Una volta determinata la concentrazione molare degli ioni idrossido ([OH⁻]), possiamo calcolare il pOH utilizzando la formula logaritmica:
pOH = -log₁₀[OH⁻]
Ad esempio, se abbiamo calcolato che [OH⁻] = 0.01 M, allora:
pOH = -log₁₀(0.01) = -(-2) = 2
4. Calcolare il pH Finale
Ora utilizziamo la relazione fondamentale tra pH e pOH per trovare il valore del pH della nostra soluzione:
pH = 14 - pOH
Riprendendo l'esempio precedente, se il pOH è 2:
pH = 14 - 2 = 12
Un pH di 12 indica una soluzione fortemente basica, come ci aspetteremmo dall'idrossido di calcio.
Esempio Pratico: Mettiamo le Mani sulla Calce!
Per rendere tutto più concreto, facciamo un esempio completo. Immaginiamo di preparare una soluzione contenente 3.7 grammi di idrossido di calcio in 1 litro d'acqua. Vogliamo calcolare il pH di questa soluzione a 25°C.
Passo 1: Conversione della Concentrazione da g/L a mol/L
- Massa di Ca(OH)₂ = 3.7 g
- Volume della soluzione = 1 L
- Massa molare di Ca(OH)₂ = 74.10 g/mol
Molarità dell'idrossido di calcio (CCa(OH)₂) = 3.7 g / 74.10 g/mol = 0.0499 mol/L (approssimativamente 0.05 mol/L)
Passo 2: Calcolo della Concentrazione di OH⁻
Poiché Ca(OH)₂ rilascia 2 ioni OH⁻ per ogni molecola dissociata:

[OH⁻] = 2 × CCa(OH)₂ = 2 × 0.0499 mol/L = 0.0998 mol/L (approssimativamente 0.1 mol/L)
Passo 3: Calcolo del pOH
pOH = -log₁₀[OH⁻] = -log₁₀(0.0998)
Utilizzando una calcolatrice, otteniamo:
pOH ≈ -(-1.0008) ≈ 1.00
Passo 4: Calcolo del pH Finale
pH = 14 - pOH = 14 - 1.00 = 13.00
Quindi, una soluzione contenente 3.7 grammi di idrossido di calcio per litro ha un pH di circa 13.00, che è un valore altamente alcalino.
Considerazioni Importanti e Limitazioni
È importante sottolineare che questi calcoli si basano su alcune assunzioni e che ci sono fattori che possono influenzare il pH reale in diverse condizioni:
- Solubilità Limitata: Come accennato, l'idrossido di calcio non è estremamente solubile. Se tentate di sciogliere una quantità eccessiva in acqua, non tutto si dissolverà, e la soluzione rimarrà satura. Il calcolo del pH dovrebbe basarsi sulla concentrazione massima solubile in quelle specifiche condizioni, non sulla quantità totale aggiunta. La solubilità dell'idrossido di calcio diminuisce all'aumentare della temperatura.
- Effetti della Temperatura: La relazione pH + pOH = 14 è valida specificamente a 25°C. A temperature diverse, l'equilibrio ionico dell'acqua (Kw) cambia, e quindi anche questa relazione. Tuttavia, per la maggior parte delle applicazioni pratiche, l'assunzione a 25°C è sufficiente.
- Forza della Base: L'idrossido di calcio è considerato una base forte perché si dissocia quasi completamente in acqua. Questo semplifica il calcolo perché non dobbiamo preoccuparci di costanti di dissociazione acida o basica (Ka o Kb) come faremmo con acidi o basi deboli.
- Purezza del Reagente: La purezza dell'idrossido di calcio utilizzato influenzerà la concentrazione effettiva in soluzione.
Perché questo è Importante per Voi?
Capire come calcolare il pH di una soluzione di idrossido di calcio non è solo un esercizio accademico. Vi dà il potere di:
- Prevedere e controllare il comportamento chimico di questa sostanza in varie applicazioni.
- Garantire la sicurezza quando si maneggia idrossido di calcio, riconoscendo il suo potenziale corrosivo a pH elevati.
- Ottimizzare processi industriali dove l'idrossido di calcio è utilizzato per il trattamento delle acque, la neutralizzazione dell'acidità, o come reagente.
- Comprendere meglio le reazioni chimiche fondamentali che governano il nostro mondo.
Speriamo che questa guida dettagliata vi abbia fornito una comprensione chiara e pratica del calcolo del pH dell'idrossido di calcio. Ricordate, la chimica, anche nei suoi aspetti apparentemente complessi, può essere resa accessibile con il giusto approccio e gli strumenti adeguati. Ora siete equipaggiati per affrontare le soluzioni di idrossido di calcio con maggiore sicurezza e conoscenza!